Clear Sky Science · nl
Voorspelling van uitkomst op basis van ruimtelijke eiwitprofilering van triple-negatieve borstkankers
Waarom de ligging van kankercellen ertoe doet
Als artsen een agressieve borstkanker onder de microscoop bekijken, zien ze een druk landschap van tumorcellen, immuuncellen en ondersteunend weefsel. Tot voor kort richtten de meeste tests zich echter op de hoeveelheid van een bepaald molecuul, niet op waar het zich bevindt. Deze studie laat zien dat de fysieke rangschikking van eiwitten en cellen in triple-negatieve borstkankers kan voorspellen hoe patiënten het doen, en introduceert een nieuwe manier om die ruimtelijke patronen direct uit gedetailleerde beelden te lezen.
Kankergewebe in veel kleuren bekijken
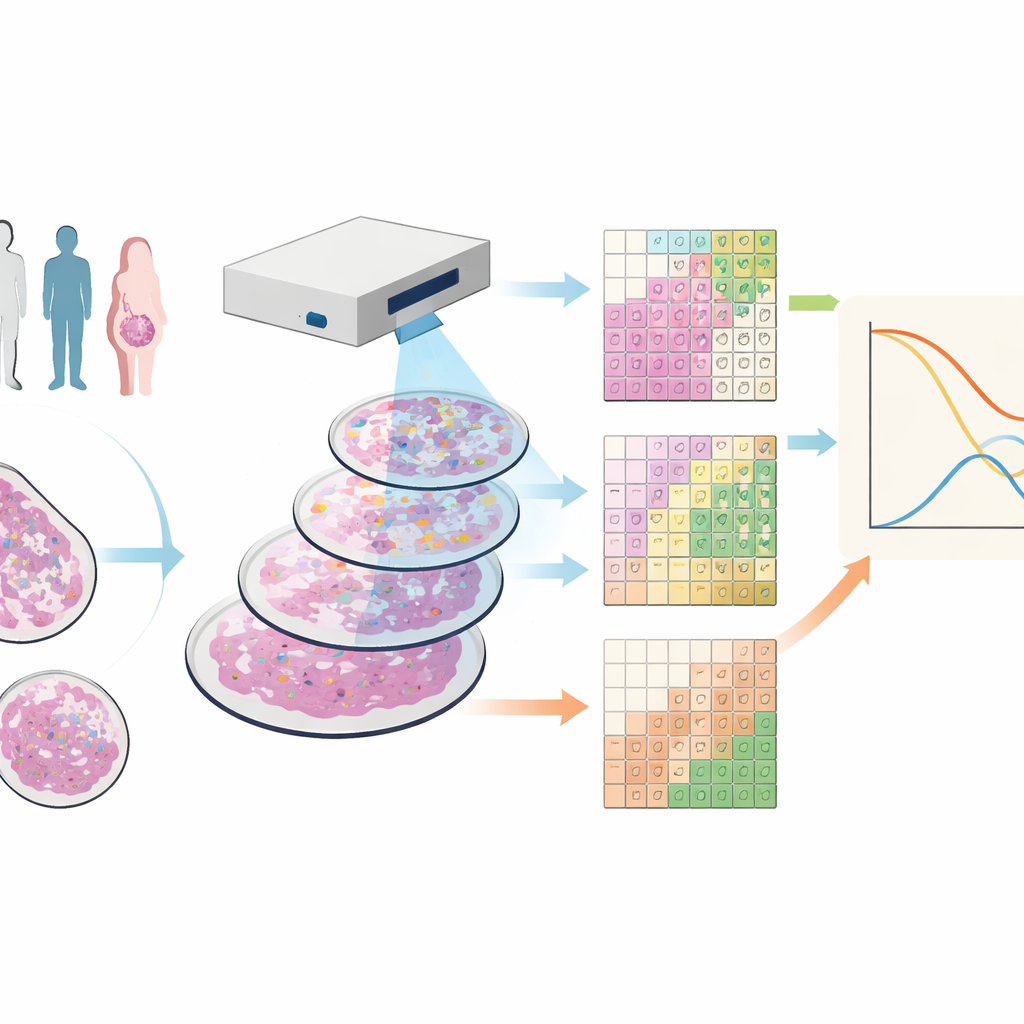
De onderzoekers werkten met weefselmonsters van 88 mensen met triple-negatieve borstkanker, een vorm van de ziekte die geen veelvoorkomende medicijndoelen heeft en vaak een slechte prognose kent. Ze gebruikten een techniek genaamd imaging mass cytometry, waarbij elk monster wordt gekleurd met tientallen metaal-gelabelde antilichamen. Onder een gespecialiseerde scanner levert dit beelden op waarbij elk punt in het weefsel een gedetailleerd vingerafdruk heeft van vele verschillende eiwitten, waardoor tumorcellen, diverse immuuncellen, bloedvaten en structurele vezels tegelijk zichtbaar worden.
Het beeld in tiles opdelen in plaats van in cellen
De meeste huidige tools proberen grenzen rond elke cel te trekken en die vervolgens per type te classificeren, een proces dat foutgevoelig en traag kan zijn, vooral in dunne weefselsnedes waarin cellen slechts gedeeltelijk voorkomen. Het team ontwikkelde in plaats daarvan SparTile, een methode die het tekenen van individuele celcontouren overslaat. SparTile verdeelt elk beeld in vele kleine overlappende vierkanten, of tiles, en gebruikt wiskundige technieken om terugkerende patronen van eiwitcombinaties binnen die tiles te leren. Eerst groepeert het tiles in brede regio’s—tumor, ondersteunend weefsel (stroma) of immuunrijke zones—en vervolgens verdeelt het elke regio verder in specifiekere "micro-omgevingen", elk met hun eigen mix van eiwitten en naburige celtypes.
Verborgen buurten gekoppeld aan patiëntuitkomst
Met deze micro-omgevingen in kaart brachten de wetenschappers in hoeveel ieder patroon in het monster van elke patiënt voorkwam en vergeleken dat met de lange-termijn overleving. Verschillende opvallende verbanden kwamen naar voren. Een tumorgecentreerde micro-omgeving rijk aan een eiwit genaamd MX1 en kenmerken van myeloïde immuuncellen was geassocieerd met een aanzienlijk hoger sterfterisico. Een ander tumorpatroon, gemarkeerd door vimentine—een teken dat tumorcellen zijn verschoven naar een meer mobiele, invasieve toestand—hing ook sterk samen met slechte overleving. Daarentegen werden gebieden gedomineerd door bepaalde T-cellen geassocieerd met betere uitkomsten, terwijl B-cel-rijke regio’s zwakkere effecten lieten zien, mogelijk omdat ze zeldzaam waren in de kleine weefselcores die werden geanalyseerd.
Afstand tussen tumor- en immuuncellen als waarschuwingsteken
Naast de aanwezigheid van bepaalde buurten waren ook hun ruimtelijke relaties van belang. Het team onderzocht hoe dicht tumorregio’s en myeloïde immuunregio’s bij elkaar lagen door een statistische maat te berekenen van hoeveel hun eiwitsignalen ruimtelijk overlappen. Patiënten wiens tumoren myeloïde-rijke gebieden hadden die dicht tussen tumorcellen lagen, deden het over het algemeen slechter dan degenen waarbij de twee populaties meer gescheiden waren. Deze "afstand"-maat bleef een sterke voorspeller van risico, zelfs nadat rekening was gehouden met standaard klinische factoren, en het belang ervan hield stand toen het werd getest op twee onafhankelijke borstkankerbeelddatasets van andere onderzoeksgroepen.
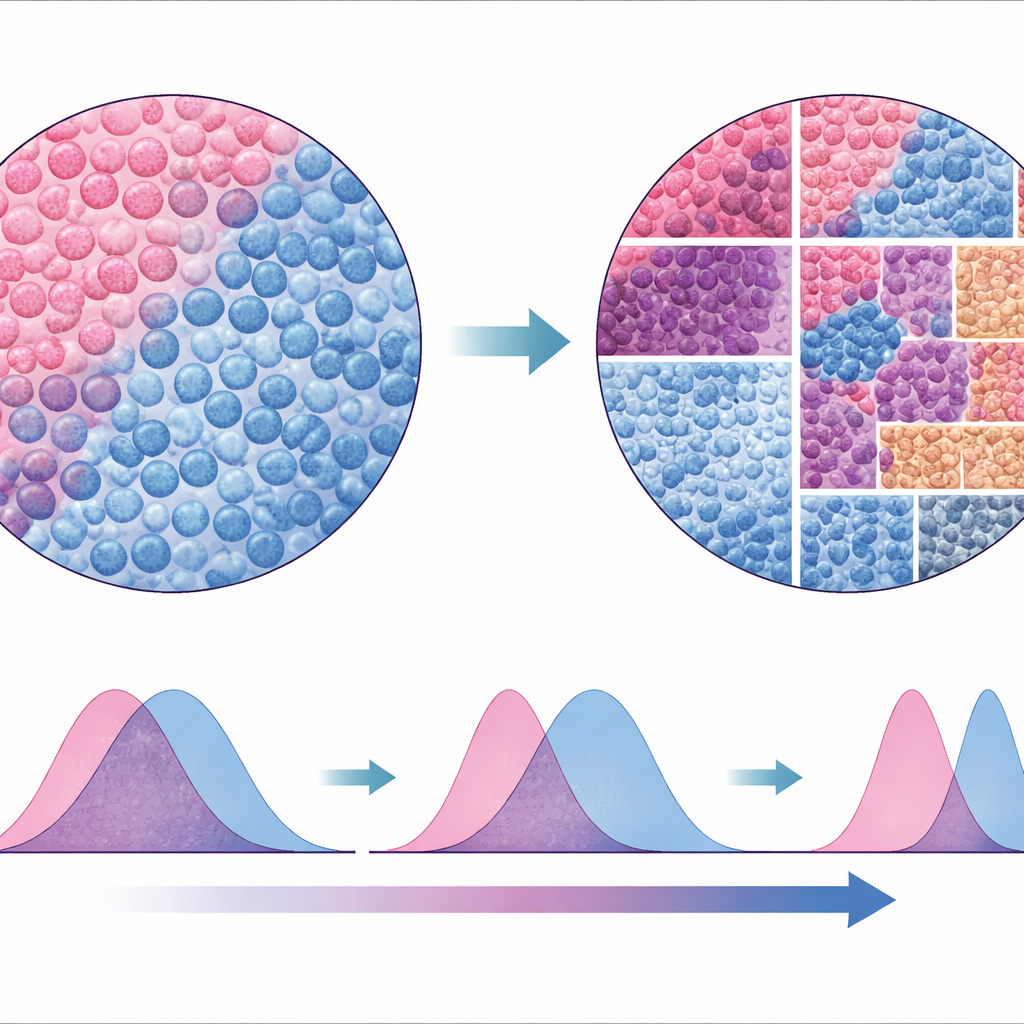
Een nieuwe manier om het tumorlandschap te lezen
Om te testen hoe robuust hun aanpak was, vergeleken de auteurs SparTile met traditionele methoden die vertrouwen op segmentatie en classificatie van individuele cellen en vervolgens het bouwen van buurten daaromheen. Hoewel de celgebaseerde analyses enkele van dezelfde patronen terugvonden, waren ze minder consistent tussen datasets en minder betrouwbaar in het signaleren van bepaalde risicovolle micro-omgevingen, zoals die met MX1 en myeloïde cellen. Doordat SparTile direct op de ruwe eiwitbeelden werkt, vermijdt het veel van de aannames en technische valkuilen van cel-voor-cel-benaderingen, maar het kan nog steeds later gecombineerd worden met die methoden wanneer gedetailleerde celtypes nodig zijn voor het plannen van experimenten of therapieën.
Wat dit betekent voor patiënten en toekomstige zorg
Dit werk toont aan dat niet alleen de ingrediënten, maar ook de indeling van een tumor van belang is voor het voorspellen hoe een patiënt met triple-negatieve borstkanker zal verlopen. Door complexe, multi-eiwitbeelden om te zetten in interpreteerbare ruimtelijke patronen en eenvoudige afstandsmetingen, biedt SparTile een manier om hoogrisicopatiënten te signaleren op basis van kleine weefselmonsters en biologische rangschikkingen te ontdekken die mogelijk door toekomstige behandelingen kunnen worden gericht. Hoewel meer validatie nodig is voordat het routinematig gebruik kan sturen, wijst de aanpak op een toekomst waarin de "kaart" van een tumor net zo belangrijk wordt als de lijst met moleculaire onderdelen.
Bronvermelding: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Trefwoorden: triple-negatieve borstkanker, tumormicroomgeving, ruimtelijke proteomica, imaging mass cytometry, prognostische biomarkers