Clear Sky Science · nl
Tekort aan homologe recombinatie in primair ER-positieve en HER2-negatieve borstkanker
Waarom dit belangrijk is voor borstkankerpatiënten
De meeste borstkankers vallen in een grote groep genaamd oestrogeenreceptor-positief en HER2-negatief. Deze tumoren worden meestal behandeld met hormoonremmende middelen, soms gecombineerd met chemotherapie. Toch krijgen veel patiënten nog steeds recidieven en ontbreekt het artsen aan nauwkeurige instrumenten om te bepalen wie echt intensieve behandeling nodig heeft of baat kan hebben bij nieuwe gerichte medicijnen. Deze studie onderzoekt een specifieke zwakte in sommige tumoren—genoemd tekort aan homologe recombinatie, of HRD—waardoor kankercellen slecht zijn in het herstellen van gebroken DNA, wat mogelijk de weg opent naar meer gepersonaliseerde behandeling.
Een verborgen zwakte in slechts enkele tumoren
Homologe recombinatie is een van de belangrijkste systemen van de cel om gevaarlijke DNA-breuken te herstellen. Wanneer dit systeem faalt—vaak door fouten in bekende genen zoals BRCA1, BRCA2, PALB2 of RAD51C—lopen cellen mutaties op en kunnen ze bijzonder gevoelig worden voor bepaalde medicijnen, waaronder platinumchemotherapieën en PARP-remmers. HRD is veelvoorkomend in een agressieve vorm van borstkanker die triple-negatief wordt genoemd, maar de rol ervan in de meer voorkomende oestrogeenreceptor-positieve, HER2-negatieve groep was onzeker. Om dit te verduidelijken, analyseerden onderzoekers 502 van dergelijke tumoren uit de Zweedse SCAN-B studie met whole-genome sequencing, samen met bijbehorende gegevens over genactiviteit, DNA-methylatie, ontvangen behandelingen en langetermijnuitkomsten.
Hoe de studie werd uitgevoerd
Alle tumoren werden verzameld op het moment van operatie, vóór enige medicamenteuze behandeling, wat een duidelijk beeld geeft van hun oorspronkelijke biologie. Het team gebruikte een geavanceerd patroonherkenningsinstrument, HRDetect, om de “mutatiesignaturen” te lezen die in kankergeen voorkomen wanneer homologe recombinatie verstoord is. Tumoren werden als HRD aangeduid als ze een strikte waarschijnlijkheidsdrempel overschreden. De wetenschappers vergeleken ook verschillende manieren om HRD te detecteren—van andere DNA-gebaseerde scores tot een RNA-gebaseerde genexpressietest—om te zien hoe betrouwbaar de methoden overeenkomen. Daarnaast onderzochten ze bredere kenmerken zoals de totale mutatielast, patronen van chromosomale winsten en verliezen, immuun-gerelateerde genactiviteit en chemische merken op DNA (methylatie) die genen aan of uit kunnen zetten.
Hoe vaak komt HRD voor en wat veroorzaakt het?
De onderzoekers vonden dat slechts 8,4% van de oestrogeenreceptor-positieve, HER2-negatieve tumoren in hun gesequenseerde groep sterke aanwijzingen voor HRD vertoonde—veel lager dan de ongeveer 60% die gezien wordt in triple-negatieve ziekte. Door deze gegevens te combineren met nationale registers en andere studies, schatten ze dat ongeveer 1 op 20 tumoren in deze klinische subgroep, en ongeveer 1 op 9 borstkankers in het algemeen in West-Europese/Noordse populaties, HRD heeft. In de HRD-tumoren konden ze vaak een waarschijnlijke oorzaak aanwijzen: ongeveer 70% had duidelijke schade aan BRCA1, BRCA2, RAD51C of PALB2, door erfelijke mutaties, tumor-specifieke mutaties of deleties, of epigenetische stillegging van genpromoters. Opvallend was dat ongeveer een derde van de HRD-gevallen werd veroorzaakt door promoter-hypermethylatie—een extra chemische laag die DNA-reparatiegenen uitschakelt zonder hun sequentie te veranderen. Echter, ruwweg 30% van de HRD-tumoren toonde geen duidelijke enkele oorzaak, wat suggereert dat er aanvullende, nog onontdekte wegen naar dit hersteltekort bestaan.
Hoe HRD-tumoren er onder de microscoop en in de kliniek uitzien
HRD-tumoren in deze veelvoorkomende borstkankergroep vertoonden vaak kenmerken van een agressievere ziekte: ze hadden vaak hogere celdelingssnelheden, lagere niveaus van hormoonreceptor-kleuring en complexere, meer gemuteerde genomen dan HR-competente tumoren. Ze kwamen voor in bijna alle grote moleculaire subtypes, maar waren zeldzaam in de meer indolente Luminal A-klasse en relatief verrijkt in een kleinere basal-achtige subset. Toch vielen HRD-tumoren, wanneer de onderzoekers keken naar algemene genactiviteit en DNA-methylatiepatronen, niet in één eenvoudig herkenbaar profiel. Hun expressiepatronen waren divers en eventuele verschillen binnen specifieke subtypes waren bescheiden. Sommige HRD-tumoren, vooral in de Luminal B- en basal-achtige groepen, toonden hogere signalen van immuunactiviteit en verhoogde expressie van PD-L1, wat suggereert dat ze zichtbaarder zijn voor het immuunsysteem en mogelijk beter reageren op immunotherapie.
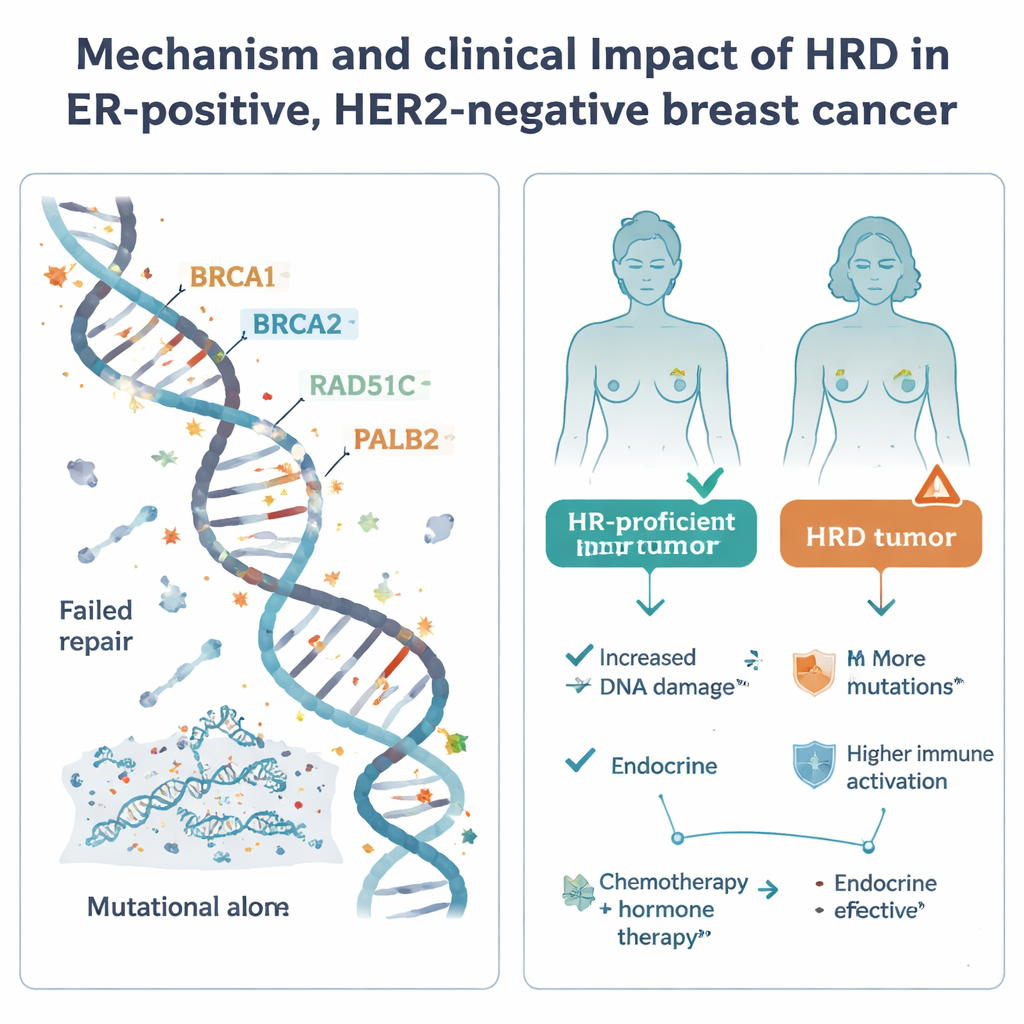
Verandert HRD de uitkomsten voor patiënten?
De studie onderzocht vervolgens hoe HRD-status gerelateerd was aan uitkomsten onder standaardzorg. Bij patiënten die na de operatie alleen hormoontherapie kregen, lieten HRD-tumoren een trend zien naar slechtere ziektevrije overleving op afstand, hoewel het aantal HRD-gevallen klein was en het resultaat geen formele statistische significantie bereikte. Dit patroon, samen met hun agressieve moleculaire kenmerken, suggereert dat alleen vertrouwen op endocriene therapie riskant kan zijn voor patiënten met HRD-tumoren. Daarentegen was bij patiënten die zowel chemotherapie als hormoontherapie kregen de HRD-status niet duidelijk gekoppeld aan betere of slechtere uitkomsten; alle groepen hadden over het algemeen vergelijkbare recidiefpercentages, en chemotherapie kan een deel van het extra risico in HRD-tumoren mitigeren.
Wat dit betekent voor toekomstige behandelkeuzes
Voor de algemene lezer is de kernboodschap dat slechts een minderheid van de oestrogeenreceptor-positieve, HER2-negatieve borstkankers deze specifieke DNA-reparatiezwakte heeft, maar wanneer die aanwezig is, markeert het vaak een agressiever ziektebeeld dat mogelijk niet goed onder controle blijft met alleen hormoontherapie. Het werk ondersteunt het idee dat whole-genome sequencing HRD betrouwbaar kan aantonen en de onderliggende oorzaken kan verhelderen, verder dan alleen testen op erfelijke BRCA1- of BRCA2-mutaties. Hoewel de studie nog niet aantoont dat het aanpassen van de behandeling op basis van HRD-status de overleving verbetert, levert het vroege aanwijzingen dat patiënten met HRD-tumoren kunnen profiteren van chemotherapie en, in toekomstige trials, van PARP-remmers of immunotherapieën. Kort gezegd zou HRD-testen een onderdeel kunnen worden van een verfijndere toolkit om de intensiteit van therapie—en nieuwe gerichte opties—af te stemmen op de biologie van de borstkanker van iedere patiënt.
Bronvermelding: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Trefwoorden: borstkanker, DNA-reparatie, BRCA-genen, genoomsequencing, gerichte therapie