Clear Sky Science · nl
Op oppervlakte aangepaste, dubbel-beladen, tumorgerichte liposomale nanodeeltjes om therapeutische resistentie bij glioblastoma multiforme te overwinnen
Waarom dit onderzoek naar hersenkanker ertoe doet
Glioblastoom is een van de dodelijkste vormen van hersenkanker. Zelfs met operatie, bestraling en chemotherapie leven de meeste patiënten weinig meer dan een jaar na de diagnose. Een groot probleem is dat standaardmedicijnen vaak de tumor in de hersenen niet bereiken, en zelfs wanneer ze dat wel doen, past de tumor zich snel aan en wordt resistent. Deze studie onderzoekt een nieuwe methode om meerdere medicijnen langs de natuurlijke barrières van de hersenen te smokkelen en ze in de tumor te concentreren, met als doel bestaande behandelingen zoals bestraling veel effectiever te maken.
Een minuscuul bezorgbusje voor kankergeneesmiddelen
De onderzoekers bouwden ultrasmall geneesmiddel-dragers genaamd tumorgerichte liposomen. Dit zijn zachte, vetachtige belletjes op de schaal van miljardsten van een meter die medicijnen binnenin kunnen bevatten. Het team modificeerde het oppervlak van deze belletjes met een speciaal peptide dat glioblastoomcellen herkent en eraan hecht, waardoor de deeltjes zich op tumoren richten in plaats van op gezond weefsel. Elk belletje was ontworpen om twee kankergeneesmiddelen tegelijk te vervoeren: ofwel everolimus plus vinorelbine, of rapamycine plus vinorelbine. Het idee is dat de twee medicijnen de tumorcellen op complementaire manieren aanvallen, terwijl de beschermende schaal de middelen helpt te overleven in de bloedbaan en in de hersenen te sluipen.
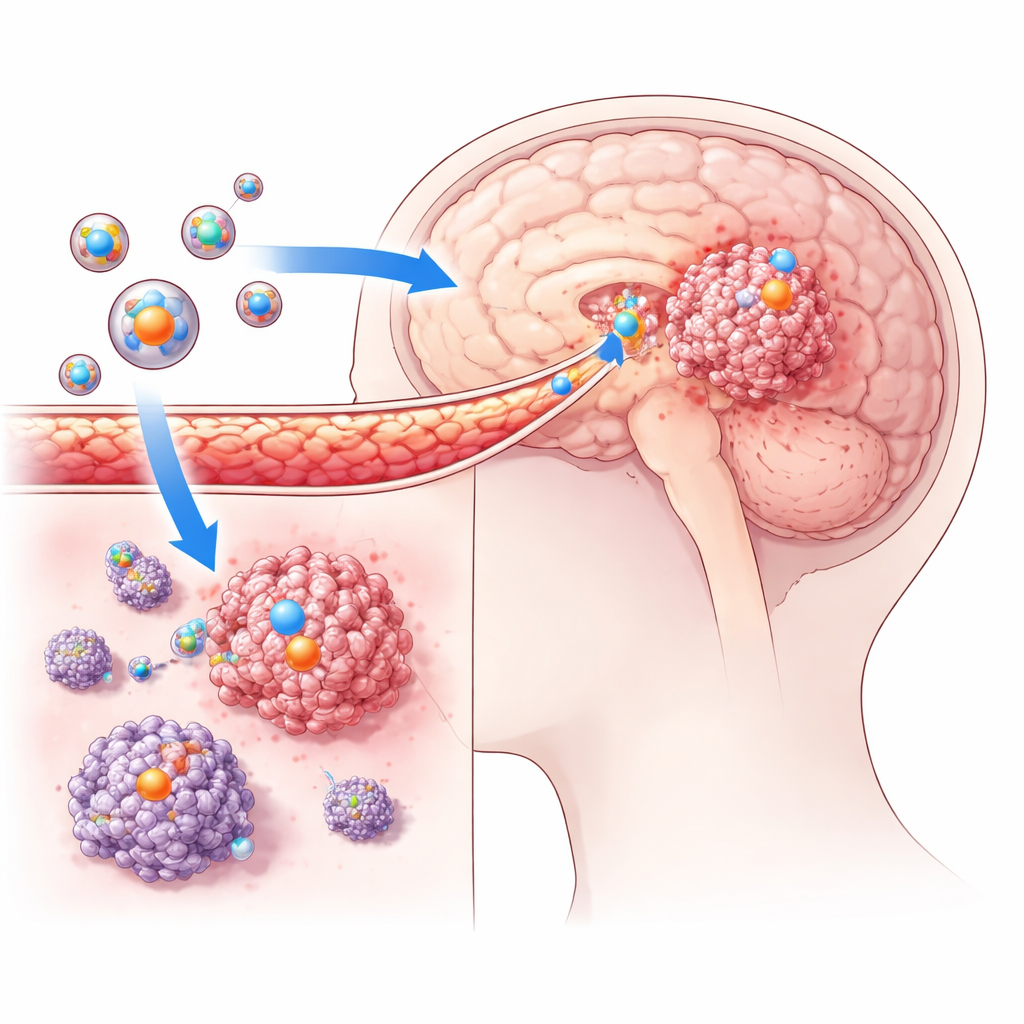
De beschermende wand van de hersenen passeren
Met muismodellen waarin menselijke glioblastoomcellen waren geïmplanteerd, testte het team of deze liposomen daadwerkelijk tumoren in de hersenen konden bereiken. Ze labelden de deeltjes met fluorescerende kleurstoffen en volgden hun reis met behulp van geavanceerde beeldvormingstechnieken. In vergelijking met niet-gerichte liposomen vertoonden de tumorgerichte versies veel sterkere signalen binnen de hersentumoren en weinig signaal in normale hersengebieden. Dit bevestigde dat de ontworpen deeltjes de bloed-hersenbarrière konden passeren en zich specifiek ophoopten waar de kankercellen groeiden. In celkweekexperimenten namen glioblastoomcellen ook veel meer van de gerichte liposomen op dan van de controledeeltjes, wat het idee versterkt dat het oppervlaktepeptide tumorgerichtheid en opname sterk verbetert.
De tumor harder raken en de rest van het lichaam sparen
De wetenschappers vergeleken eerst hoe goed enkelvoudig geladen en dubbel-beladen liposomen kankercellen in kweek vernietigden. De dubbel-beladen versies, met name de combinatie everolimus–vinorelbine, waren krachtiger dan elk middel afzonderlijk en werkten beter dan dezelfde middelen buiten de liposomale drager. In combinatie met bestraling was het effect nog sterker: kankercellen vormden veel minder kolonies, bewoog minder en vertoonde tekenen van grotere schade. In muizen met hersentumoren hadden dieren die werden behandeld met dubbel-beladen liposomen plus bestraling een tragere tumorprogressie en leefden ze langer dan dieren die alleen bestraling, alleen liposomen of standaardchemotherapie met temozolomide kregen. Belangrijk is dat de onderzoekers geen duidelijke schade in andere organen zagen, wat suggereert dat het concentreren van de behandeling in de tumor bijwerkingen kan verminderen.
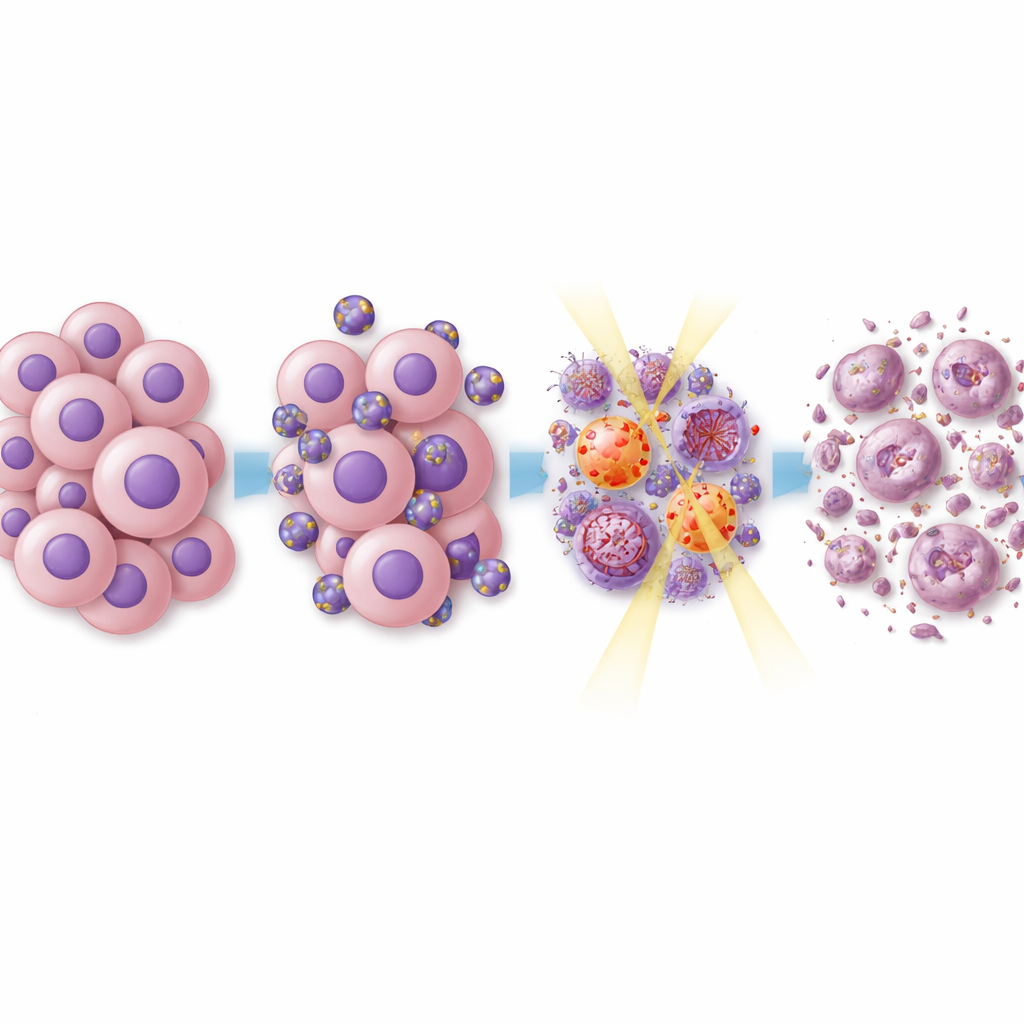
Wat er binnen in de kankercellen gebeurt
Om te begrijpen waarom deze benadering tumoren gevoeliger maakte voor behandeling, onderzocht het team sleutelroutes van signaaloverdracht binnen de kankercellen. Everolimus en rapamycine staan bekend als remmers van het mTOR-pad, dat cellen helpt groeien en weerstand te bieden aan stress. De dubbel-beladen liposomen onderdrukten mTOR-gerelateerde signalen, evenals andere groeipaden die de deling en beweging van glioblastoomcellen aansturen. Wanneer bestraling werd toegevoegd, werden ook eiwitten die betrokken zijn bij DNA-schadeherstel verzwakt. Dat betekent dat de tumorcellen minder in staat waren de genetische schade veroorzaakt door bestraling te herstellen, waardoor ze naar celdood werden geduwd in plaats van herstel. Gedetailleerde analyses van genactiviteit in behandelde tumoren toonden brede veranderingen in netwerken die verband houden met celcycluscontrole, DNA-reparatie en de interactie van de tumor met het immuunsysteem, en veel genen die met behandelresistentie geassocieerd zijn, werden naar beneden gereguleerd.
Wat dit voor toekomstige patiënten kan betekenen
Dit werk toont aan dat zorgvuldig ontworpen, tumorzoekende nanodeeltjes twee samenwerkende medicijnen over de beschermende barrière van de hersenen kunnen vervoeren, ze in glioblastomen kunnen concentreren en bestraling effectiever kunnen maken. Bij muizen vertraagde deze strategie de tumorgroei en verlengde de overleving zonder duidelijke toegevoegde toxiciteit. Hoewel deze resultaten nog preklinisch zijn en veel meer testen nodig zijn voordat toepassing bij mensen mogelijk is, wijst de studie op een praktische manier om gerichte medicijnaflevering te combineren met bestaande behandelingen om een zeer resistente kanker te slim af te zijn. Als vergelijkbare voordelen bij mensen worden aangetoond, zouden dergelijke dubbel-beladen liposomen patiënten met glioblastoom ooit langere en kwalitatief betere levens kunnen bieden.
Bronvermelding: Angom, R.S., Rachamala, H.K., Nakka, N.M.R. et al. Surface-engineered dual drug-loaded tumor-targeted liposomal nanoparticles to overcome the therapeutic resistance in glioblastoma multiforme. Commun Med 6, 152 (2026). https://doi.org/10.1038/s43856-025-01279-7
Trefwoorden: glioblastoom, nanodeeltjes, liposomen, behandeling van hersenkanker, verhoging van radiosensitiviteit