Clear Sky Science · nl
Subtypen van de ziekte van Alzheimer en de ziekte van Parkinson bepalen met longitudinale elektronische patiëntendossiers
Waarom dit belangrijk is voor families en patiënten
Over de ziekte van Alzheimer en de ziekte van Parkinson wordt vaak gesproken alsof het één uniforme aandoening betreft. Maar wie een dierbare heeft zien achteruitgaan weet dat geen twee trajecten hetzelfde zijn. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen de medische dossiers die we al jarenlang verzamelen verborgen “varianten” van deze hersenziekten blootleggen, op een manier die mogelijk kan leiden tot meer op maat gemaakte zorg? Met moderne patroonherkenningstools op de gezondheidsverhalen van meer dan 100.000 mensen in het Verenigd Koninkrijk tonen de auteurs aan dat zowel Alzheimer als Parkinson in elk vijf onderscheiden subtypen kunnen worden opgedeeld, met verschillende risico’s, symptomen en waarschijnlijke toekomstbeelden.
De gezondheidsverhalen van mensen tientallen jaren volgen
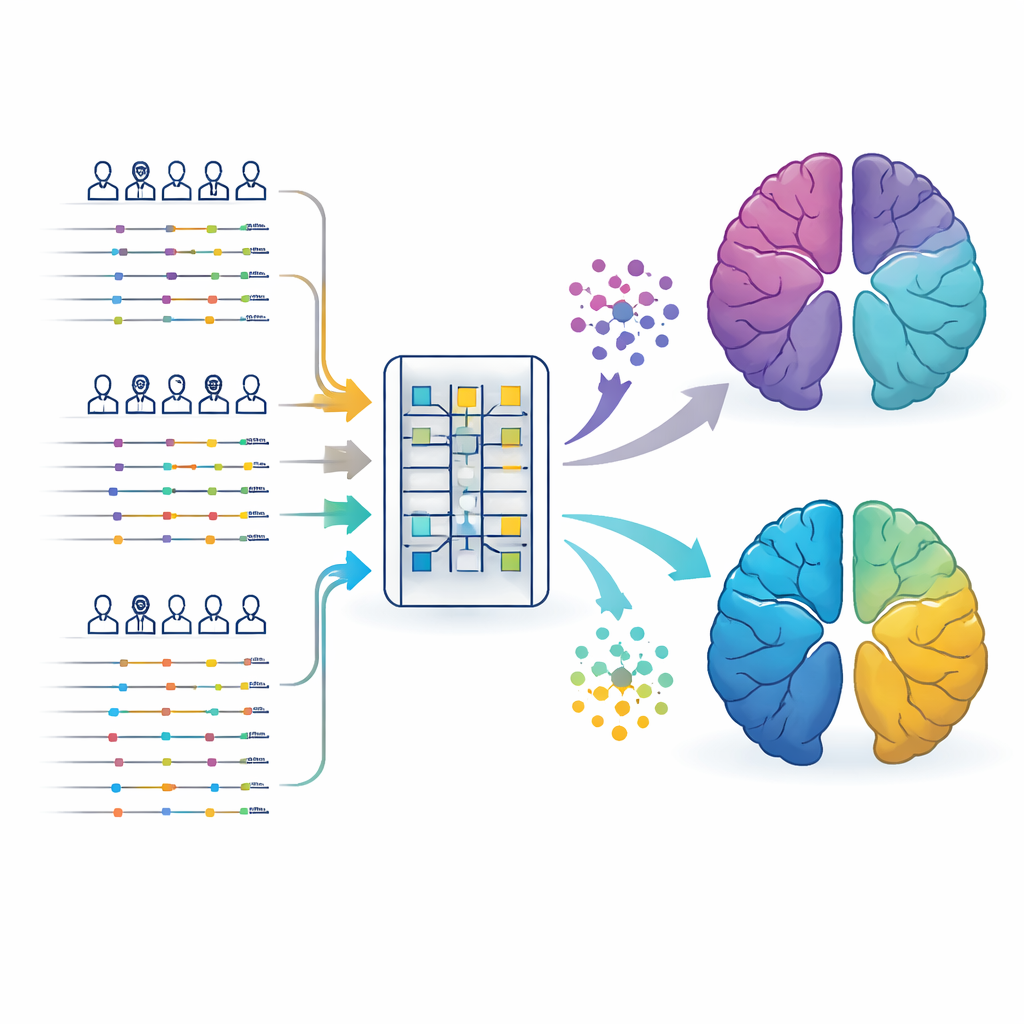
De onderzoekers gebruikten geanonimiseerde elektronische patiëntendossiers uit twee grote Britse bronnen: de Clinical Practice Research Datalink, die gegevens van huisartsen bevat, en de UK Biobank, een langlopend onderzoeksproject dat poliklinische bezoeken, ziekenhuisopnames, voorschriften en genetische data koppelt. Ze concentreerden zich op meer dan 113.000 mensen met de ziekte van Alzheimer en ruim 45.000 met de ziekte van Parkinson, elk met twee tot drie decennia aan medische voorgeschiedenis vóór de diagnose. In plaats van alleen naar testresultaten te kijken die pas na herkenning van de hersenziekte zijn afgenomen, voerde het team deze lange, tijdgestempelde gezondheids“verhalen” in een transformer, een type kunstmatige intelligentie dat goed is in het begrijpen van reeksen zoals taal of, in dit geval, een tijdlijn van doktersbezoeken.
De data patiënten laten indelen in verborgen groepen
Uit elk persoonsdossier maakte het model een compact numeriek “vingerafdruk” dat patronen van ziekten, medicatie en timing vastlegde. Een clusteringmethode sorteerde deze vingerafdrukken vervolgens in groepen zonder vooraf te worden verteld waar naar gezocht moest worden. Voor zowel Alzheimer als Parkinson bleek de meest stabiele en reproduceerbare oplossing telkens vijf subtypen. Eén groep in elke ziekte leek op een klassiek, grotendeels “zuiver” hersenaandoeningstype: mensen hadden sterkere genetische risicoscores maar relatief weinig andere medische problemen en deden het beter na diagnose. Andere groepen werden gekenmerkt door patronen die jaren eerder zichtbaar waren, zoals uitgesproken vaatziekten, metabole problemen zoals diabetes en obesitas, of een lange voorgeschiedenis van angst en depressie.
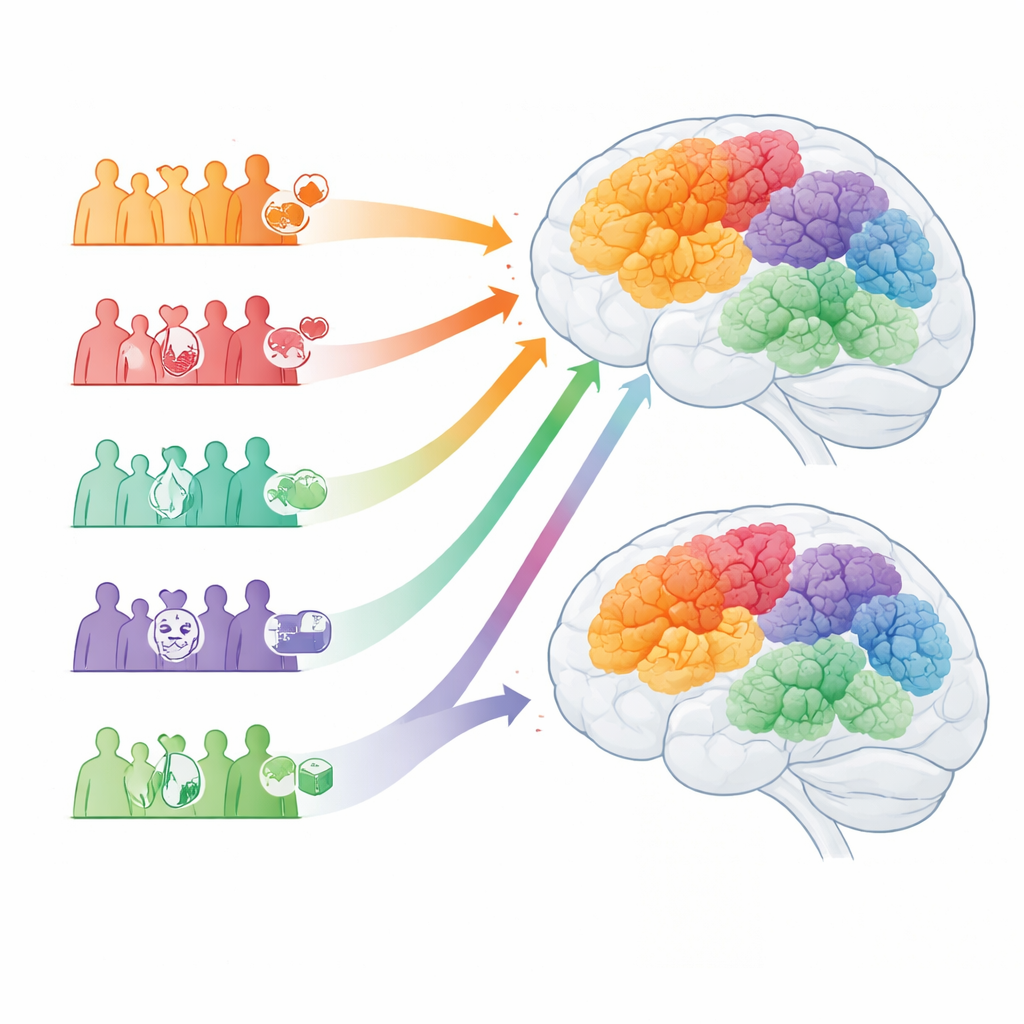
Verschillende paden, verschillende uitkomsten
De vijf Alzheimer-subtypen varieerden van een veelvoorkomend laatoptredend type met minder comorbiditeiten, tot een door vaatproblemen gedomineerd patroon met wijdverspreide hoge bloeddruk, tot een “geestelijke gezondheid”-vorm gekenmerkt door prominente depressie, angst en snellere achteruitgang van denkvermogen. Een ander subtype was sterk gekoppeld aan diabetes, nierziekte en tekenen van chronische ontsteking, ondanks een lager aangeboren risico; deze patiënten werden vaak eerder ziek en overleden eerder. Een laatste Alzheimergroep toonde meer hart- en bewegingsproblemen en had de hoogste ziekenhuisopname- en sterftecijfers. De Parkinson-subtypen weerspiegelden deze thema’s: één groep met relatief ‘schone’ medische geschiedenissen en hoger genetisch risico, één gedomineerd door hoge bloeddruk en vaataandoeningen, één met ernstige stemmings- en bewegingsproblemen, één met sterke metabole en inflammatoire kenmerken, en één die ernstige hart- en bewegingsproblemen combineerde met bijzonder slechte overleving.
Genen en gedeelde risicofactoren tussen hersenziekten
Aangezien de UK Biobank DNA-data bevat, konden de auteurs nagaan of deze klinisch gedefinieerde subtypen ook biologisch van elkaar verschilden. In beide aandoeningen hadden alle patiëntengroepen hogere ziektegerelateerde genetische risicoscores dan mensen zonder diagnose, zoals verwacht. Toch droegen sommige clusters bijzonder sterke of zwakke genetische signalen. Zo had een “metabool–inflammatoir” Alzheimersubtype lagere scores voor klassieke Alzheimer-risicogenen en was relatief verrijkt voor een beschermende vorm van het APOE-gen, wat suggereert dat levenslange aandoeningen zoals diabetes en obesitas een dementieachtig beeld kunnen veroorzaken zelfs wanneer het erfelijke risico beperkt is. Over zowel Alzheimer als Parkinson heen kwamen subtypen die werden gevormd door hoge bloeddruk, beroerterisico of stemmingsstoornissen op vergelijkbare wijze terug, wat erop wijst dat vaatgezondheid, metabolisme en geestelijke gezondheid het brein in de richting van verschillende degeneratiepatronen kunnen duwen in plaats van louter bijverschijnselen van veroudering te zijn.
Wat dit voor toekomstige zorg kan betekenen
Dit werk verandert nog niet hoe artsen patiënten aan het bed diagnosticeren, en de auteurs benadrukken dat medische dossiers op zichzelf niet het exacte biologische mechanisme achter elk subtype kunnen bewijzen. Toch laat de studie zien dat routinematige langetermijngegevens op natuurlijke wijze in consistente, betekenisvolle groepen vallen die overeenkomen met verschillen in symptomen, overleving en genetica. Dat biedt een blauwdruk voor preciezere, vroege risicoprofielen. In de toekomst kunnen mensen met bepaalde combinaties van vaatziekten, diabetes of stemmingsproblemen nauwer worden gevolgd op specifieke patronen van Alzheimer of Parkinson, en kunnen geneesmiddelenonderzoeken subtypen targeten die het meest waarschijnlijk baat hebben. Kort gezegd ondersteunen de bevindingen een verschuiving van het behandelen van deze aandoeningen als één monolithische ziekte naar het zien ervan als families van verwante maar onderscheiden paden — wat de deur opent naar meer gepersonaliseerde preventie en therapie.
Bronvermelding: Lian, J., Fan, Z., Petrazzini, B.O. et al. Subtyping Alzheimer’s disease and Parkinson’s disease using longitudinal electronic health records. Nat Aging 6, 612–625 (2026). https://doi.org/10.1038/s43587-026-01085-3
Trefwoorden: Subtypen van de ziekte van Alzheimer, Subtypen van de ziekte van Parkinson, elektronische patiëntendossiers, machine learning in de neurologie, risicofactoren voor neurodegeneratie