Clear Sky Science · nl
Structureel kenmerk van plasmaleiwitten classificeert de status van de ziekte van Alzheimer
Waarom een bloedtest voor geheugenverlies ertoe doet
De ziekte van Alzheimer is vaak al ver gevorderd lang voordat geheugenproblemen duidelijk worden, maar de huidige tests om die vroeg te detecteren kunnen invasief, duur of moeilijk toegankelijk zijn. Deze studie onderzoekt een ander idee: of kleine veranderingen in de driedimensionale vormen van eiwitten die in ons bloed circuleren kunnen onthullen waar iemand zich bevindt op het traject van gezond ouder worden naar milde vergeetachtigheid tot volledige ziekte van Alzheimer. Als dit lukt, zou zo’n bloedtest screening eenvoudiger kunnen maken, vroege behandeling ondersteunen en onderzoekers helpen te volgen wie baat heeft bij nieuwe therapieën.
Kijken naar eiwitvorm, niet alleen hoeveelheid
De meeste bloedtests meten hoeveel van een bepaalde molecule aanwezig is. Hier richtten wetenschappers zich in plaats daarvan op de vorm van eiwitten. Binnen onze cellen houdt een kwaliteitscontrolesysteem eiwitten goed gevouwen; wanneer dit systeem met de leeftijd hapert, kunnen verkeerd gevouwen eiwitten zich ophopen en hersencellen beschadigen. Het team vroeg zich af of deze ineenstorting van de “eiwithuishouding” een structurele vingerafdruk achterlaat in bloedproteïnen. Van 520 vrijwilligers die ofwel cognitief gezond waren, milde cognitieve stoornis (MCI) hadden of de ziekte van Alzheimer hadden, werd bloed afgenomen en werd een chemische techniek genaamd covalente eiwitprofilering gebruikt om blootgestelde delen van eiwitten te labelen. Hoe meer een plaats blootligt, hoe gemakkelijker deze gelabeld wordt, wat een numerieke weergave geeft van de eiwitvorm die grotendeels onafhankelijk is van de hoeveelheid aanwezig eiwit.
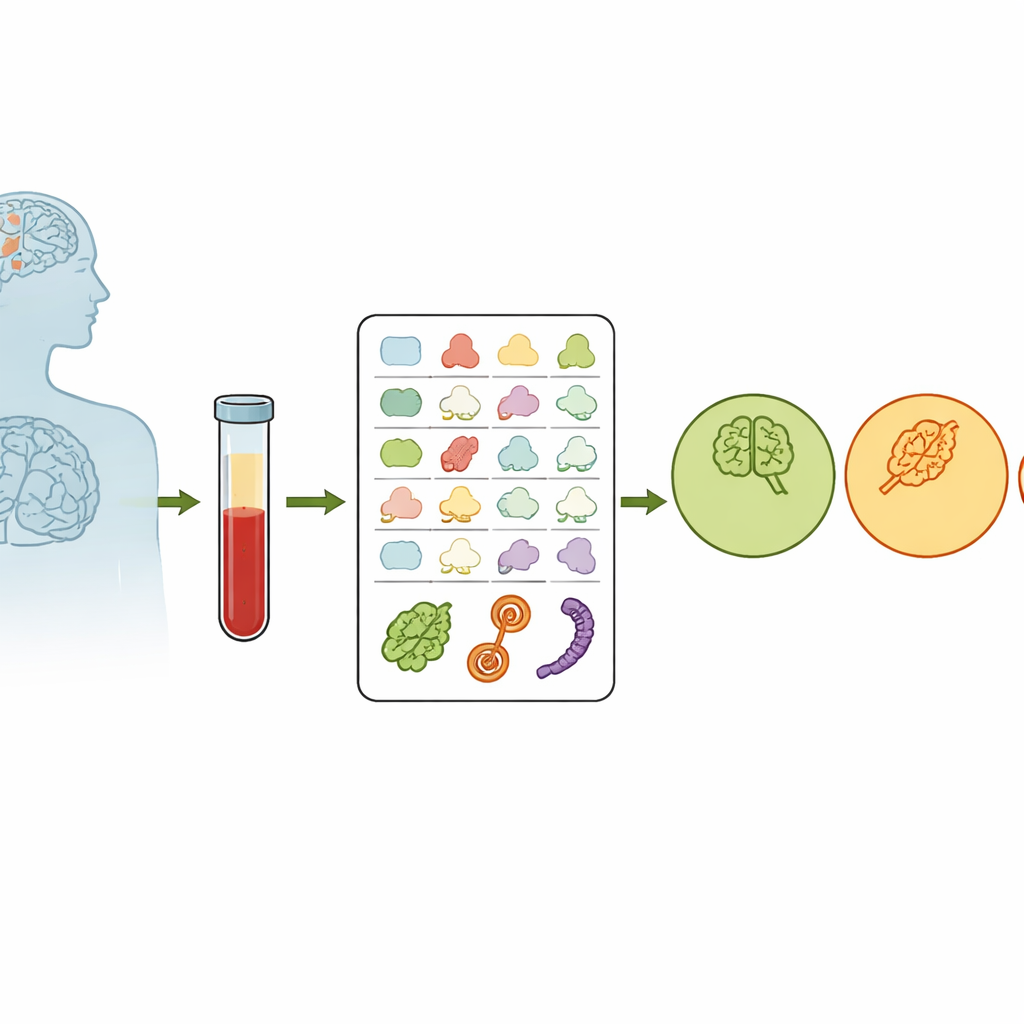
Structurele vingerafdrukken in het bloed vinden
Over bijna 900 gelabelde eiwitfragmenten zagen de onderzoekers een subtiele maar consistente trend: naarmate mensen van gezond naar MCI naar Alzheimer gingen, werden bepaalde eiwitoppervlakken minder blootgelegd en meer variabel tussen personen. Dit patroon past bij het idee dat de eiwitvouwingcontrole van het lichaam verslechtert naarmate de ziekte vordert. Het team onderzocht ook hoe een belangrijke genetische risicofactor voor Alzheimer, de APOE ε4-variant, de eiwitstructuur beïnvloedde. Ze ontdekten dat mensen met twee kopieën van ε4 opvallende structurele verschuivingen vertoonden in verschillende eiwitten die met het APOE-eiwit interageren, wat suggereert dat dit risicogene niet alleen bepaalt welke eiwitten aanwezig zijn, maar ook hoe ze gevouwen en gerangschikt zijn.
Het koppelen van bloedproteïnen aan stemming en gedrag
Alzheimer raakt veel meer dan geheugen; symptomen zoals agitatie, depressie en hallucinaties komen vaak voor en verschillen vaak tussen mannen en vrouwen. De onderzoekers combineerden klinische beoordelingen van 12 soorten neuropsychiatrische symptomen met hun metingen van eiwitvorm. In beide geslachten gingen ernstigere symptomen vaak samen met eiwitten die structureel meer “afgesloten” raakten. Sommige eiwitten, waaronder clusterine en verschillende anderen die met amyloïdeophoping zijn verbonden, volgden de ernst van symptomen op vergelijkbare wijze bij mannen en vrouwen, terwijl andere geslachtspecifieke patronen lieten zien. Deze bevindingen suggereren dat de structuur van bloedproteïnen mogelijk niet alleen de aanwezigheid van de ziekte weerspiegelt, maar ook hoe die zich uit in gedrag en stemming.
Een driestoffenpanel om ziektestadium te classificeren
Om deze complexe metingen klinisch bruikbaar te maken, voerde het team de structurele data in 18 verschillende machine-learningbenaderingen. Het best presterende model, gebaseerd op deep learning, vertrouwde op slechts drie eiwitfragmenten afkomstig van C1QA, clusterine (ook CLUS genoemd) en apolipoproteïne B (ApoB). Alleen met de structurele readouts van deze drie fragmenten sorteerde het model mensen in een onafhankelijke testset ongeveer 83% van de tijd correct in gezonde, MCI- of Alzheimer-groepen. Bij eenvoudiger tweerichtingsvragen—zoals het onderscheiden van gezond versus MCI, of MCI versus Alzheimer—was de prestatie van het panel nog sterker, met nauwkeurigheidsmaten die vergelijkbaar waren met of beter dan veel huidige bloedgebaseerde benaderingen die zich richten op eiwithoeveelheden in plaats van structuur.
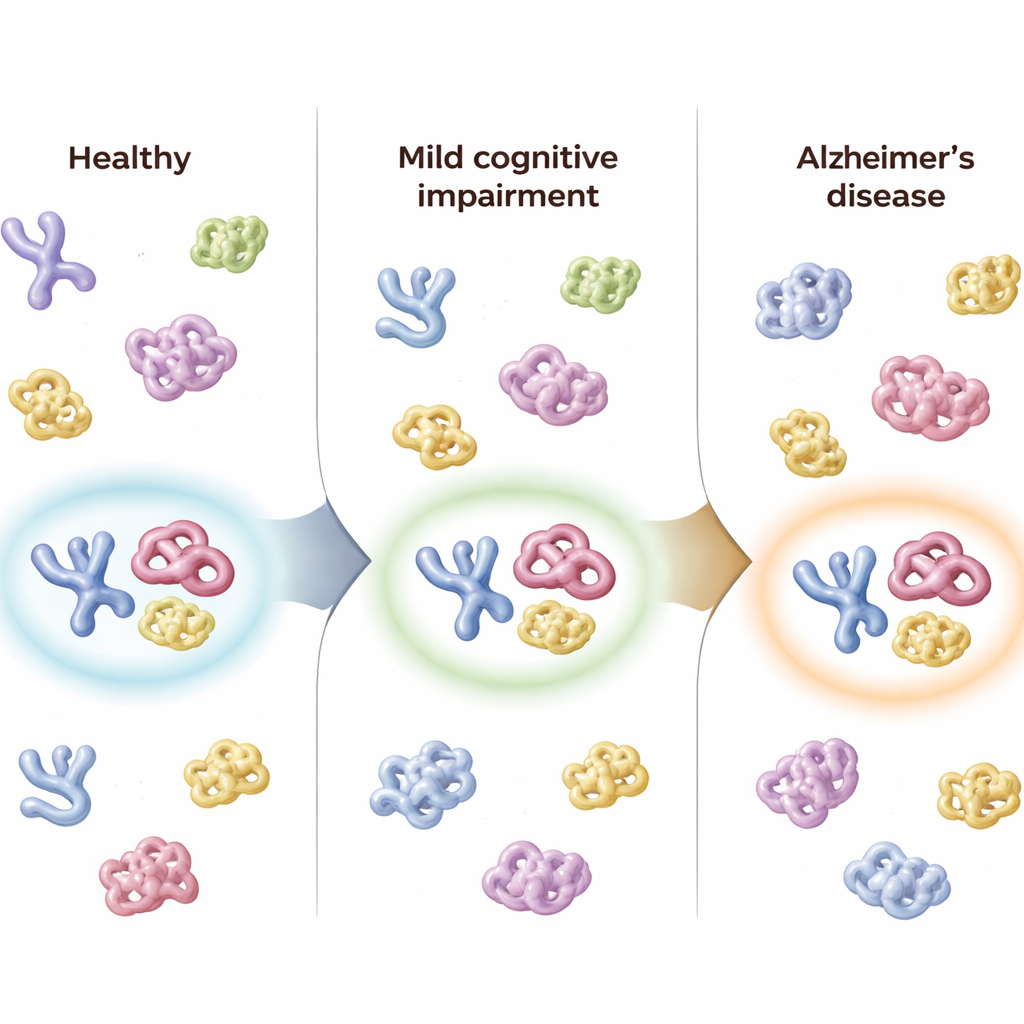
Mensen in de loop van de tijd volgen
De onderzoekers beschikten ook over vervolgmonsters van 50 deelnemers die tot ongeveer acht maanden later werden genomen. Bij mensen waarvan de diagnose verslechterde—bijvoorbeeld van gezond naar MCI, of van MCI naar Alzheimer—verschoof de gecombineerde score van het driestoffenpanel in dezelfde richting, wat de ziekteprogressie weerspiegelde. Daarentegen vertoonden individuen van wie de klinische status hetzelfde bleef weinig verandering in hun panelscores. De algehele “Alzheimer-confidence”-score van het panel volgde nauw cognitieve standaardscores, met maten van dagelijkse functioneren, met hersenkrimp zichtbaar op MRI-scans en met gevestigde ruggenmergvochtmarkers van amyloïde en tau, wat suggereert dat het structurele signaal in bloed de onderliggende hersenveranderingen weerspiegelt.
Wat dit voor patiënten kan betekenen
Samengevat laat het werk zien dat kleine, gecoördineerde veranderingen in de vormen van slechts een paar veelvoorkomende bloedproteïnen betrouwbaar kunnen aangeven of iemand cognitief gezond is, licht aangetast is of de ziekte van Alzheimer heeft. Omdat de test bloed gebruikt in plaats van ruggenmergvocht of beeldvorming van de hersenen, zou hij in principe opgeschaald kunnen worden voor routinematige screening of om deelnemers in klinische proeven te selecteren en te volgen. De auteurs waarschuwen dat grotere en langere studies nodig zijn en dat de gebruikte chemie nog gespecialiseerd is. Niettemin wijzen hun resultaten op eiwitstructuur—niet alleen eiwithoeveelheden—als een veelbelovende nieuwe informatiebron om de ziekte van Alzheimer eerder en nauwkeuriger op te sporen en te volgen.
Bronvermelding: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
Trefwoorden: Biomarkers voor de ziekte van Alzheimer, bloedtest voor dementie, veranderingen in vouwing van eiwitten, machine learning diagnose, clusterine en C1QA