Clear Sky Science · nl
Weerstand tegen platina-gebaseerde chemotherapie bij long- en eierstokkanker wordt aangedreven door een targeteerbaar TGFβ-senescente secretoom
Wanneer kankerbehandeling averechts werkt
Platina-gebaseerde chemotherapie is een van de pijlers van moderne kankerbehandeling, vooral bij long- en eierstokkanker. Het is ontworpen om het DNA van tumoren zo ernstig te beschadigen dat kankercellen zich niet meer kunnen delen. Toch zien veel patiënten aanvankelijk een krimp van hun tumoren, om vervolgens een terugkeer van de ziekte te ervaren, die harder is dan voorheen. Deze studie stelt een eenvoudige maar verontrustende vraag: kunnen dezelfde medicijnen die levens redden ook overlevende kankercellen helpen terugveren? Het antwoord, zo vinden de auteurs, ligt bij een speciale groep beschadigde, verouderingsachtige cellen en de krachtige chemische signalen die zij afgeven.
Het dubbele leven van verouderende kankercellen
Chemotherapie treft niet alle tumorcellen op dezelfde manier. Sommige worden direct gedood, maar andere treden een toestand binnen die cellulair senescentie wordt genoemd—permanent gestopt met delen, maar nog steeds levend. Deze senescente cellen zwellen op en beginnen een mengsel van eiwitten en signalen af te scheiden dat bekendstaat als het senescence-associated secretory phenotype, ofwel SASP. Met behulp van menselijke long- en eierstokkankercellen in het lab en muismodellen toonden de onderzoekers aan dat platina‑middelen zoals cisplatine en carboplatine bijzonder krachtige senescente cellen induceren. Wanneer verse kankercellen werden blootgesteld aan het medium afkomstig uit deze senescente kweek, groeiden ze sneller, migreerden ze makkelijker en vormden ze grotere, agressievere klonten en sferen dan controlecellen.
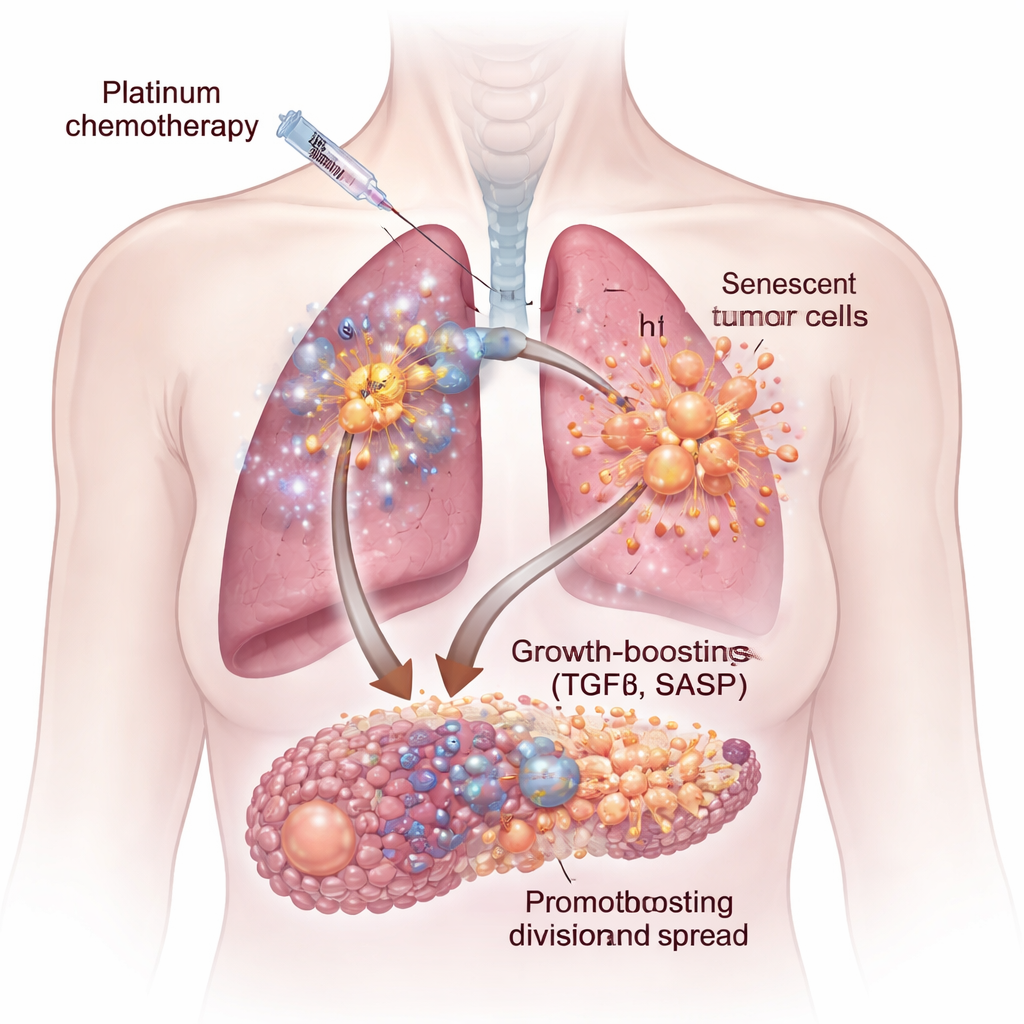
Een verborgen groeisignaal: TGFβ
Niet alle chemotherapieën veroorzaakten dezelfde schadelijke afscheidingen. Toen het team platina-middelen vergeleek met twee andere veelgebruikte middelen, docetaxel en palbociclib, produceerden alleen de platina-behandelde cellen een SASP die de tumorgroei sterk versterkte. Door genexpressiestudies, eiwitmetingen en een high-throughput microenvironment-microarray te combineren, identificeerden ze een hoofdverdachte: het signaalmolecuul transforming growth factor‑beta, of TGFβ. Senescente cellen geïnduceerd door cisplatine waren verrijkt met meerdere vormen van TGFβ en gerelateerde pathways. Het toevoegen van gezuiverd TGFβ aan kankercellen imiteerde de groeiboost die gezien werd met het senescente-cell-medium, waarmee deze cytokinefamilie als centrale motor van het pro‑tumor secretoom naar voren kwam.
Hoe het signaal kankercellen herprogrammeert
De studie volgde vervolgens hoe deze TGFβ-rijke signalen het gedrag van naburige tumorcellen veranderen. Op het oppervlak van ontvangende cellen bindt TGFβ aan een receptor genaamd TGFBR1. Dit schakelt op zijn beurt een interne keten van eiwitten in—met name de AKT- en mTOR-pathways—die bekendstaan om hun rol in celgroei, metabolisme en overleving. Zowel in menselijke als muis-longkankercellen verhoogde blootstelling aan cisplatine-afgeleide secreties snel de geactiveerde (gefosforyleerde) vormen van AKT en zijn downstream target p70S6K, en versterkte de expressie van celcyclusgenen. Het blokkeren van TGFBR1 met een middel genaamd galunisertib, of het direct remmen van mTOR, schakelde deze signalering grotendeels uit en verminderde de extra proliferatie, kolomvorming en invasieve sfeergroei die door het senescente secretoom werden veroorzaakt.
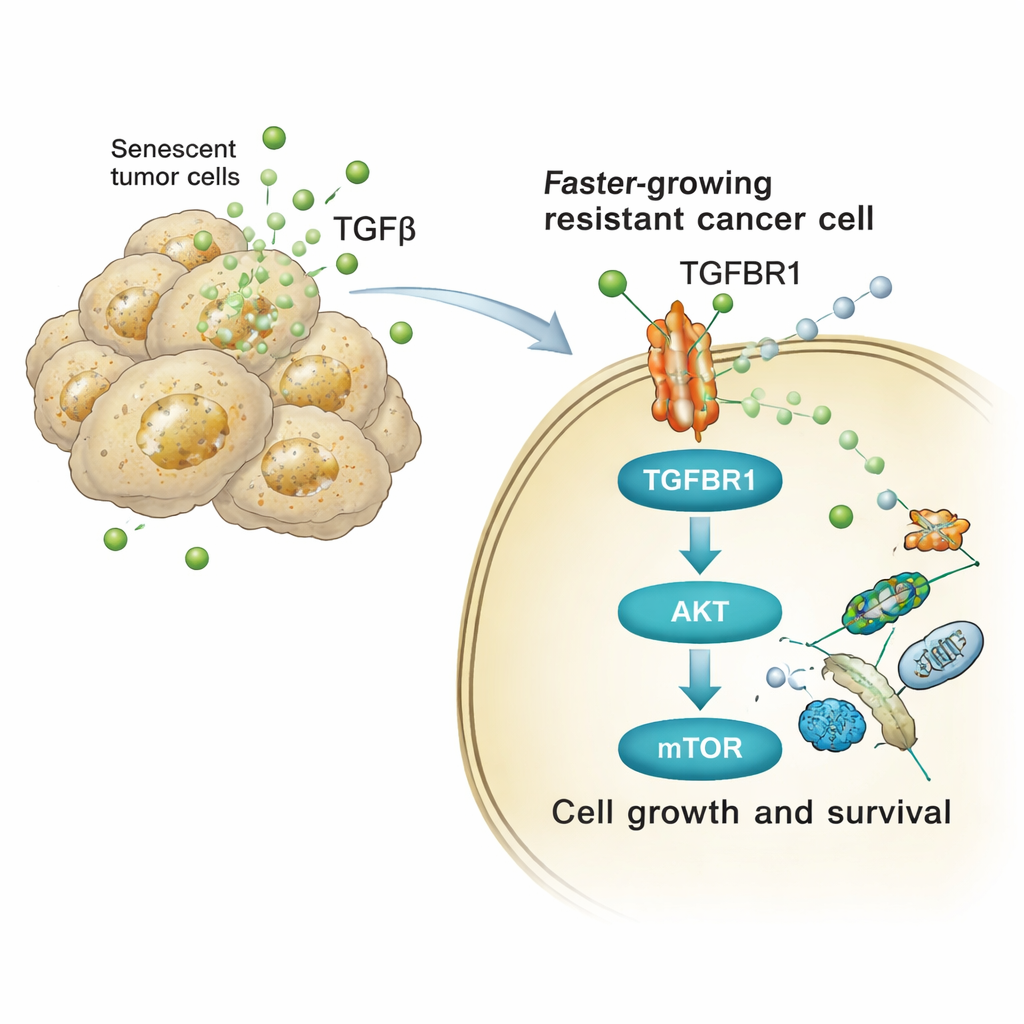
Van muizen tot patiënten: een gedeelde zwakke plek
Deze mechanismen bleven niet beperkt tot petrischaaltjes. Bij muizen met longtumoren leidde het mengen van senescente en niet-senescente kankercellen tot sneller groeiende tumoren en kortere overleving, terwijl het verwijderen van senescente cellen of het blokkeren van TGFBR1 dit effect afremde. Toen standaard cisplatinebehandeling werd gegeven aan muizen met genetisch gemodificeerde longkankers, hoopten tumoren senescentiemarkers op naast hoge AKT/mTOR-activiteit in nabijgelegen nog delende cellen. Het combineren van cisplatine met TGFBR1-remming of senolytische geneesmiddelen (die selectief senescente cellen doden) verminderde de tumorlast en verlengde de overleving vergeleken met chemotherapie alleen. Cruciaal zijn analyses van menselijke long- en hooggradige serieuze eierstokkankermonsters genomen na platina-gebaseerde therapie, die vergelijkbare patronen toonden: verhoogde markers van senescentie en versterkte AKT/mTOR-signaleringsactiviteit in het tumor micro‑milieu, met name in regio’s rijk aan senescente cellen.
Een nadeel omzetten in een voordeel
Voor een leek is de kernboodschap dat platina-chemo een populatie beschadigde maar gevaarlijke “zombie”-cellen kan achterlaten. Deze senescente tumorcellen delen zichzelf niet meer, maar pompen TGFβ-rijke signalen uit die naburige kankercellen wekken, waardoor tumoren opnieuw groeien en verder weerstand ontwikkelen tegen behandeling. Het bemoedigende nieuws is dat deze zwakke plek doelgericht kan worden aangepakt. In preklinische long- en eierstokkankermodellen maakte het toevoegen van middelen die de TGFβ-receptor TGFBR1 blokkeren, of die selectief senescente cellen opruimen, platina-chemotherapie effectiever en verbeterde de overleving zonder duidelijke extra toxiciteit. Het werk wijst op toekomstige klinische onderzoeken die standaard platina-behandeling combineren met senolytische of anti‑TGFβ-strategieën, met als doel de voordelen van chemotherapie te behouden terwijl de verborgen, door senescentie aangedreven bijwerkingen worden uitgeschakeld.
Bronvermelding: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Trefwoorden: chemotherapie-resistentie, cellulaire veroudering, TGFβ-signaleringsweg, longkanker, eierstokkanker