Clear Sky Science · nl
DNA-schade in macrofagen drijft immuunautoreactiviteit via presentatie van nucleaire antigenen
Wanneer cellaire slijtage het immuunsysteem tegen ons keert
Veroudering gaat gepaard met een hoger risico op auto-immuunziekten, waarbij het immuunsysteem begint het lichaam aan te vallen dat het juist moet beschermen. Deze studie onderzoekt een verrassende schuldige: alledaagse DNA-schade binnen immuuncellen genaamd macrofagen. Door na te gaan hoe deze schade verandert wat macrofagen tonen aan andere immuuncellen, leggen de onderzoekers een mogelijk ontbrekende schakel bloot tussen ouder worden en het ontstaan van ziekten zoals lupus.
Bewaarders van het lichaam die uit de band springen
Macrofagen zijn de frontlinieverdedigers die microben en afval insluiten en vervolgens eiwitfragmenten aan T-cellen tonen, zodat het immuunsysteem kan beslissen wat aangevallen moet worden. Het team maakte muizen waarvan de macrofagen een defect hadden in een belangrijk DNA-reparatie-eiwit, ERCC1-XPF, zodat deze cellen aanhoudende DNA-schade droegen. Toen deze muizen ouder werden, ontwikkelden ze kenmerken van auto-immuniteit: ontstekingshaarden in de nieren, afzettingen van immuuncomplexen en complement-eiwitten, vergrote milten en hoge niveaus van antinucleaire antilichamen vergelijkbaar met die bij natuurlijk oude dieren. Gedetailleerde immuunprofilering toonde een toename van plasmacellen, geactiveerde T-cellen en natuurlijke killercellen, allemaal tekenen van een chronisch gestimuleerd immuunsysteem.
Van gebroken DNA naar T-cellen die het eigen weefsel aanvallen
Hoe kon beschadigd DNA in macrofagen zo’n sterke auto-immune-achtige reactie veroorzaken? De onderzoekers vonden dat DNA-breuken een klassieke schade-responsweg in deze cellen activeerden, met enzymen zoals ATM, ATR en DNA‑PK. Deze signalering verhoogde het oppervlak aan MHC klasse II, de moleculaire etalages die eiwitfragmenten aan CD4-T-cellen presenteren. Wanneer macrofagen met DNA-schade werden gemengd met T-cellen, dreven ze sterkere T-celactivering en interferon-gamma-productie dan normale macrofagen. Het blokkeren van MHC-II of het verstoren van de DNA-schaderespons keerde een groot deel van dit effect om, en in levende dieren verminderden antilichamen die MHC-II blokkeerden of depletie van CD4-T-cellen nierontsteking en autoantilichaamniveaus.
Zelf-eiwitten uit de kern op het etalagebord
Om precies te zien wat beschadigde macrofagen aan T-cellen toonden, isoleerde het team de peptiden gebonden aan MHC-II en analyseerde ze met massaspectrometrie. Vergeleken met normale of lipopolysaccharide-geactiveerde cellen presenteerden DNA-beschadigde macrofagen een opvallend verschillende reeks peptiden. In plaats van vooral membraan- en extracellulaire eiwitten waren hun MHC-II-moleculen verrijkt met fragmenten afgeleid van nucleaire en ribosomale eiwitten, waaronder histonen en andere componenten die nauw aan DNA verbonden zijn. Wanneer sommige van deze nucleaire peptiden werden gesynthetiseerd en gebruikt om immuuncellen van de gemodificeerde muizen opnieuw te stimuleren, veroorzaakten ze sterke T-celresponsen, wat suggereert dat deze zelfafgeleide fragmenten inderdaad immunogeen zijn.
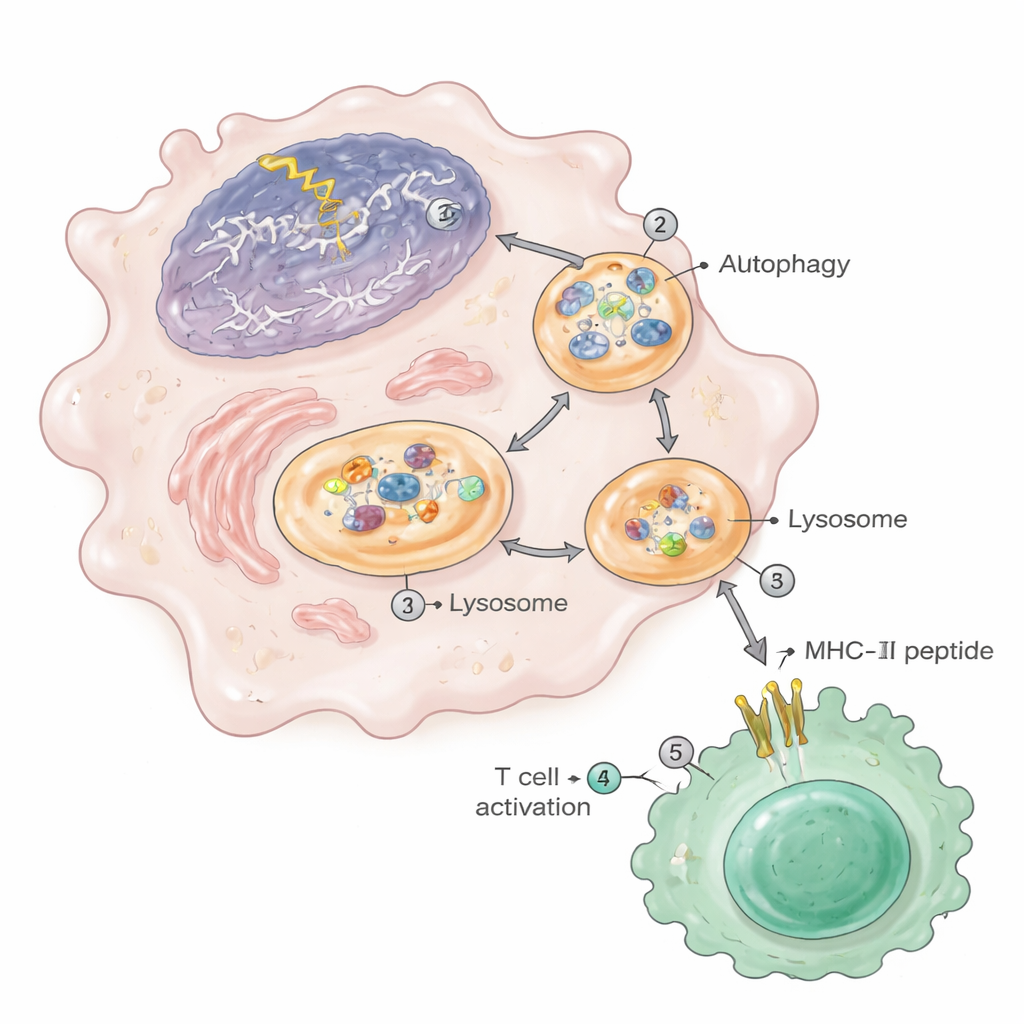
Autofagie: het opruimpad dat auto-immuniteit aanwakkert
De route van nucleair materiaal naar de MHC-II-etalage hing sterk af van autofagie, het interne recyclingsysteem van de cel. Bij DNA-schade nam autofagie toe en vervoerde chromatinefragmenten — uit de eigen celkern — naar autofagosomen die vervolgens fuseerden met lysosomen, waar eiwitten worden afgebroken tot peptiden. Deze lysosomen in beschadigde macrofagen bevatten verhoogde niveaus van nucleaire en ribosomale eiwitten. Toen de onderzoekers autofagie blokkeerden met geneesmiddelen of genetisch een essentieel autofagiegen (Atg5) verwijderden in dezelfde myeloïde cellen, vertoonden de dieren minder nierletsels, minder geactiveerde T‑cellen en plasmacellen, en een dramatische vermindering van nucleaire peptiden die op MHC-II verschenen. Vergelijkbare chromatinefragmenten en verhoogde antigeenpresentatie werden gezien in macrofagen van lupus‑gevoelige muizen, menselijke monocytenlijntjes blootgesteld aan DNA‑beschadigende middelen, en in macrofagen van zeer oude muizen.
Waarom dit ertoe doet voor veroudering en auto-immuunziekten
Gezamenlijk suggereren de bevindingen een eenvoudig maar krachtig idee: naarmate we ouder worden hoopt DNA‑schade zich op in macrofagen, die op hun beurt autofagie gebruiken om nucleair puin op te ruimen. Daarbij hakken ze onbedoeld nucleair materiaal in peptiden die op MHC‑II worden geladen en aan T‑cellen getoond alsof het vreemde antigenen zijn. In de loop van de tijd kan deze chronische blootstelling aan nucleaire zelfantigenen het immuunsysteem trainen om tegen het eigen lichaam te reageren en zo auto-immuniteit bevorderen. Door deze route — van DNA‑schade via autofagie naar nucleaire antigeenpresentatie — te identificeren, benadrukt de studie nieuwe strategieën om leeftijdsgerelateerde auto-immuniteit te remmen, zoals het verbeteren van DNA‑herstel, het fijnafstellen van autofagie, of het selectief blokkeren van de presentatie van nucleaire zelfpeptiden zonder de cruciale verdedigingen van het immuunsysteem uit te schakelen.
Bronvermelding: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
Trefwoorden: veroudering en auto-immuniteit, DNA-schade, macrofagen, autofagie, antistoffen tegen kerncomponenten