Clear Sky Science · nl
Verkennende analyses van klinische uitkomsten uit de BIIB080 fase 1b-studie bij milde ziekte van Alzheimer
Waarom dit onderzoek belangrijk is voor families
De ziekte van Alzheimer tast geheugen, zelfstandigheid en identiteit langzaam aan, en de huidige medicijnen bieden slechts beperkte verlichting. De meeste nieuwe behandelingen richtten zich op het opruimen van een van de boosdoeners, het amyloïde-eiwit, met beperkt effect op het andere belangrijke kenmerk van de ziekte: verwarde kluwens van een eiwit dat tau heet binnen hersencellen. Deze studie onderzocht of een experimenteel middel, BIIB080, dat tot doel heeft de productie van tau bij de genetische bron te verminderen, veilig het geheugenverlies en de dagelijkse achteruitgang bij mensen met beginnende Alzheimer zou kunnen vertragen.
Een nieuwe manier om een probleemgevend eiwit terug te schakelen
In plaats van tau aan te pakken nadat het al kluwens heeft gevormd, werkt BIIB080 een stap eerder. Het is een antisense-oligonucleotide, een korte streng synthetisch genetisch materiaal die ontworpen is om zich te binden aan het boodschapper-RNA dat cellen gebruiken om tau te maken. Door zich aan dit bericht te hechten, zet BIIB080 cellen ertoe aan het te vernietigen, waardoor de totale hoeveelheid tau die de hersenen produceren afneemt, inclusief vormen waarvan men denkt dat ze bijzonder toxisch zijn. De verwachting is dat bij minder aanmaak van nieuw tau bestaande kluwens kunnen krimpen en langzamer verspreiden, waardoor de schade aan neurale netwerken die ten grondslag ligt aan geheugen- en denkproblemen bij Alzheimer vermindert.
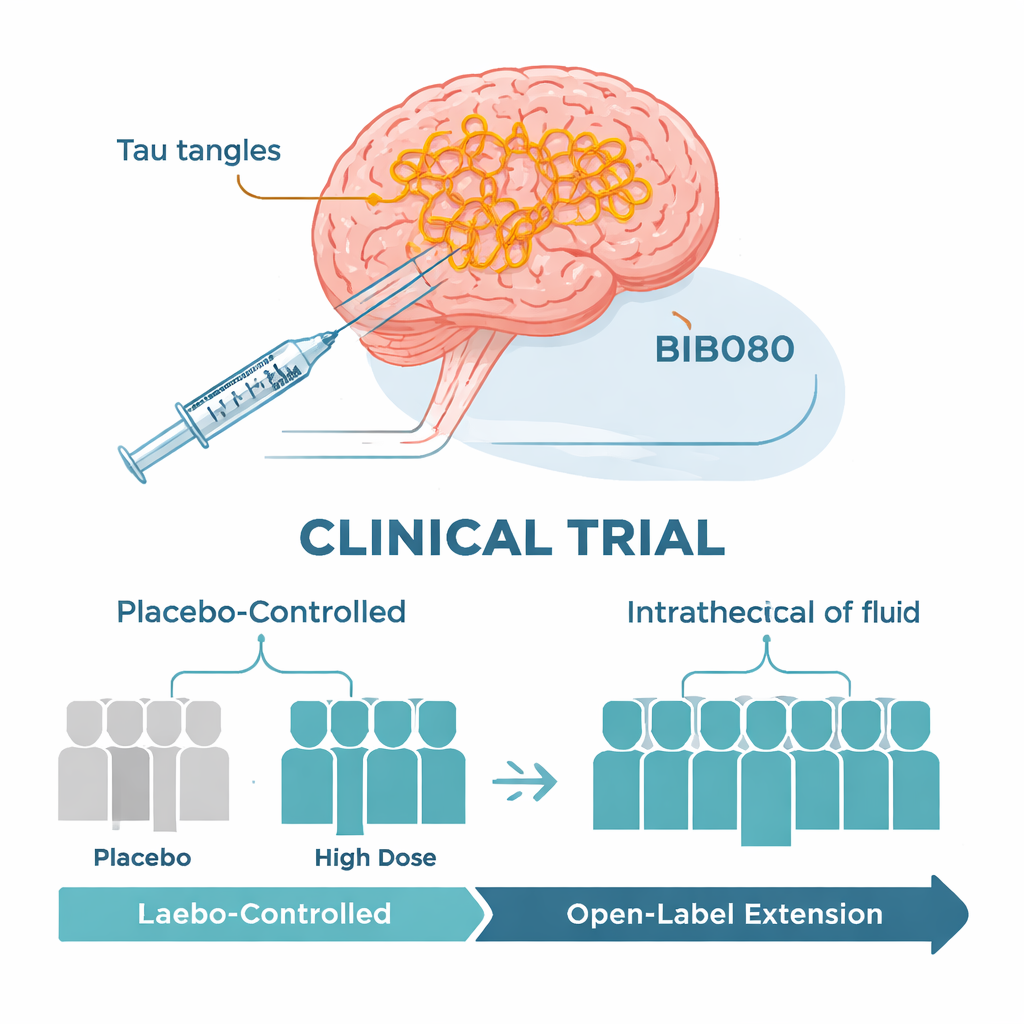
Hoe de vroege proef was opgezet
De onderzoekers voerden een internationale fase 1b-klinische proef uit die vooral bedoeld was om veiligheid te testen. Iets meer dan 100 personen van 50 tot 74 jaar met milde Alzheimer, bevestigd met ruggenmergvloeistoftests, werden geïncludeerd. In het eerste deel van de studie werden deelnemers random toegewezen om BIIB080 of placebo te ontvangen via periodieke injecties in het vocht rond het ruggenmerg over drie maanden, gevolgd door nog enkele maanden follow-up. Verschillende groepen kregen geleidelijk hogere doses. Daarna volgde een langetermijnverlenging waarin iedereen wat het team als hoge dosis BIIB080 beschouwde bijna een jaar kreeg. Omdat er in deze tweede fase geen placebogroep was, vergeleken de onderzoekers de behandelde patiënten met goed-afgestemde patiënten uit andere grote Alzheimer-studies.
Signalen van langzamere achteruitgang in denken en dagelijks functioneren
Hoewel de studie klein was en niet was opgezet om effectiviteit te bewijzen, kwamen er meerdere patronen naar voren. Mensen die de hogere doses BIIB080 kregen lieten gemiddeld minder verslechtering zien op standaardtesten voor cognitieve functies (zoals de Mini-Mental State Examination), geheugen en het vermogen om alledaagse taken uit te voeren dan degenen die placebo kregen in de eerste maanden. In de langetermijnverlenging werden 16 deelnemers die gedurende de hele periode op hoge doses bleven vergeleken met zorgvuldig afgestemde “externe controles” uit een andere tau-gerichte proef en uit een grote Alzheimer-database. Over meerdere meetinstrumenten—globale dementieclassificatie, cognitieve scores en functionele vragenlijsten—neigde de BIIB080-groep ernaar langzamer achteruit te gaan dan deze vergelijkingsgroepen over ongeveer twee jaar vanaf de start van de behandeling.
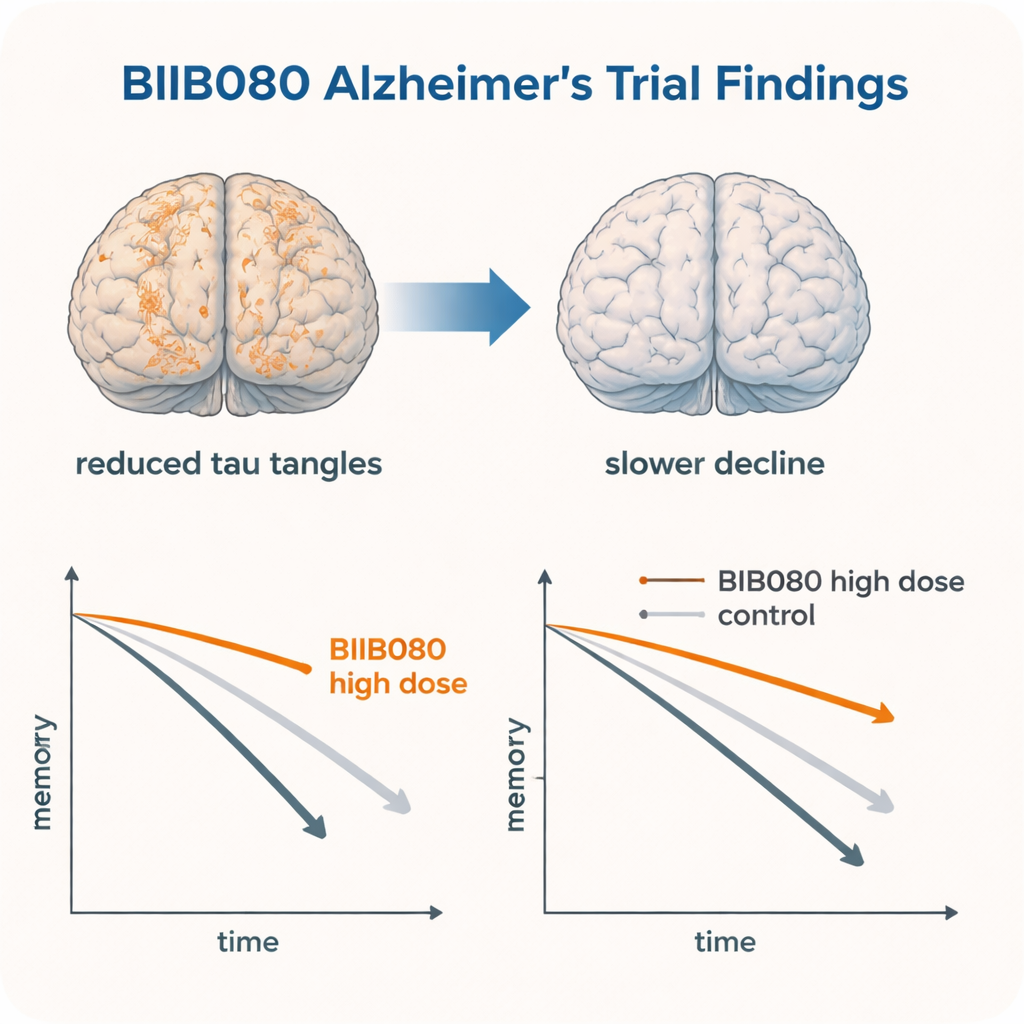
Veranderingen in de hersenen die overeenkomen met de klinische trends
Eerdere rapporten van dezelfde proef hadden al aangetoond dat BIIB080 de tau-spiegels in ruggenmergvocht scherp verlaagde en, opvallend, de hoeveelheid tau-kluwens die op gespecialiseerde hersenscans te zien waren in veel regio’s verminderde. De verkennende klinische bevindingen van deze studie sluiten aan bij die biologische veranderingen: waar tau-kluwens afnamen, leken denken en dagelijks functioneren langzamer te verslechteren. In diermodellen die te veel tau produceren, hadden soortgelijke antisense-middelen niet alleen de tau-afzettingen verminderd maar ook aanvallen, verlies van zenuwcellen en gedragsproblemen verminderd. Samen suggereren deze aanwijzingen dat het terugschakelen van tau bij de bron mogelijk werkelijk het verloop van Alzheimer kan veranderen, en niet alleen de symptomen maskeren.
Veiligheid, kanttekeningen en wat er hierna komt
De meeste bijwerkingen van BIIB080 in deze proef waren mild tot matig en gerelateerd aan de ruggenmerginjecties zelf, zoals hoofdpijn, rugpijn of tijdelijke duizeligheid. Een paar deelnemers ontwikkelden ernstiger problemen, waaronder verslechtering van dementiesymptomen, en stopten met de behandeling, dus zorgvuldige monitoring blijft essentieel. Belangrijk is dat de studie klein was, meerdere dosisgroepen met ongelijke uitgangskenmerken gebruikte en afhankelijk was van vergelijking met externe gegevens zodra iedereen actief geneesmiddel kreeg. De auteurs benadrukken daarom dat de veelbelovende trends nog steeds aan toeval of subtiele vertekeningen te wijten kunnen zijn.
Wat dit zou kunnen betekenen voor toekomstige behandeling
Voor mensen met de ziekte van Alzheimer bieden deze bevindingen nog geen nieuw goedgekeurd middel, maar ze wijzen op een veelbelovende richting. BIIB080 lijkt veilig tau-kluwens in het menselijk brein te verminderen en wordt in deze vroege studie geassocieerd met een tragere klinische achteruitgang, met name bij hogere doses. Omdat de proef verkennend was, zijn grotere en strengere studies nodig om te bevestigen of het middel echt geheugenverlies vertraagt en zelfstandigheid behoudt. Dergelijk onderzoek loopt nu in een fase 2-studie genaamd CELIA, die meer patiënten langer zal volgen. Als toekomstige resultaten standhouden, zouden therapieën die de productie van tau verlagen amyloïde-gerichte middelen kunnen aanvullen of combineren, en zo een meer omvattende aanpak bieden om het beloop van Alzheimer te veranderen.
Bronvermelding: Shulman, M., Wu, S., Ziogas, N. et al. Exploratory analyses of clinical outcomes from the BIIB080 phase 1b study in mild Alzheimer’s disease. Nat Aging 6, 445–453 (2026). https://doi.org/10.1038/s43587-025-01031-9
Trefwoorden: Ziekte van Alzheimer, tau-eiwit, antisense-therapie, klinische proef, neurodegeneratie