Clear Sky Science · nl
Senotoxines richten zich op veroudering via lipide-bindingsspecificiteit, ionenbalans en remodelering van het lipideome
Waarom het doden van “zombie”-cellen de kankerbehandeling kan verscherpen
Naarmate we ouder worden — of zware behandelingen zoals chemotherapie ondergaan — stoppen sommige cellen met delen maar weigeren ze te sterven. Deze “zombie”-cellen, bekend als senescente cellen, kunnen ontstekingsbevorderende moleculen uitscheiden die weefsels beschadigen en tumoren kunnen helpen terugkomen. Deze studie onderzoekt een verrassende nieuwe manier om zulke probleemcellen selectief te verwijderen met een door gif afgeleid eiwit, wat kankerbehandelingen zowel effectiever als veiliger zou kunnen maken.
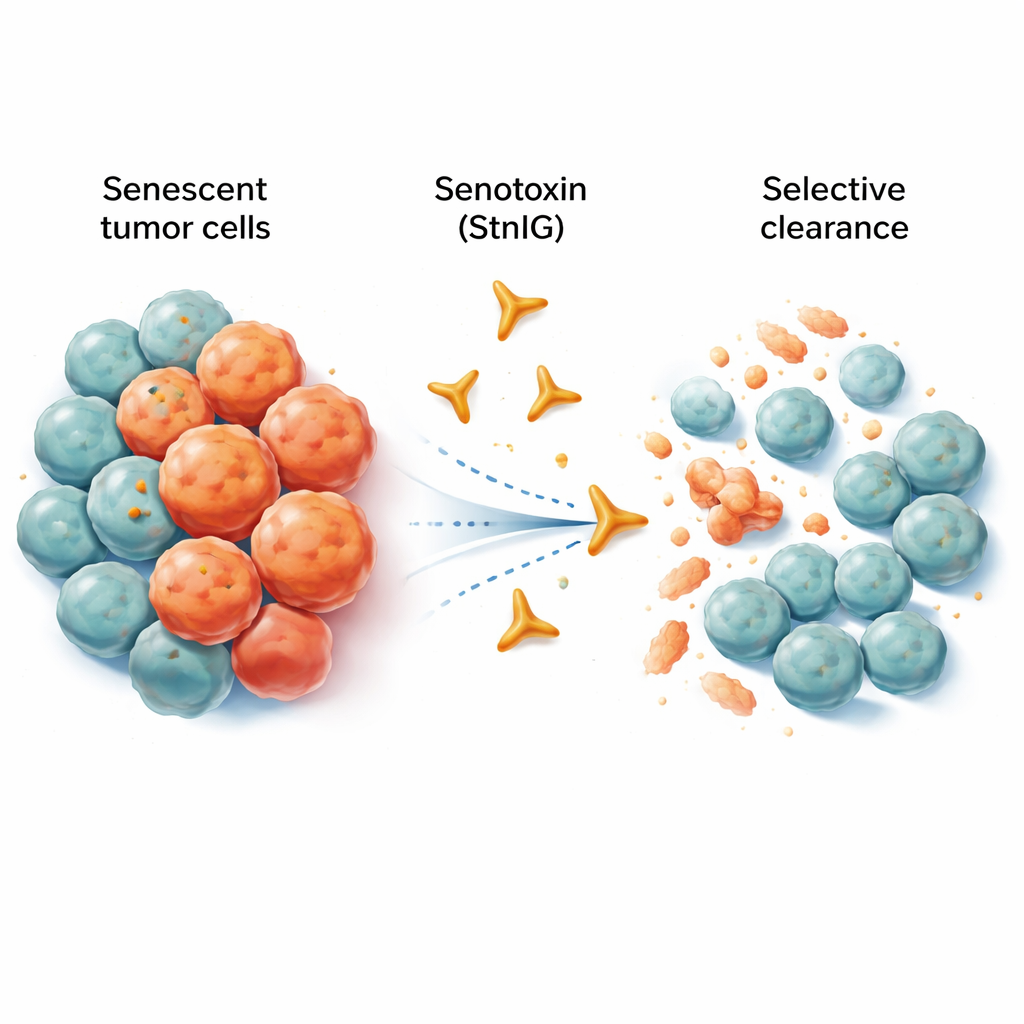
Oude cellen die niet opgeven
Senescente cellen zijn als gepensioneerde werknemers die hun bureau blijven bezetten en de werkplek verstoren. Ze delen niet meer, maar scheiden een cocktail van ontstekingssignalen uit die nabijgelegen weefsel kunnen verzwakken, veroudering kunnen bevorderen en zelfs tumorgroei en -verspreiding kunnen ondersteunen. Chemotherapie doodt veel kankercellen, maar laat vaak een spoor van senescente cellen achter in en rond de tumor. Deze achterblijvende cellen kunnen chronische ontsteking, bijwerkingen en uiteindelijk terugval aanwakkeren. Bestaande experimentele medicijnen, senolytica genoemd, beogen senescente cellen te verwijderen, maar veel van deze middelen treffen ook gezonde cellen, werken alleen in zeer smalle doseringen of worden slecht door het lichaam opgenomen.
Zeenaakhorengif omvormen tot een precisie-instrument
De onderzoekers wendden zich tot de natuur’s eigen specialisten in celvernietiging: dierlijke giffen. Ze richtten zich op een pore-vormend eiwit genaamd sticholysine I (StnI), gevonden in een Caribische zeeanemoon. Dit eiwit kan kleine gaatjes in celmembranen maken. Het team ontdekte dat StnI, en een verfijnde versie die ze ontwierpen, StnIG, opvallend beter zijn in het doden van senescente kankercellen dan van niet-senescente buren. Over meerdere typen menselijke kankercellen (melanoom, lever, long en zenuwafgeleide tumoren) die door chemotherapie in senescentie werden gebracht, wisten StnI en vooral StnIG de verouderde cellen uit te roeien bij veel lagere doses dan nodig om actief delende cellen te treffen. StnIG was selectiever dan een toonaangevend experimenteel senolyticum, navitoclax, wat suggereert dat zorgvuldig afgestemde toxines huidige benaderingen kunnen overtreffen.
Hoe veranderde celmembranen een achilleshiel worden
Senescente cellen veranderen niet alleen van binnen; hun buitenste membraan — de vettige huid rond elke cel — ondergaat ook remodelering. In gezonde cellen bevinden bepaalde lipiden zich voornamelijk aan de binnenzijde van het membraan, verborgen voor de buitenwereld. Bij senescente cellen raakt dit evenwicht verstoord en komen deze lipiden aan het oppervlak te liggen. Met gedetailleerde chemische analyse en computersimulaties toonden de onderzoekers aan dat StnIG dit gewijzigde lipidenlandschap herkent en eraan hecht. De structuur van StnIG is bijzonder geschikt om zich vast te klampen aan specifieke lipiden die senescente cellen aan hun oppervlak blootleggen. Eenmaal gebonden vormt StnIG poriën die het mogelijk maken dat geladen deeltjes, of ionen, op sterk onevenwichtige wijze in- en uitstromen.
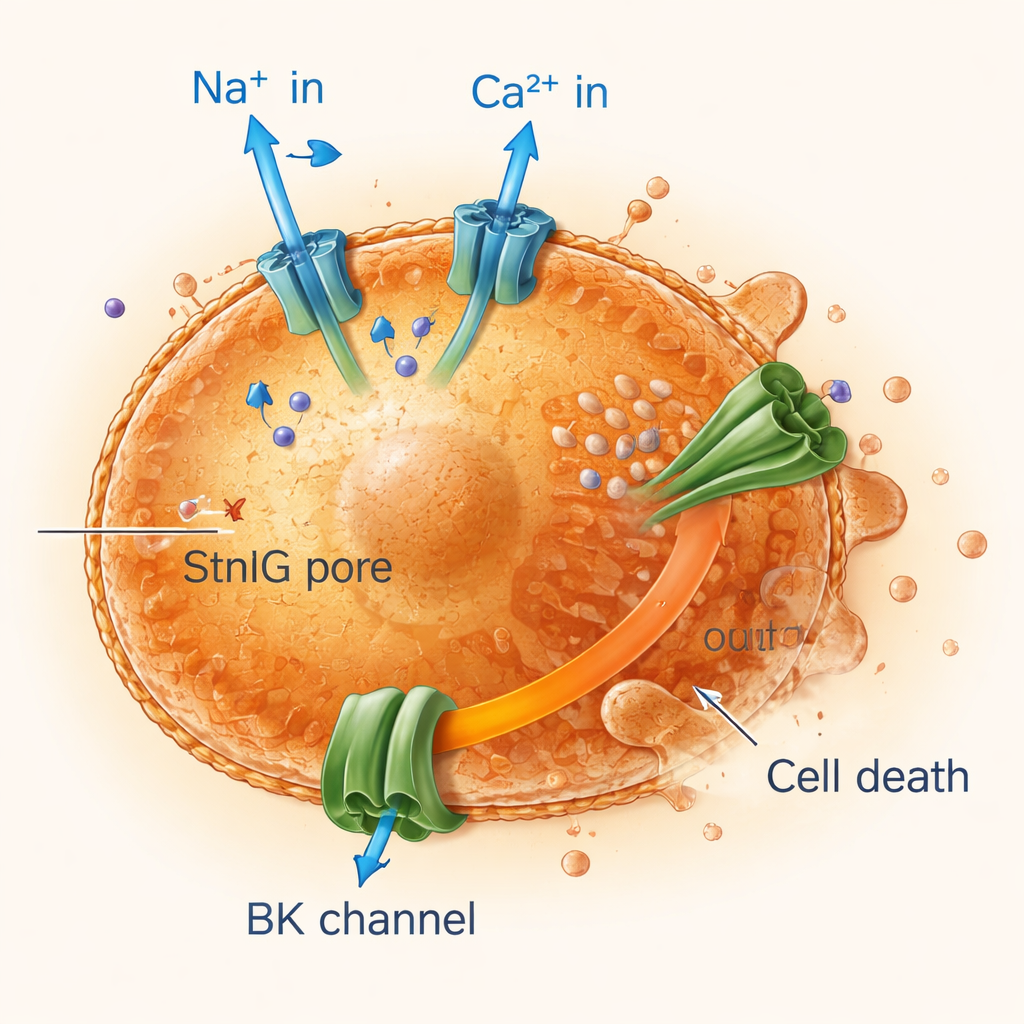
Verouderende cellen kortsluiten met ionenstoornis
Door elektriciteit en ionenbeweging over celmembranen te volgen, vonden de onderzoekers dat StnIG-poriën natrium- en calciumionen snel in senescente cellen laten binnenstromen terwijl kalium continu weglekt. De calciuminflux activeert grote kaliumkanalen, wat het verlies van kalium versterkt—essentieel voor het behouden van celvolume en overleving. Senescente cellen, al minder flexibel en gevoeliger dan gezonde cellen, kunnen niet omgaan met deze aanhoudende ionverstoring. Hun mitochondriën — de energiecentrales van de cel — verliezen hun elektrische lading, de energieproductie keldert en de cellen ondergaan geprogrammeerde vormen van celdood, waaronder apoptose en een vurig ontstekingsde lot genaamd pyroptose. Het blokkeren van calciuminstroom of kaliumkanalen beschermde senescente cellen, wat bevestigt dat deze ionenverstoring centraal staat in de werking van het toxine.
Van kWeekschalen naar levende dieren
Het team testte vervolgens of deze strategie ook in levende organismen werkt. In zebravisembryo’s met menselijke senescente melanoomcellen verminderden lage doses StnIG het aantal van deze cellen even doeltreffend als navitoclax, zonder duidelijke toxiciteit. In muismodellen van melanoom en leverkanker vertraagde chemotherapie met een celdelingsremmer (palbociclib) de tumorgroei door veel kankercellen in senescentie te duwen. Toen de onderzoekers StnIG periodiek toevoegden, krimpten tumoren of gingen ze eerder in remissie dan bij alleen chemotherapie, en vergelijkbaar met de combinatie chemotherapie–navitoclax. Belangrijk is dat StnIG-behandelde muizen beperkte bijwerkingen vertoonden en geen duidelijke schade aan belangrijke organen, hoewel het kaliumgehalte in het bloed steeg bij dieren met senescente tumoren—wat waarschijnlijk de massale vrijgave van kalium reflecteert toen tumorcellen werden vernietigd.
Wat dit betekent voor toekomstige kankerzorg
Dit werk introduceert “senotoxines”: ontworpen, door gif geïnspireerde eiwitten die inspelen op de unieke membraan- en ionenhandhavingskenmerken van senescente cellen. Door zich te richten op gewijzigde lipiden en dodelijke ionenonevenwichtigheden te forceren, kan StnIG schadelijke senescente cellen selectief verwijderen terwijl het meeste gezonde weefsel gespaard blijft. In combinatie met chemotherapie zouden dergelijke senotoxines op termijn kunnen helpen de zombie-cellen die terugval en chronische ontsteking aandrijven weg te vegen, waardoor kankerbehandelingen duurzamer worden en sommige langetermijnbijwerkingen mogelijk verminderen.
Bronvermelding: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Trefwoorden: cellulaire senescentie, senolytica, kankertherapie, geneesmiddelen afgeleid van gif, ionkanalen