Clear Sky Science · nl
PIK3CD-bewerking aangepast aan CAR verbetert de antitumorwerking van T-cellen
Het herprogrammeren van kankervechtende cellen
Chimeric antigen receptor (CAR) T-celtherapie heeft de behandeling van sommige bloedkankers getransformeerd, maar veel patiënten vallen toch terug of reageren nooit. Een belangrijk probleem is dat deze gemodificeerde immuuncellen kunnen uitputten of niet lang genoeg in het lichaam blijven. Deze studie stelt een eenvoudige maar krachtige vraag: in plaats van CAR’s volledig te herontwerpen, wat als we de interne bedrading van T-cellen subtiel konden "herstemen" zodat ze langer krachtig blijven, en dat op een veilige manier?
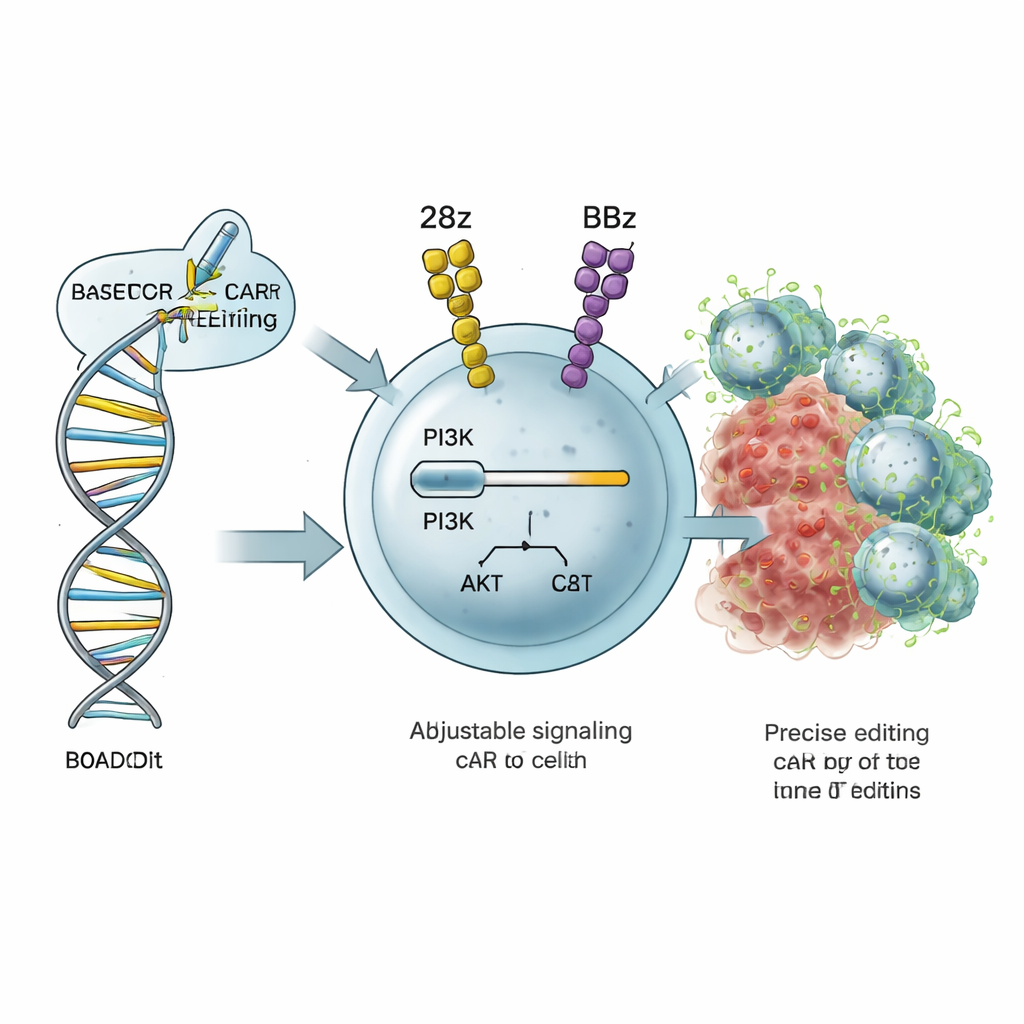
De volumeknop van de T-cel richten
Door kanker dodelijke T-cellen vertrouwen op interne signaalcircuits die bepalen hoe sterk ze geactiveerd worden, hoe snel ze delen en of ze kortlevende strijders of langlevende geheugencellen worden. Een belangrijk circuit is de PI3K–AKT-route, waarbij een eiwit PI3Kδ—gecodeerd door het PIK3CD-gen—als een volumeknop voor activatie en metabolisme fungeert. De auteurs ontwikkelden een strategie die ze ROADSTAR noemen, waarbij base editing wordt gebruikt, een zeer precieze vorm van CRISPR-genoombewerking, om enkele "letters" in PIK3CD te veranderen. In plaats van de route volledig aan of uit te zetten, zoekt ROADSTAR naar kleine mutaties die de signalering zachtjes verhogen of verlagen op een manier die het beste past bij het specifieke CAR-ontwerp binnen de T-cel.
Het ontdekken van behulpzame mutaties
Het team bouwde een bibliotheek van 34 verschillende enkel-letterveranderingen in het regulerende deel van PIK3CD en introduceerde die in menselijke T-cellen die al één van twee veelvoorkomende CAR-ontwerpen droegen: 28z (gebaseerd op het CD28-molecuul) en BBz (gebaseerd op 4-1BB). Deze CAR’s verschillen in hoe ze T-cellen stimuleren: 28z neigt naar een sterke, snelle aanval maar ook uitputting, terwijl BBz betere overleving en geheugen bevordert maar soms minder agressief kan zijn. De bewerkte CAR-T-cellen werden onderworpen aan een "stresstest" door ze herhaaldelijk bloot te stellen aan leukemiecellen. Met behulp van diepe sequencing volgden de onderzoekers welke mutaties het de CAR-T-cellen mogelijk maakten hun onbewerkte tegenhangers te overtreffen gedurende meerdere weken.
Twee mutaties staken er duidelijk uit. In BBz CAR-T-cellen verhoogde een verandering genaamd E81K de PI3Kδ-activiteit licht, waardoor signalen via de PI3K–AKT-route toenamen. In 28z CAR-T-cellen dempte een andere verandering, L32P, de PI3Kδ-activiteit. Structurele modellering suggereerde dat beide aanpassingen subtiel veranderen hoe PI3Kδ met zijn regulatorische partner interageert, waardoor de signaalsterkte wordt fijngeregeld in plaats van volledig aan of uit te zetten. Belangrijk is dat de voordelige mutatie voor het ene CAR-ontwerp niet dezelfde was als voor het andere, wat benadrukt dat elke CAR-architectuur zijn eigen optimale interne afstemming vereist.
Sterkere, fittere en langer houdbare CAR-T-cellen
Wanneer de veelbelovende edits individueel werden getest, zorgde E81K ervoor dat BBz CAR-T-cellen bij het zien van tumorcellen steviger geactiveerd werden, beter konden prolifereren en veel efficiënter kankerdoelen doodden, ook bij lage antigeenniveaus. Deze cellen ontwikkelden zich tot effector-geheugen T-cellen die robuuste dodelijkheid combineerden met het vermogen om aan te houden. In muismodellen van leukemie en gemetastaseerde neuroblastoom beheersten E81K-bewerkte BBz CAR-T-cellen tumoren vollediger en veel langer dan onbewerkte BBz-cellen, en versloegen ze zelfs meerdere rondes van tumorheruitdaging. Gedetailleerde enkelcellig RNA- en metabole profileringsanalyse toonde aan dat E81K-cellen verbeterde mitochondriale functie hadden, een hogere spare respiratory en glycolytische capaciteit en minder tekenen van uitputting—ze waren in wezen energieker en veerkrachtiger.
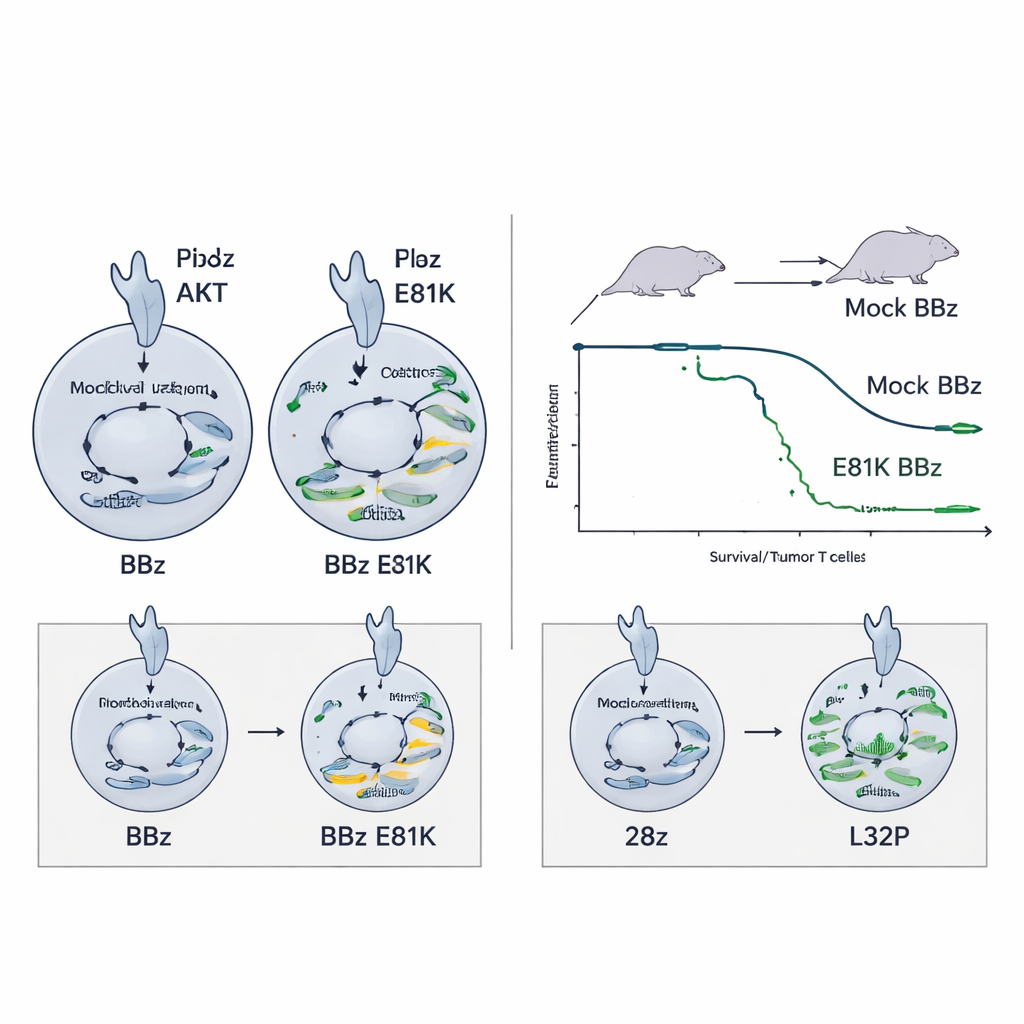
Uitputting voorkomen bij zeer actieve CAR’s
Dezelfde E81K-boost hielp 28z CAR-T-cellen niet—en kon zelfs schadelijk zijn—omdat die al sterk signaleren. In dat geval vergrootte extra PI3K-activiteit merkers van uitputting zonder de functie te verbeteren. Hier bleek de L32P-mutatie geschikter: door de PI3K–AKT-signaleringsroute bescheiden terug te draaien, vertoonden L32P-bewerkte 28z CAR-T-cellen een lagere basisactivatie maar behielden ze hoge dodelijkheid en gingen ze in de loop van de tijd meer prolifereren. Ze behielden ook een minder gedifferentieerde, geheugenachtige toestand, inclusief een stamcelachtige geheugenpool die verondersteld wordt langdurige responsen te ondersteunen. In een veeleisend neuroblastoommodel verbeterden L32P-gemodificeerde 28z CAR-T-cellen de overleving vergeleken met hun onbewerkte tegenhangers.
Veiligheid en toekomstige belofte
Een centraal bezwaar bij het permanent aanpassen van immuunsignalen is het risico op ongecontroleerde groei of secundaire kankers. De auteurs voerden daarom uitgebreide veiligheidscontroles uit. E81K-bewerkte BBz CAR-T-cellen vertoonden geen abnormale groei in kweek, veroorzaakten geen orgaanschade of inflammatoire crises bij muizen en toonden maanden na toediening geen tekenen van lymfoom of weefselinvasie. Klinische databases laten eveneens geen verrijking zien van deze specifieke PIK3CD-mutaties in T-celleukemieën. Al met al toont het werk aan dat zorgvuldig gekozen enkel-letter genoomwijzigingen als precisiedraaiknoppen voor T-celgedrag kunnen fungeren—ze vergroten antitumorkracht en volharding terwijl ze de unieke biologie van elke CAR respecteren. Deze ROADSTAR-aanpak zou kunnen helpen bij het ontwikkelen van de volgende generatie CAR-T-therapieën die zowel effectiever als betrouwbaarder zijn bij bloedkankers en mogelijk ook solide tumoren.
Bronvermelding: Bucher, P., Brückner, N., Kortendieck, J. et al. CAR-adapted PIK3CD base editing enhances T cell anti-tumor potency. Nat Cancer 7, 368–383 (2026). https://doi.org/10.1038/s43018-025-01099-7
Trefwoorden: CAR-T-cellen, PI3K-signaaltransductie, base editing, kankerimmunotherapie, T-celmetabolisme