Clear Sky Science · nl
De novo H3.3K27M-veranderde diffuse midline-glioma in menselijke hersenstamorganoïden om GD2 CAR-T-celfunctie te ontleden
Waarom deze studie naar kinderkanker ertoe doet
Diffuse midline-glioma is een van de dodelijkste kinderkankers van de hersenen: hij treft zeer jonge kinderen in de hersenstam en laat gezinnen vrijwel geen effectieve behandelingsopties. Omdat tumoren diep in de hersenen liggen en zelden operatief worden verwijderd, hebben onderzoekers weinig weefsel om te bestuderen en weinig veilige manieren om nieuwe therapieën te testen. Deze studie bouwt een realistisch „mini‑hersenstam in een schaaltje” en gebruikt dat om te observeren hoe een veelbelovende immunotherapie — GD2 CAR‑T‑cellen — zich gedraagt over weken, inclusief waarom die soms faalt.
Het bouwen van een mini‑hersenstam in het laboratorium
Het team begon met humane stamcellen en leidde deze stap voor stap naar driedimensionale hersenorganoïden die lijken op de hersenstamregio die pons heet, waar deze tumoren meestal ontstaan. Door groeisignalen zorgvuldig te timen, produceerden ze organoïden die rijk zijn aan dezelfde soorten steuncellen, of glia, die normaal in dit gebied voorkomen. Gedetailleerde genetische analyses toonden aan dat de celtypen en hun rijping patronen volgden die gezien worden in de vroege menselijke hersenontwikkeling, met name de gliale lijnen die typisch zijn voor de pons en de aangrenzende medulla. Dit betekende dat de organoïden als een realistische achtergrond konden dienen om te bestuderen hoe deze kanker begint en groeit.
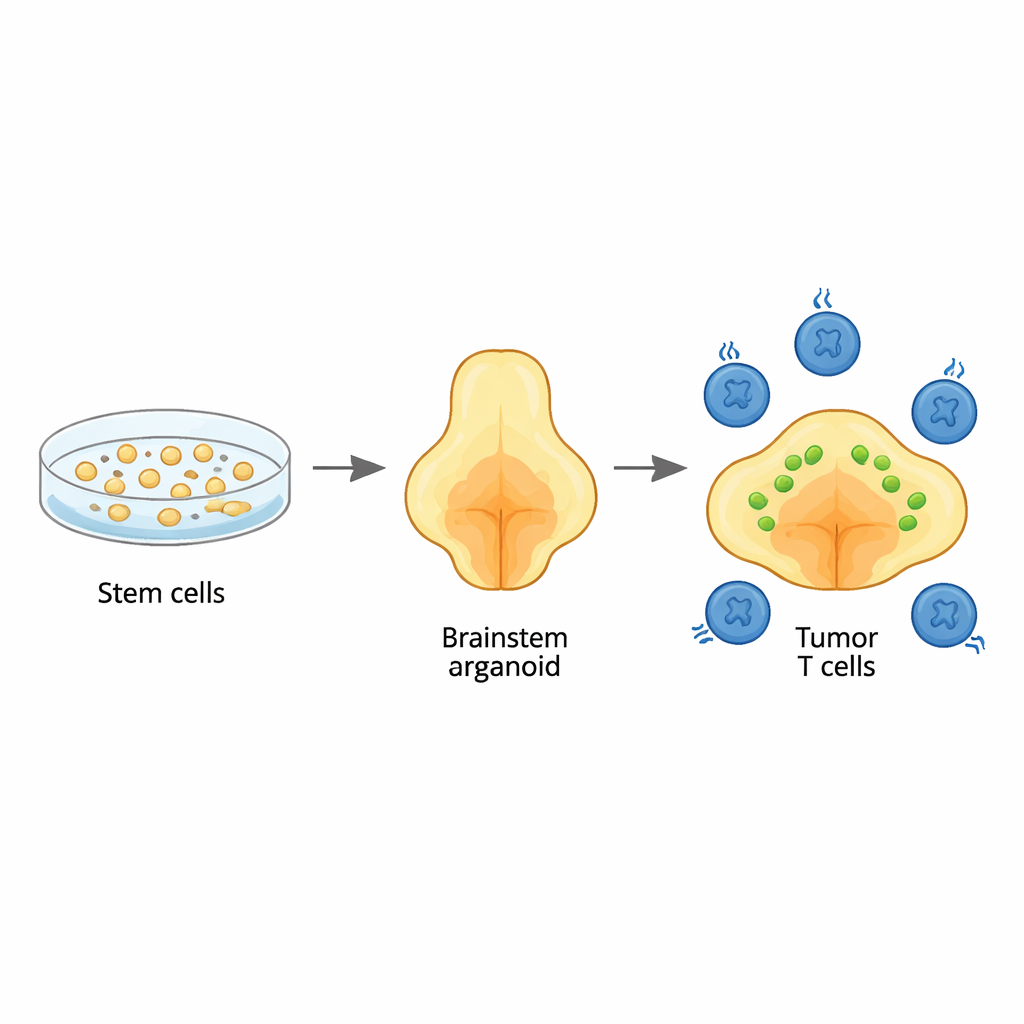
De tumor van het kind nabootsen binnen het organoïde
Om diffuse midline‑glioma na te bootsen, brachten de onderzoekers drie sleutelgenetische veranderingen in in jonge organoïden: een kenmerkende mutatie in een histon‑eiwit (H3.3K27M), verlies van de tumorsuppressor TP53 en een activerende verandering in de groeireceptor PDGFRA. Wanneer deze wijzigingen in een zeer vroeg ontwikkelingsstadium werden ingebracht, veranderden geselecteerde glia‑achtige cellen in kankercellen. De resulterende tumoren verspreidden zich diffus door de organoïden, net zoals ze dat doen in de hersenstam van kinderen, en droegen dezelfde brede DNA‑ en RNA‑handtekeningen als patiënttumoren. Single‑cell sequencing toonde een mengeling van kankercelstaten, waaronder onrijpe, pons‑specifieke gliale cellen die overeenkomen met die in echte pediatrische tumoren, wat onderstreept dat het model de menselijke ziekte trouw nabootst.
Observeren hoe immuuntherapieën vechten — en uitgeput raken — in de tijd
Met dit tumor‑in‑een‑hersenstammodel voegde het team GD2 CAR‑T‑cellen toe — bij patiënten afgenomen T‑cellen die zijn aangepast om een molecuul genaamd GD2 op tumorcellen te herkennen — en volgde zowel tumorgrootte als T‑celgedrag tot een maand lang. Sommige organoïden lieten sterke tumorkrimp zien, andere slechts gedeeltelijke controle, wat de gemengde uitkomsten in klinische studies weerspiegelt. Single‑cell RNA‑sequencing van meer dan 20.000 CAR‑T‑cellen die aan de tumoren werden blootgesteld, onthulde een verrassende diversiteit aan T‑celstaten. Sommige cellen waren hoogst cytotoxische “killers”, andere waren geactiveerd maar niet volledig dodelijk, en een aparte groep toonde kenmerken van uitputting, met gedempte kanker‑dodelijke genen en hoge expressie van remmende „brakes”. De uitgeputte cellen leken sterk op uitgeputte T‑cellen die gezien worden bij chronische infecties en menselijke tumoren, wat aangeeft dat het organoïde‑systeem klinisch relevante T‑celvermoeidheid vastlegt die wordt aangedreven door aanhoudend contact met kanker.
Sterke maar kortdurende T‑cellen vinden
Nadere analyse identificeerde een subset van CAR‑T‑cellen gemarkeerd door een oppervlakte-eiwit genaamd NCAM1 die op korte termijn bijzonder krachtige doders waren. Wanneer deze NCAM1‑positieve cellen werden geïsoleerd en afzonderlijk gebruikt, controleerden ze aanvankelijk tumoren sterker dan hun NCAM1‑negatieve tegenhangers. Ze raakten echter ook sneller uitgeput en namen sneller in aantal af, wat op termijn leidde tot zwakkere controle. Deze afweging tussen onmiddellijke kracht en duurzaamheid helpt verklaren waarom CAR‑T‑therapieën spectaculaire maar tijdelijke reacties kunnen geven en suggereert dat het vooraf selecteren of vormgeven van T‑cel subsets de behandelingsduur zou kunnen optimaliseren.
Hoe brain‑immune cellen therapie kunnen ondermijnen
In de echte hersenen worden tumoren niet alleen omgeven door neuronen en glia maar ook door microglia, de resident‑immuuncellen van de hersenen. Om deze laag van complexiteit vast te leggen, voegden de wetenschappers uit stamcellen afgeleide microglia toe aan hun organoïden. Deze cellen rijpten, namen morfologieën en genexpressiepatronen aan die specifiek zijn voor microglia gevonden in diffuse midline‑glioma, en produceerden moleculen die geassocieerd worden met een immunosuppressieve omgeving. Wanneer CAR‑T‑cellen werden toegevoegd aan tumor‑dragende organoïden met microglia, verschoof het T‑celprofiel verder naar uitgeputte en lage‑effector staten en verslechterde de tumorcontrole. Tegelijkertijd namen inflammatoire factoren toe die gekoppeld zijn aan bijwerkingen van de behandeling, zoals IL‑6, wat suggereert dat het model ook kan helpen bij het bestuderen van CAR‑T‑gerelateerde toxiciteiten.
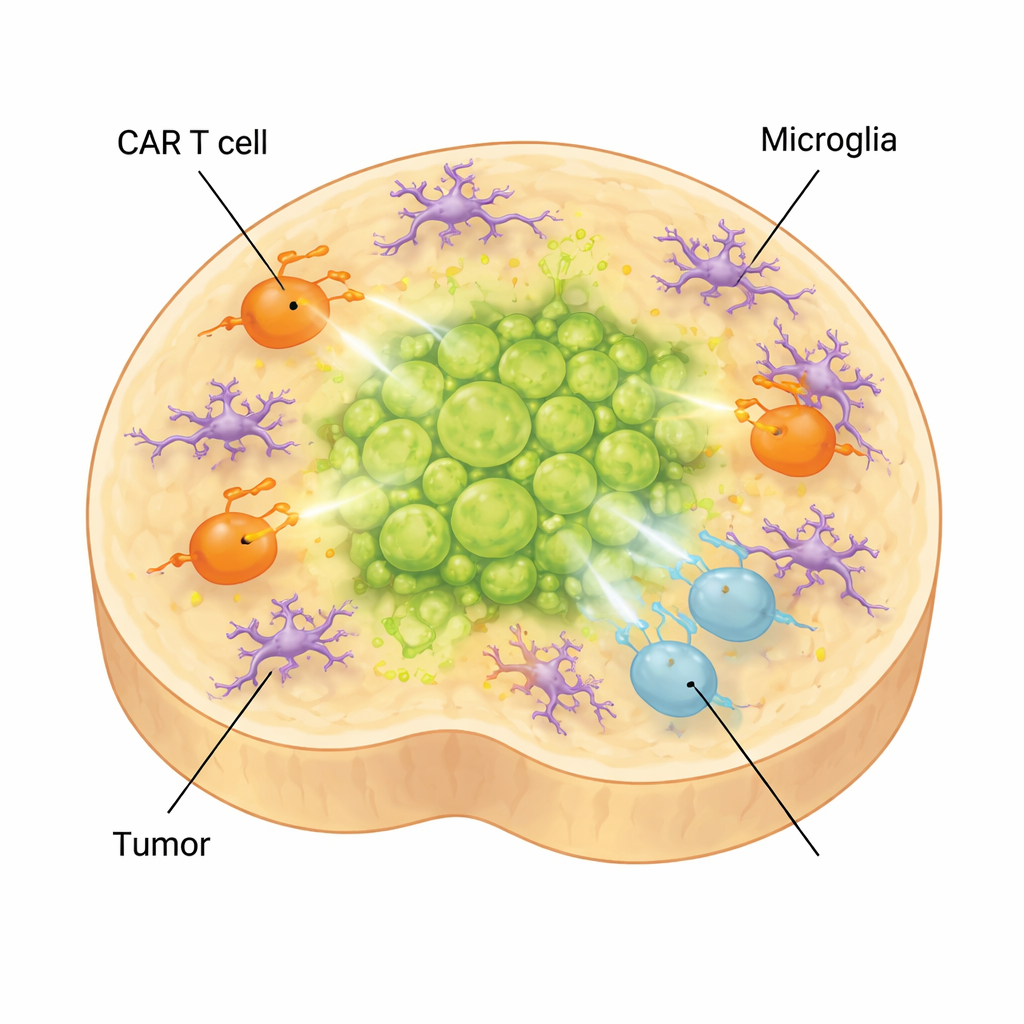
Wat dit betekent voor kinderen met deze kanker
Voor gezinnen die geconfronteerd worden met diffuse midline‑glioma biedt dit werk nog geen nieuwe genezing, maar het levert een krachtig testplatform om daar sneller te komen. Door de hersenstamomgeving en de tumor van een kind in een schaaltje na te bootsen, kunnen wetenschappers nu in realtime observeren hoe verschillende tumorcellen, CAR‑T‑celtypes en microglia wekenlang met elkaar interageren. Dit stelt hen in staat te achterhalen welke gemodificeerde T‑cellen het meest effectief zijn, wanneer en waarom ze uitgeput raken, en hoe hersen‑residente immuuncellen hun inspanningen ondermijnen. Uiteindelijk zouden zulke organoïde‑modellen voor individuele patiënten gepersonaliseerd kunnen worden en gebruikt kunnen worden om immunotherapieën fijn af te stemmen voordat ze worden toegediend, waardoor de kans toeneemt dat toekomstige CAR‑T‑behandelingen veiliger en effectiever zijn voor kinderen.
Bronvermelding: Bessler, N., Wezenaar, A.K.L., Ariese, H.C.R. et al. De novo H3.3K27M-altered diffuse midline glioma in human brainstem organoids to dissect GD2 CAR T cell function. Nat Cancer 7, 316–333 (2026). https://doi.org/10.1038/s43018-025-01084-0
Trefwoorden: diffuse midline-glioma, hersenorganoïden, CAR-T-cellen, kinderhersenkanker, microglia