Clear Sky Science · nl
Voorspellen en interpreteren van celtypespecifieke geneesmiddelreacties in het kleine-data regime met inductieve priors
Waarom dit onderzoek belangrijk is voor toekomstige medicijnen
Wanneer een nieuw medicijn wordt getest, is een van de grootste onbekenden hoe verschillend het verschillende celtypen in ons lichaam zal beïnvloeden. Een verbinding die een celtype helpt, kan in een ander celtype weinig doen of zelfs schadelijk zijn. Deze informatie experimenteel genereren voor duizenden geneesmiddelen en talloze celtypen is veel te langzaam en te duur. Dit artikel introduceert een computergebaseerde benadering, PrePR-CT, die leert voorspellen hoe individuele celtypen op geneesmiddelen reageren, zelfs wanneer er slechts beperkte data beschikbaar zijn. Het werk wijst op snellere, goedkopere en nauwkeurigere manieren om potentiële geneesmiddelen in silico te verkennen voordat dure laboratorium- en klinische studies worden gestart.
In cellen kijken in plaats van alleen naar geneesmiddelen
Traditionele screenings van geneesmiddelen behandelen cellen vaak alsof ze allemaal hetzelfde zijn en richten zich vooral op bulkgemiddelden. In werkelijkheid kunnen immuuncellen, levercellen en kankercellen sterk verschillend reageren op dezelfde verbinding. De auteurs stellen dat om deze verschillen te voorspellen, een model de interne bedrading van elk celtype moet begrijpen: welke genen vaak samen actief zijn en hoe die patronen de identiteit van de cel bepalen. Ze bouwen celtype-"kaarten" door te onderzoeken welke genen in ongestoorde (controle)cellen gelijktijdig op- en neerdalen. Elke kaart wordt weergegeven als een netwerk, waarbij knopen genen voorstellen en verbindingen sterke co-activiteit weerspiegelen. Deze netwerken dienen als voorafgaande kennis over hoe een bepaald celtype georganiseerd is voordat een geneesmiddel wordt toegevoegd.
Een netwerkbewuste leerengine
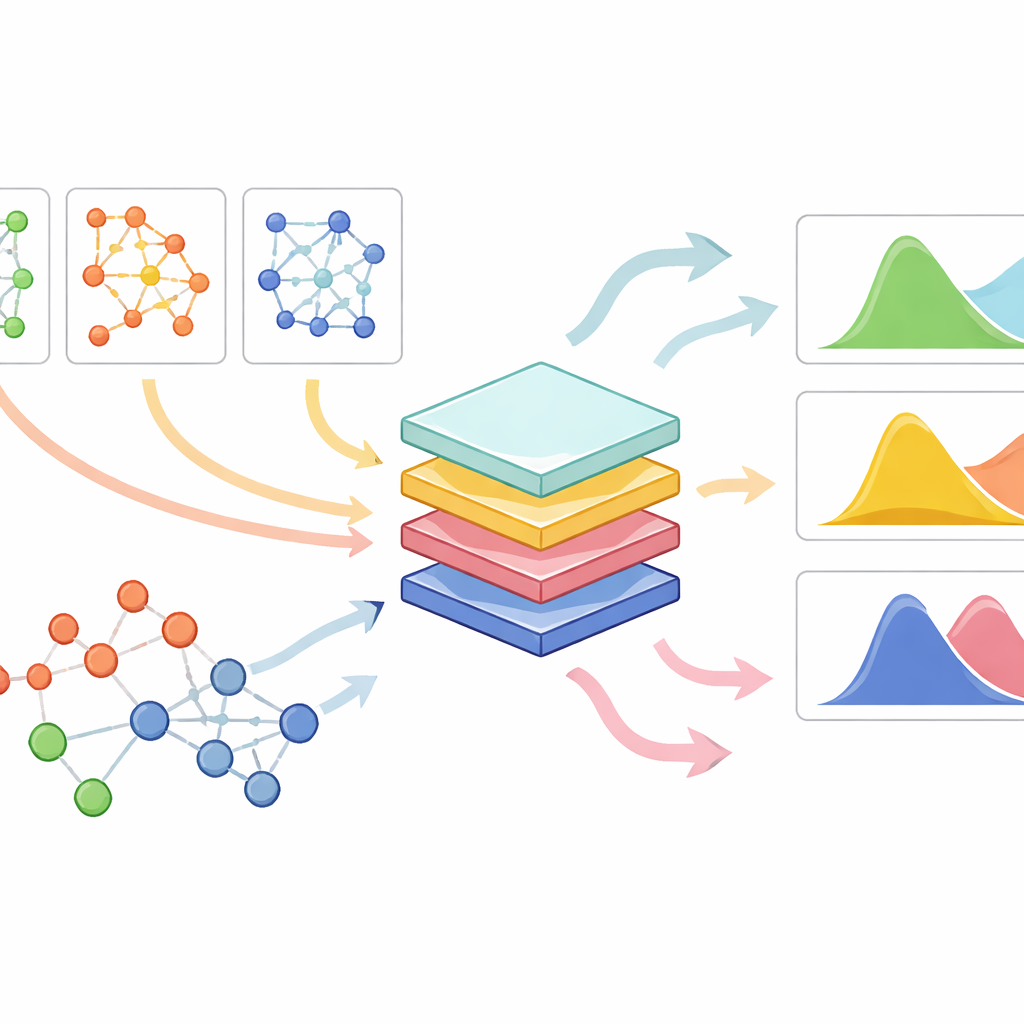
PrePR-CT combineert drie ingrediënten: het gen-activiteitsnetwerk van een celtype, de basislijn genexpressie van dat celtype en een compacte beschrijving van de chemische structuur van het geneesmiddel. Het model gebruikt een klasse neurale netwerken die is ontworpen voor grafen om het genen netwerk van de cel te verwerken en een samenvatting te extraheren die de karakteristieke patronen vastlegt. Parallel daaraan zet het elk geneesmiddel om in een numerieke vingerafdruk afgeleid van zijn moleculaire structuur. Deze onderdelen worden gevoed in een downstream voorspellingsmodule die, uit beschikbare experimenten, leert hoe een bepaald geneesmiddel de verdeling van genactiviteit in dat celtype zal verschuiven. In plaats van één getal per gen te produceren, schat de methode zowel de gemiddelde verandering als hoe variabel de reactie is over individuele cellen, wat cruciaal is om zowel subtiele als sterke effecten te begrijpen.
Werken over veel celtypen, geneesmiddelen en kleine datasets
De onderzoekers testten PrePR-CT op een brede verzameling datasets, waaronder menselijke bloedcellen blootgesteld aan immuunsignalen, meerdere kankercellijnen behandeld met verschillende verbindingen, muislevercellen blootgesteld aan een verontreinigende stof en grootschalige geneesmiddenschermen uit openbare bronnen. In uitdagende scenario's waarin een heel celtype tijdens het trainen werd weggelaten, kon het model nog steeds voorspellen hoe dat nieuwe celtype op een bekend geneesmiddel zou reageren, vaak met een nauwkeurigheid die eerdere generatieve modellen overtrof. Evenzo, wanneer een nieuw geneesmiddel maar een bekend celtype werd weggelaten, voorzag de methode succesvol de impact op basis van alleen de chemische vingerafdruk. Belangrijk is dat het model effectief bleef bij training op relatief kleine aantallen cellen, een situatie waarin veel deep learning-benaderingen moeite hebben.
Van black box naar aanwijzingen over het mechanisme
Buiten pure voorspelling wilden de auteurs weten of hun model inzicht kon geven in welke genen en paden de reactie van een cel aansturen. De grafgebaseerde architectuur bevat een attention-mechanisme dat genen markeert die het model als bijzonder invloedrijk in elk celtype beschouwt. Veel van deze "high-attention" genen waren niet de gebruikelijke verdachten die door standaard differentiële expressie-analyse worden gemarkeerd, maar ze clusterden in immuungerelateerde paden die consistent waren met de biologie van de geteste geneesmiddelen. Toen de onderzoekers deze invloedrijke genen opzettelijk verstoorden in de input van het model, daalde de voorspellingskwaliteit, vooral voor de meest reagerende genen, wat suggereert dat de attention-scores wijzen op betekenisvolle mechanistische spelers in plaats van ruis.
Wat dit betekent voor het ontwerpen van betere medicijnen
In eenvoudige bewoordingen laat dit werk zien dat het geven van kunstmatige-intelligentie-modellen van een gestructureerd beeld van hoe elk celtype is bekabeld — het interne genennetwerk — hun vermogen om te voorspellen hoe geneesmiddelen die cellen zullen hervormen sterk verbetert, zelfs wanneer maar beperkte data beschikbaar zijn. PrePR-CT vervangt experimenten niet, maar het kan helpen beperken welke verbindingen en celtypen het waard zijn om te testen en aanwijzingen geven waarom bepaalde cellen zo reageren. Naarmate datasets groeien en aanvullende cellulaire kenmerken worden opgenomen, kunnen dergelijke benaderingen sleuteltools worden voor het afstemmen van therapieën op specifieke weefsels of patiëntceltypen, het verminderen van trial-and-error in het laboratorium en het dichterbij brengen van preciezere geneesmiddelen in de praktijk.
Bronvermelding: Alsulami, R., Lehmann, R., Khan, S.A. et al. Predicting and interpreting cell-type-specific drug responses in the small-data regime using inductive priors. Nat Mach Intell 8, 461–473 (2026). https://doi.org/10.1038/s42256-026-01202-2
Trefwoorden: voorspelling van geneesmiddelrespons, single-cell transcriptomics, graph neural networks, geneesmiddelontdekking, celtypespecificiteit