Clear Sky Science · nl
Voorwaardelijke diffusie met lokaal-georiënteerde modale uitlijning voor het genereren van diverse proteïne-conformationele ensembles
Waarom beweging van eiwitten ertoe doet
Eiwitten in onze cellen zijn geen starre sculpturen; ze gedragen zich meer als kleine, flexibele machines die voortdurend van vorm veranderen. Deze vormveranderingen kunnen bepalen hoe enzymen reacties katalyseren, hoe receptoren op geneesmiddelen reageren en hoe signalen door cellen stromen. Toch tonen de meest bekende afbeeldingen van eiwitten vaak slechts één "momentopname" en missen daarmee het rijke ensemble aan vormen dat in werkelijkheid bestaat. Dit artikel introduceert Mac-Diff, een kunstmatige-intelligentie-methode die snel vele realistische vormen voor een gegeven eiwit kan genereren, waardoor wetenschappers niet alleen zien hoe een eiwit eruitziet, maar ook hoe het ademt en beweegt.
Van enkele snapshots naar bewegende ensembles
Decennialang vertrouwden onderzoekers op arbeidsintensieve experimenten of langdurige moleculaire-dynamica-simulaties om eiwitbeweging te onderzoeken, die beide traag en kostbaar kunnen zijn. Doorbraaktools zoals AlphaFold2 voorspellen nu direct uit de aminozuurvolgorde de meest waarschijnlijke 3D-structuur van een eiwit, maar leveren meestal slechts één of enkele voorkeursvormen op. Veel eiwitten, vooral die betrokken bij signaaloverdracht en allosterische regulatie, bezetten van nature meerdere, vaag omschreven toestanden. De auteurs stellen dat om te begrijpen hoe zulke eiwitten echt werken — en om geneesmiddelen te ontwerpen die binden aan minder voor de hand liggende, tijdelijke vormen — we een manier nodig hebben om volledige ensembles van plausibele conformaties te genereren, niet slechts één beste gok.
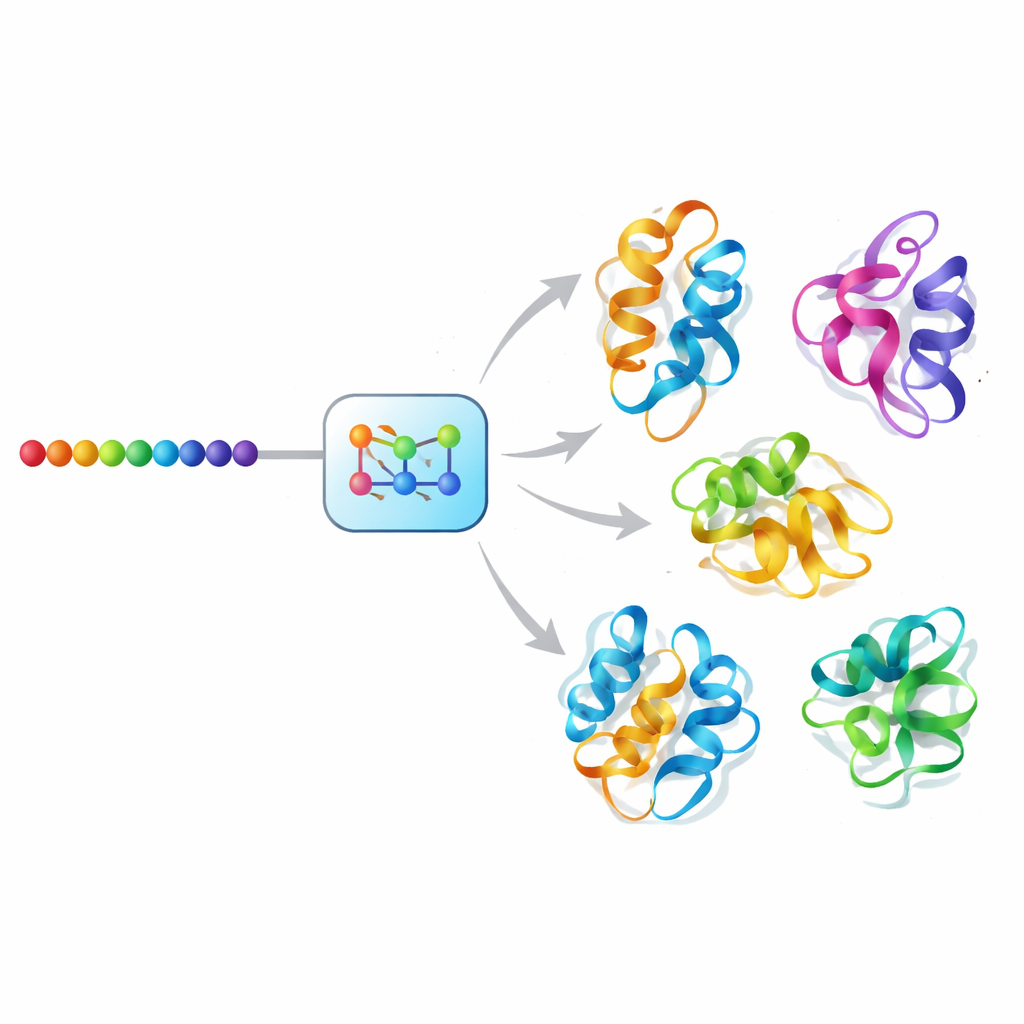
Een AI-diffusiebenadering voor eiwitbeweging
Mac-Diff pakt deze uitdaging aan met een generatief model in diffusiestijl, een klasse AI die recente sprongen in beeldsynthese heeft aangedreven. In plaats van ruis uit foto’s te verwijderen, denoist Mac-Diff abstracte geometrische beschrijvingen van eiwitruggen. Het model stelt een eiwit voor als een raster van paargewijze relaties tussen residuen — afstanden en hoeken die ongevoelig zijn voor rotatie of translatie van het hele molecuul. In een voorwaartse stap voegt het systeem geleidelijk ruis toe aan deze geometrische patronen totdat ze op willekeurige ruis lijken. In de omgekeerde stap leert het stapsgewijs die ruis te verwijderen, gestuurd door de aminozuurvolgorde van het eiwit, totdat coherente, 3D-compatibele geometrieën terugkeren, die daarna met standaard structurele opbouwsoftware in volledige atomaire modellen kunnen worden omgezet.
Lokale verbinding tussen sequentie en structuur
Een belangrijke innovatie zit in hoe Mac-Diff een lineaire sequentie van residuen koppelt aan hun 3D-buren. Elk residu simpelweg elk ander residu laten 'aandacht schenken', zoals in tekst-naar-beeldmodellen, zou belangrijke fysische beperkingen vervagen. In plaats daarvan introduceren de auteurs een "locality-aware" aandachtmechanisme dat elk residu focust op een klein, waarschijnlijk burenbestand van interactiepartners. Om deze buurten te schatten gebruikt Mac-Diff drie ingrediënten: een proteïnen taalmodel genaamd ESM-2 dat de biochemische context van elk residu codeert; een contactmap die hint welke residuparen waarschijnlijk dicht bij elkaar zitten; en een eenvoudige regel die residuen bevoordeelt die dicht bij elkaar in de keten liggen. Deze signalen worden gecombineerd zodat het model tijdens het denoising preferential informatie gebruikt van residuen die fysisch plausibele partners zijn, waardoor het zijn vermogen aanscherpt om realistische, flexibele structuren te reconstrueren.
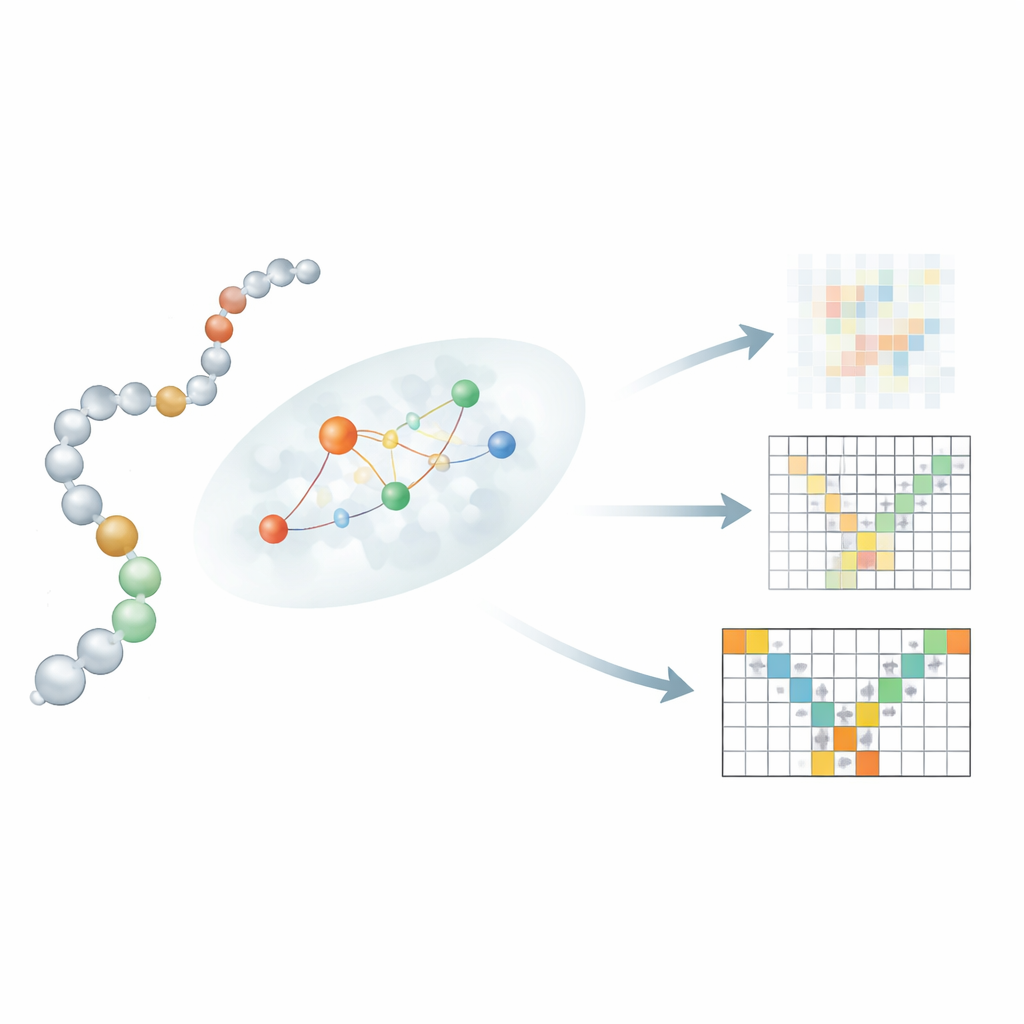
Testen tegen lange simulaties en vormveranderende eiwitten
De onderzoekers testten Mac-Diff op twee veeleisende fronten. Ten eerste onderzochten ze of het de brede verdeling van vormen kon reproduceren die in lange, zorgvuldig berekende moleculaire-dynamica-simulaties van snel vouwende eiwitten en een klassiek benchmark-eiwit bekend als BPTI werden waargenomen. Over verschillende maten die statistische eigenschappen van de gegenereerde ensembles met simulatiegegevens vergelijken — zoals verdelingen van afstanden binnen het eiwit en de algehele compactheid — presteerde Mac-Diff gelijk of beter dan concurrerende AI-methoden, en genereerde het bovendien een grotere verscheidenheid aan conformaties. Het ving de meeste sleutel-"metastabiele" toestanden die in de simulaties werden geïdentificeerd en reproduceerde flexibiliteitspatronen op residuniveau met hoge correlatie, wat aangeeft dat zijn ensembles zowel globale vouwing als lokale bewegelijkheid realistisch weergeven.
Verborgen functionele toestanden onthullen
Ten tweede daagde het team Mac-Diff uit met eiwitten die bekendstaan om het aannemen van zeer verschillende vormen tijdens hun functie, waaronder het enzym adenylatekinase, dat tijdens het energiemetabolisme tussen open en gesloten vormen schakelt, en een gecureerde set van 40 eiwitten met elk twee experimenteel bepaalde conformaties. Mac-Diff genereerde slechts 100 kandidaat-structuren per eiwit — veel minder dan typische simulatie-trajectory’s — maar vond toch de meeste bekende toestanden terug met goede geometrische overeenkomst. In adenylatekinase produceerde het bijvoorbeeld zowel open als gesloten conformaties met hoge gelijkheid aan kristalstructuren, terwijl verschillende populaire methoden geneigd waren maar één toestand te bevoordelen. Het model draaide ook ongeveer duizend keer sneller dan conventionele simulaties op vergelijkbare hardware, waardoor systematische verkenning van vormdiversiteit veel praktischer wordt.
Wat dit betekent voor biologie en geneeskunde
In gewone bewoordingen verandert Mac-Diff de sequentie van een eiwit in een galerij van plausibele houdingen in plaats van een enkel portret, en doet dat met aandacht voor welke delen waarschijnlijk tegen elkaar duwen of elkaar vastgrijpen in 3D. Door deze ensembles nauwkeurig en efficiënt te bemonsteren biedt de methode een manier om te onderzoeken hoe subtiele verschuivingen in vorm ten grondslag liggen aan functie, om zeldzame maar belangrijke conformaties op te sporen en om naar geneesmiddelbindingspockets te zoeken die alleen in transiënte toestanden verschijnen. Hoewel het nog niet de volledig tijdgeordende films vastlegt die simulaties bieden, brengt Mac-Diff het dynamische landschap van eiwitten binnen bereik van veel meer systemen en belooft het nieuwe inzichten in structurele biologie, geneesmiddelenontwerp en eiwitengineering.
Bronvermelding: Wang, B., Wang, C., Chen, J. et al. Conditional diffusion with locality-aware modal alignment for generating diverse protein conformational ensembles. Nat Mach Intell 8, 415–434 (2026). https://doi.org/10.1038/s42256-026-01198-9
Trefwoorden: proteïnedynamica, diffusiemodellen, conformationele ensembles, allosterische eiwitten, geneesmiddelenontdekking