Clear Sky Science · nl
Herbruikbaarheidsrapport: Evaluatie van de prestaties van een meta-learning foundation-model bij het voorspellen van de antibacteriële werking van natuurlijke producten
Sneller op zoek naar nieuwe antibiotica
Resistentie tegen antibiotica neemt toe, terwijl het ontdekken van nieuwe medicijnen pijnlijk traag is en vaak afhangt van trial-and-error in het laboratorium. Deze studie onderzoekt of een krachtig soort kunstmatige intelligentie, oorspronkelijk getraind op enorme verzamelingen medicijngegevens, snel kan worden aangepast om te voorspellen welke plantaardige natuurlijke verbindingen mogelijk bacteriën bestrijden — met slechts kleine hoeveelheden nieuwe experimentele data. Als dat lukt, kunnen zulke hulpmiddelen wetenschappers helpen om kostbare labtijd te richten op de meest veelbelovende kandidaten en de zoektocht naar de volgende generatie antibiotica te versnellen.
Waarom plantaardige chemicaliën ertoe doen
Veel van onze beste antibiotica begonnen als natuurlijke producten uit planten en micro-organismen. Deze moleculen kunnen de groei van bacteriën remmen, maar het vinden van nieuwe exemplaren in de natuur is een beetje als zoeken naar een speld in een hooiberg. Onderzoekers moeten veel verbindingen tegen veel bacteriestammen testen, en elke test is kostbaar. Bovendien zijn grote, zorgvuldig gelabelde datasets — die moderne deep-learningmethoden nodig hebben om goed te presteren — zeldzaam op dit gebied. Dat maakt de ontdekking van antibiotica een ideaal proefveld voor "foundation models": grote, algemeen toepasbare AI-systemen die met slechts een handvol nieuwe voorbeelden voor specifieke taken bijgeschaafd kunnen worden.
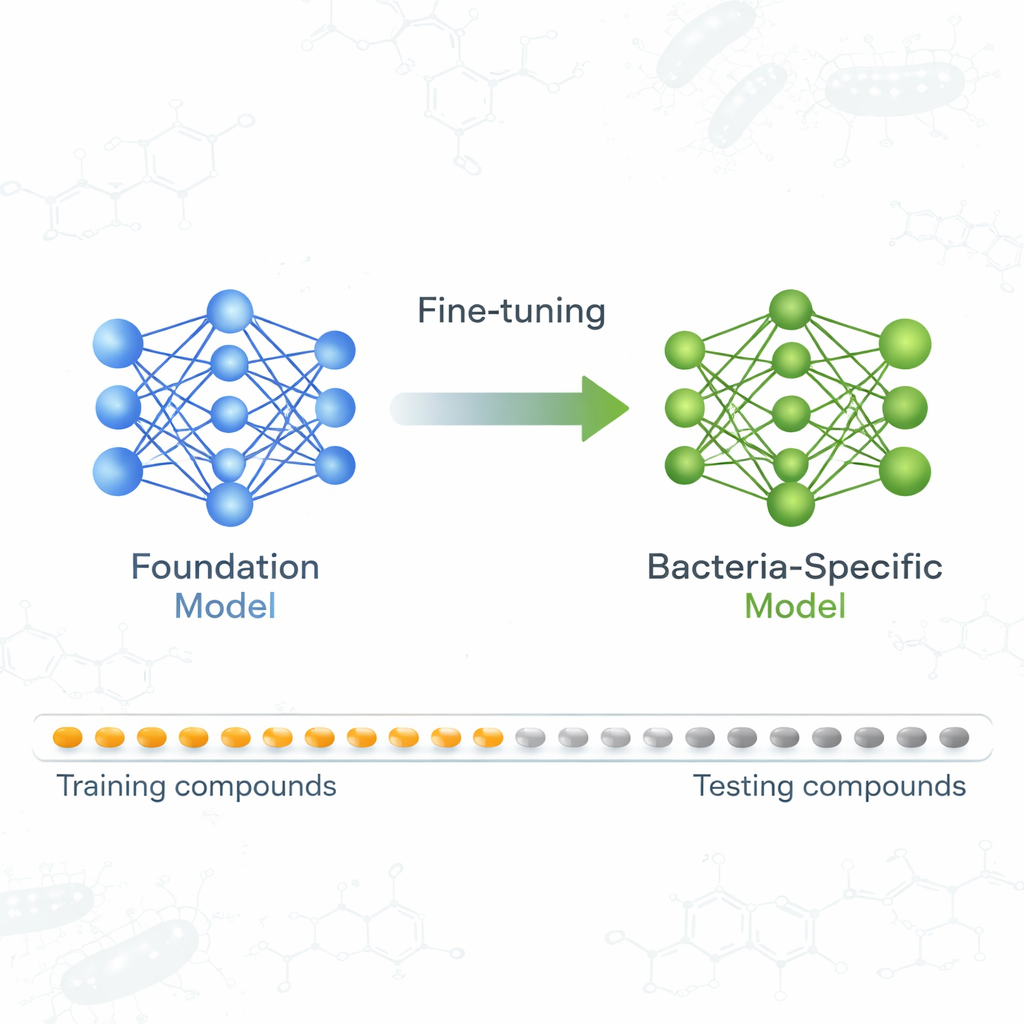
Een foundation-model leert over kiemdoders
Het team richtte zich op een foundation-model genaamd ActFound, oorspronkelijk getraind om te voorspellen hoe sterk verschillende chemicaliën biologische doelen beïnvloeden, met gebruik van grote datasets uit bronnen zoals de ChEMBL- en BindingDB-databanken. In plaats van voor elke verbinding één getal te voorspellen, leert ActFound door paren van verbindingen binnen hetzelfde experiment te vergelijken en in te schatten welke actiever is. Dit "pairwise"-leren, gecombineerd met een trainingsstrategie bekend als meta-learning, is ontworpen om het model in staat te stellen zich snel aan te passen aan nieuwe voorspellingstaken wanneer slechts een klein aantal gelabelde voorbeelden beschikbaar is — precies de situatie bij veel antibioticumscreenings.
Het model testen op echte plantaardige data
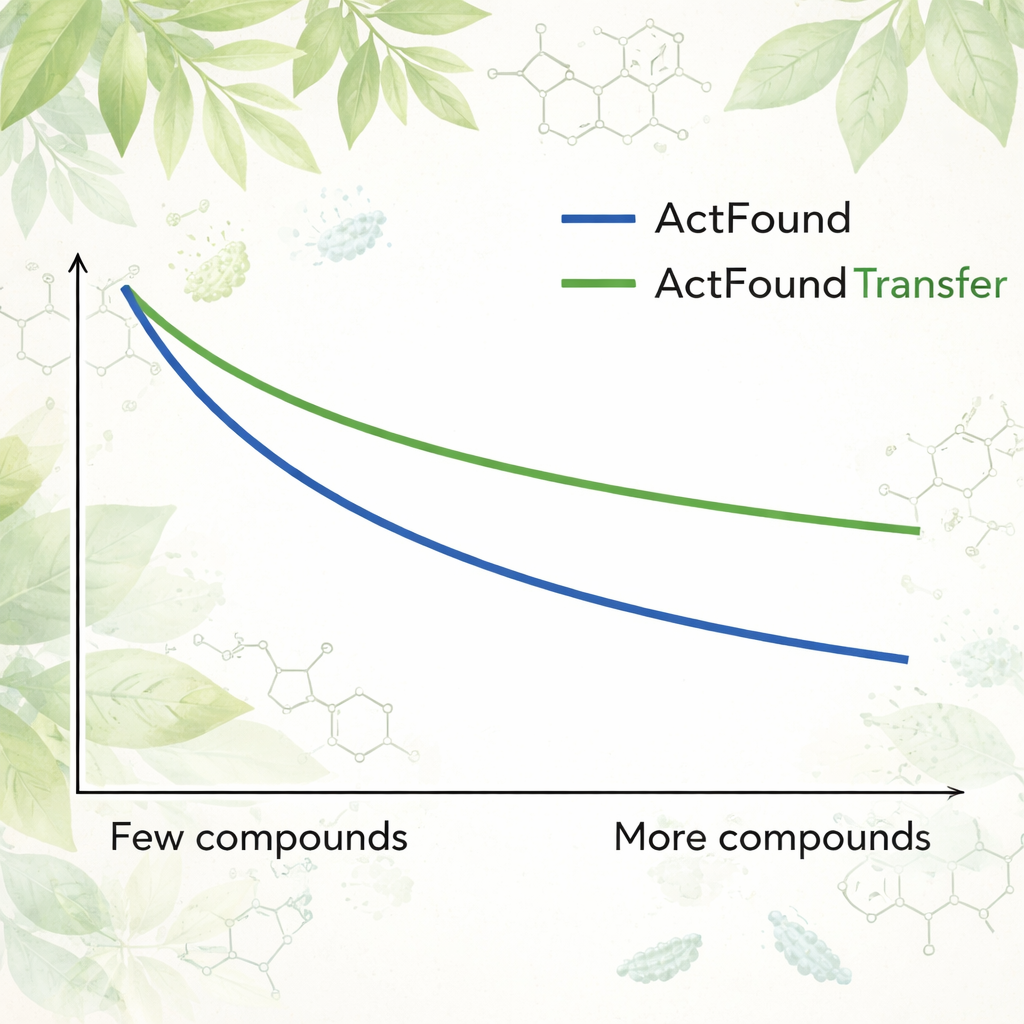
Om te onderzoeken hoe herbruikbaar ActFound werkelijk is, hebben de auteurs het fijngeslepen op een zorgvuldig samengestelde dataset van plantaardige natuurlijke producten die getest werden op hun vermogen de groei van verschillende bacteriën te remmen. Elke bacteriestam werd als een eigen taak behandeld, en het model werd aangepast met slechts 8 tot 128 verbindingen per stam, of met vaste percentages van de beschikbare data. Ze vergeleken ActFound ook met eenvoudigere meta-learning- en transfer-learningmodellen die geen pairwise-vergelijkingen gebruiken. Over deze tests heen behaalde ActFound niet de nauwkeurigheid die in eerdere studies op andere typen medicijngegevens werd getoond. Echter, wanneer zeer weinig data beschikbaar waren — ruwweg slechts een handvol verbindingen per stam — presteerden ActFound en de transfer-learningvariant meestal gelijk aan of beter dan alternatieve methoden.
Wanneer gelijkenis helpt — en wanneer het tegenwerkt
ActFound veronderstelt dat gelijksoortige moleculen zich op vergelijkbare wijze gedragen, wat goed werkt wanneer datasets zijn opgebouwd rond groepen verwante chemicaliën. De natuurlijke-productdataset was echter chemisch divers en miste vaak nauw verwante "families" van verbindingen. Deze diversiteit, hoewel wetenschappelijk waardevol, ondermijnde de pairwise-leeraanpak: wanneer verbindingen binnen een experiment sterk van elkaar verschillen, heeft het model moeite om stabiele vergelijkingen te leren. De auteurs ontdekten ook dat een eenvoudige diagnostische maatstaf, voorgesteld in het oorspronkelijke ActFound-artikel om vooraf te voorspellen hoe goed het model op een nieuwe taak zou presteren, niet standhield voor deze natuurlijke-productgegevens, wat een belangrijke beperking benadrukt bij de overgang naar nieuwe chemische ruimtes.
Wat dit betekent voor toekomstige geneesmiddelenontdekking
Voor niet-specialisten is de conclusie dat foundation-modellen zoals ActFound veelbelovende hulpmiddelen zijn voor geneesmiddelenontdekking wanneer data schaars zijn, maar dat ze geen wondermiddelen zijn. In deze studie presteerden ActFound en de transfer-learningversie vaak even goed als of beter dan concurrerende methoden wanneer slechts een paar plantverbindingen beschikbaar waren voor training, maar ze hadden moeite met deze sterk diverse set natuurlijke producten. Het werk suggereert dat deze AI-modellen het meest nuttig zijn wanneer de data veel chemisch vergelijkbare verbindingen bevatten — zoals in gerichte studies naar structuur–activiteitrelaties — maar dat ze minder betrouwbaar blijven voor het voorspellen van het gedrag van volledig nieuwe soorten moleculen. Met andere woorden: AI kan helpen de zoektocht te verkleinen, maar het moeilijkste deel van het verkennen van echt nieuw chemisch terrein ligt nog voor ons.
Bronvermelding: Butt, C.M., Walker, A.S. Reusability Report: Evaluating the performance of a meta-learning foundation model on predicting the antibacterial activity of natural products. Nat Mach Intell 8, 270–275 (2026). https://doi.org/10.1038/s42256-026-01187-y
Trefwoorden: ontdekking van antibiotica, natuurlijke producten, deep learning, meta-learning, geneesmiddelenscreening