Clear Sky Science · nl
PLIN5-fosforylering orkestreert koppeling tussen mitochondriën en lipidedruppels om leverlipidenstroom en steatose te regelen
Waarom levervet ertoe doet
Veel mensen hebben extra vet in hun lever zonder zich ziek te voelen, maar deze stille ophoping kan uiteindelijk leiden tot ontsteking, littekenvorming en zelfs kanker. Deze studie stelt een eenvoudige maar cruciale vraag: als golven vet de lever binnenstromen tijdens vasten of door een vetrijke "Westerse" voeding, hoe beslissen levercellen dan of dat vet wordt verbrand voor energie of veilig wordt opgeslagen, en wanneer begint dit veiligheidssysteem te falen?
Kleine energiecentrales en kleine vetbubbels
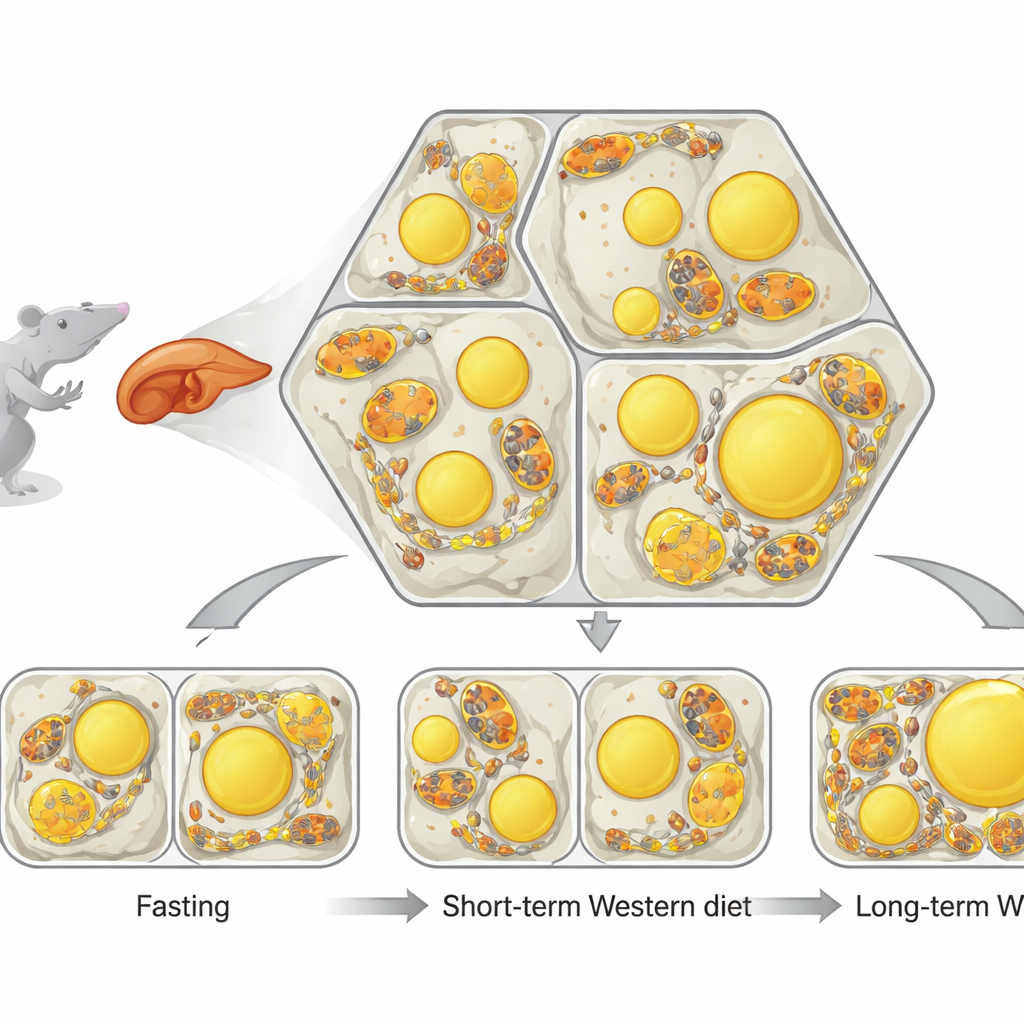
De lever is georganiseerd in repeterende, zeshoekige eenheden waar bloed van de ene naar de andere kant stroomt. Langs dit traject specialiseren levercellen zich: sommige verbranden voornamelijk vet voor energie, terwijl andere vooral vet maken en opslaan. Binnen elke cel zijn twee structuren essentieel. Mitochondriën zijn de energiecentrales van de cel, en lipidedruppels zijn kleine met vet gevulde belletjes voor opslag. De onderzoekers ontwikkelden een krachtige beeldvormings- en analysepijplijn, genoemd single-cell phenotypic profiling (scPhenomics), om de grootte, vorm en ordening van deze structuren in duizenden cellen rechtstreeks in weefseldunne secties in kaart te brengen. Ze ontdekten dat zelfs bij gezonde dieren de vorm van mitochondriën en de hoeveelheid lipidedruppels duidelijke ruimtelijke patronen vormt die weerspiegelen waar verbranding versus opslag normaal gesproken in de lever plaatsvindt.
Vasten versus een vetrijke voeding
Vervolgens onderzocht het team wat er gebeurt wanneer de lever plotseling met vet wordt overspoeld. Vasten drijft vet uit de lichaamsvetreserves naar de lever, terwijl een korte Westerse-achtige voeding extra vet rechtstreeks uit voedsel levert. Bij gevasten muizen namen lipidedruppels in de hele lever toe, en werden mitochondriën langer en vaak nauw om deze vetbubbels heen gewikkeld, waardoor veel contactplaatsen ontstonden. Bij muizen die enkele weken een Westerse voeding kregen, raakte de lever ook met vet gevuld, maar de druppels waren anders gerangschikt en mitochondriën bleven grotendeels gescheiden en ronder. Dit toonde aan dat de manier waarop vet arriveert — via vasten of chronisch vetrijke voeding — zeer verschillende structurele reacties in levercellen uitlokt, zelfs wanneer het totale vetgehalte vergelijkbaar lijkt.
Een moleculaire schakelaar voor vetverwerking
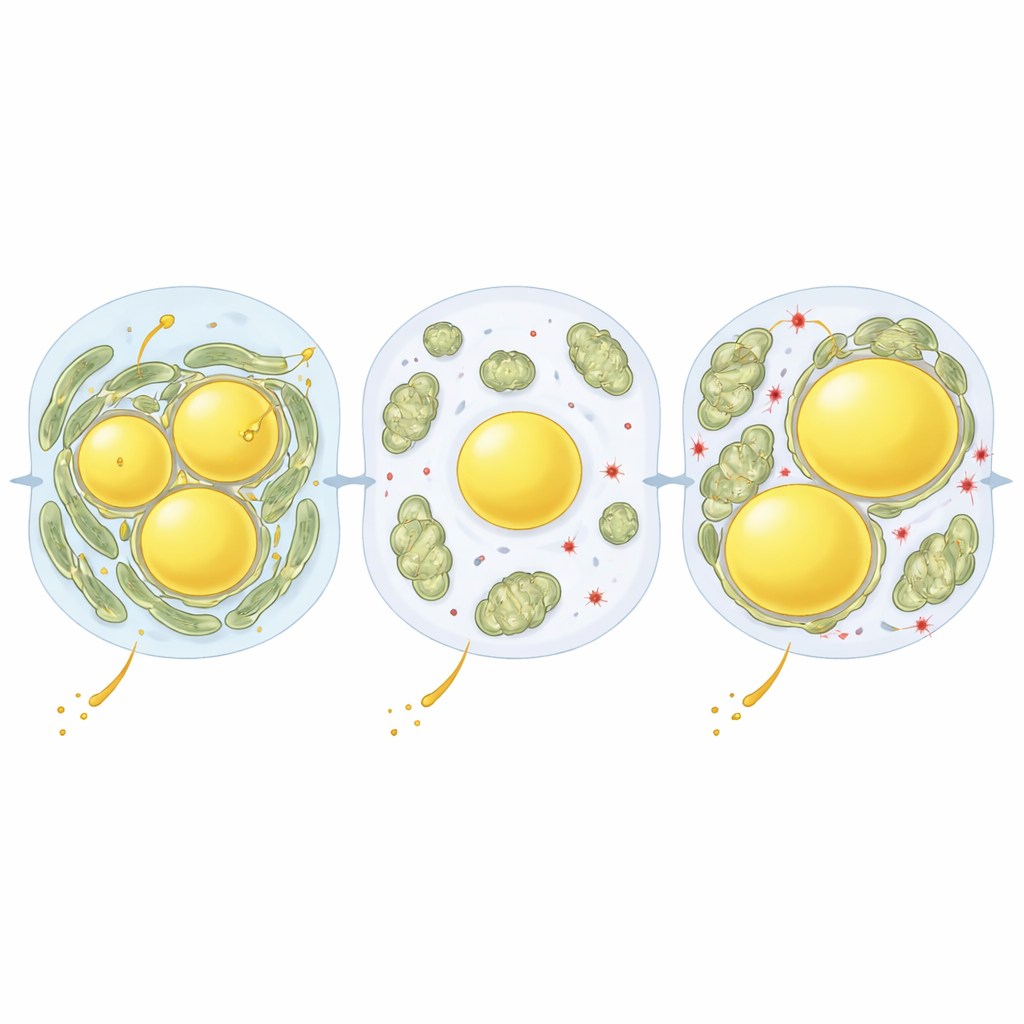
Om te achterhalen wat deze organelcontacten regelt, combineerden de auteurs hun beeldanalyse met eiwitmetingen in levercellen afkomstig uit verschillende zones en dieetcondities. Eén opvallend eiwit was perilipine‑5 (PLIN5), dat lipidedruppels bekleedt en mitochondriën eraan kan vasthechten. Vasten verhoogde PLIN5-niveaus en positioneerde het precies op het snijvlak tussen mitochondriën en druppels. De onderzoekers gebruikten vervolgens een levergericht virus om PLIN5-niveaus te verhogen en versies van het eiwit te testen die verschillende aan/uit-staten van een enkele chemische markering, fosforylering genoemd, nabootsen. Een versie die niet gefosforyleerd kon worden (S155A) vergrootte sterk de mitochondriën–druppelcontacten en maakte vetdruppels groter, zelfs bij een normaal dieet. Een versie die constante fosforylering nabootste (S155E) deed het tegenovergestelde: mitochondriën raakten zelden druppels aan, die minder en kleiner bleven.
Cellen beschermen tegen vetgeïnduceerde schade
Het team onderzocht vervolgens wat dit betekende voor levergezondheid onder een Westerse voeding. Toen muizen deze voeding enkele weken aten, dreef de niet-fosforyleerbare PLIN5-variant (S155A) meer vet in druppels en verhoogde het triglyceridengehalte in de lever, maar markers van schadelijke oxidatieve stress waren juist lager. Daarentegen liet de fosfo-mimetische versie (S155E) meer vrij vet en tekenen van een meer oxiderende, potentieel schadelijke omgeving zien, met lagere antioxidantreserves. In wezen leken nauwe samenwerkingen tussen mitochondriën en lipidedruppels te fungeren als een veiligheidsklep die overtollige vetzuren in neutrale opslag kan leiden en de kettingreacties die membranen en eiwitten beschadigen beperkt. Bij langdurigere voeding met veel vet namen mitochondriën–druppelcontacten echter weer toe en waren ze geassocieerd met zwaardere vetbelasting in zowel muizen- als menselijk leversamples, wat erop wijst dat dezelfde beschermende bedrading overbelast kan raken en bijdraagt aan ziekteprogressie.
Een nieuw aangrijpingspunt voor levervetziekte
Alles bij elkaar laat dit werk zien dat levercellen actief de fysieke relaties tussen hun energiecentrales en vetopslag herbedraden om om te gaan met veranderende voedingscondities. PLIN5, en in het bijzonder de fosforyleringsstatus op één enkele plaats, werkt als een fijnregelkraan die de koppeling tussen mitochondriën en lipidedruppels versterkt of versoepelt. Strakke koppeling bevordert het verpakken van potentieel toxische vrije vetten in veiligere triglyceridestores en helpt kortdurende voedingsstress, zoals vasten of korte blootstelling aan een vetrijk dieet, te bufferen. Wanneer dit adaptieve programma verzwakt is, of wanneer langdurige vetrijke blootstelling maanden of jaren aanhoudt, kantelt het evenwicht naar lipotoxiciteit en oxidatieve schade. Door deze structurele "circuit" binnen levercellen bloot te leggen, suggereert de studie dat medicijnen die PLIN5-activiteit of mitochondriën–druppelcontacten moduleren, een nieuwe manier kunnen bieden om vetleverziekte bij mensen te vertragen of te voorkomen.
Bronvermelding: Kang, S.W.S., Brown, L.A., Miller, C.B. et al. PLIN5 phosphorylation orchestrates mitochondria lipid-droplet coupling to control hepatic lipid flux and steatosis. Nat Metab 8, 587–603 (2026). https://doi.org/10.1038/s42255-026-01476-1
Trefwoorden: vettige leverziekte, levermetabolisme, mitochondriën, lipidedruppels, perilipine 5