Clear Sky Science · nl
PFKM regelt metabole verschuivingen tijdens de differentiatie van skeletspier
Waarom spiercellen slim met suiker moeten omgaan
Wanneer we bewegen of simpelweg opstaan uit een stoel, schakelen onze skeletspieren snel en verbranden ze suiker om elke contractie van energie te voorzien. Jonge spierstamcellen en volledig gevormde spiervezels gaan echter anders met suiker om. Deze studie onthult een ingebouwd schakelmechanisme — gecentreerd rond één enzym genaamd PFKM — dat bepaalt of glucose wordt verbrand voor directe energie of wordt omgeleid om cellen te beschermen en te herstellen. Inzicht in deze schakel kan nieuwe wegen openen voor de behandeling van spierzwakte, verouderende spieren en erfelijke stofwisselingsziekten.
Een stoplicht voor cellulaire brandstof
Inkomende glucose kan in een cel verschillende routes volgen. Een belangrijke weg, glycolyse, zet suiker snel om in energie en bouwstenen voor groeiende spiervezels. Een andere route, de pentosefosfaatroute, produceert moleculen die cellen beschermen tegen schadelijke zuurstofstress en ondersteunt de synthese van DNA en lipiden. De onderzoekers richtten zich op PFKM, een variant van het enzym fosfofructokinase-1 dat op een cruciale kruising in de glycolyse zit. Door honderden metabolieten te meten over minuten tot uren na activatie van een groeisignaal genaamd Wnt, ontdekten ze dat cellen snel vroege glycolyse-intermediaten ophoopten terwijl het product van PFKM daalde en metabolieten van de pentosefosfaatroute stegen. Dit suggereerde dat cellen PFKM actief terugschroefden om suiker om te leiden naar beschermende chemie in plaats van puur energieproductie. 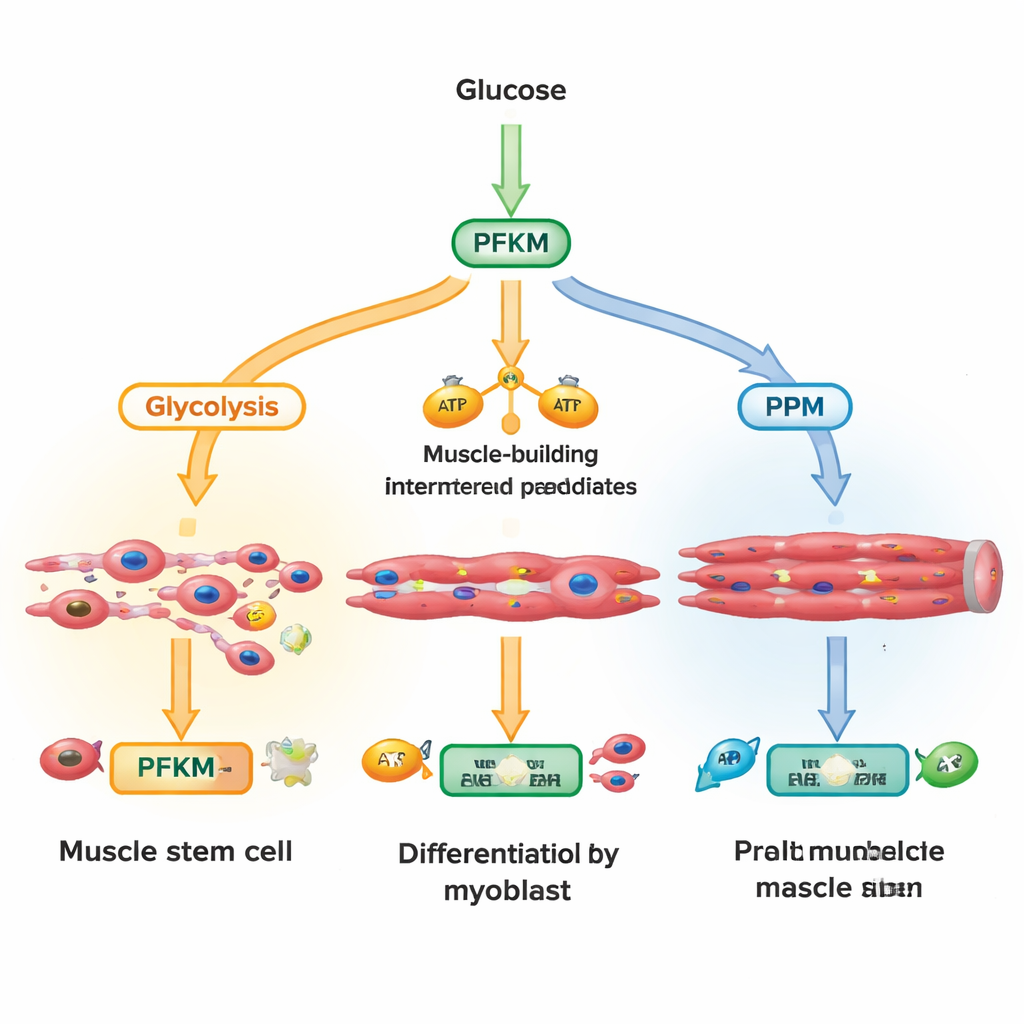
Het markeren en verwijderen van de poortwachter
Om te zien hoe PFKM wordt geregeld, volgde het team waar het eiwit zich in de cellen bevindt. In rust zweefde PFKM door het cytoplasma. Binnen enkele minuten na Wnt-stimulatie verzamelde het zich in heldere vlekken die samenvielen met lysosomen, de eiwitverslindende compartimenten van de cel. Twee verwante enzymen, PFKL en PFKP, verplaatsten zich niet en veranderden niet van niveau, wat aantoont dat alleen het spier-type PFKM werd gericht. Biochemische tests lieten zien dat het blokkeren van lysosomale functie verlies van PFKM voorkwam, terwijl remming van het proteasoom — het andere belangrijke eiwitafbraaksysteem — geen effect had. Volgordeanalyse onthulde een korte "methyl-arginine degron"-motief dat uniek is voor PFKM. Het enzym PRMT1 voegde een specifieke methylgroep toe op een arginine binnen dit motief, en dit etiket maakte het mogelijk dat microautofagie-machinerie, waaronder het eiwit VPS4, PFKM in lysosomen trok voor afbraak. Het uitschakelen van PRMT1 of VPS4 stabiliseerde PFKM en blokkeerde zijn verwijdering.
Van stamcel tot werkende spiervezel
Met grote menselijke single-cell datasets brachten de auteurs PFKM-niveaus in kaart over vele spiertypecellen. Spierstamcellen, die sluimeren tot ze nodig zijn voor herstel, hadden zeer weinig PFKM maar drukten veel genen van de pentosefosfaatroute en lysosomale componenten uit. Naarmate cellen zich committeerden aan spierwording en samensmolten tot multinucleaire vezels, stegen PFKM-transcripten en -eiwit sterk, terwijl Wnt-doelgenen en lysosomale genen afnamen. In gekweekte menselijke en muizencellen dreef Wnt snel PFKM naar lysosomen in vroege, enkelkernige cellen maar niet in rijpe multinucleaire vezels. Dit patroon ondersteunt een model waarin ongedifferentieerde cellen PFKM laag houden — via lysosomale afbraak — om beschermend metabolisme te bevorderen, en het vervolgens opnieuw tot expressie brengen wanneer ze overgaan naar energievragende contractiele vezels.
Wat gebeurt er als de schakel vastzit
Om te testen hoe cruciaal PFKM is voor spieropbouw, verlaagde het team de niveaus met RNA-interferentie. Cellen met lage PFKM hadden moeite om karakteristieke spiergenen aan te zetten, produceerden minder myosine-eiwit en vormden minder en kleinere multinucleaire vezels, hoewel het totale celtal ongewijzigd bleef. Metabole profilering toonde verminderde downstream glycolyse-intermediaten en brandstoffen voor de tricarboxylzuurcyclus, maar toegenomen pentosefosfaatgenen en -markers, samen met een verhoogde weerstand tegen oxidatieve stress. Belangrijk: het voorzien van cellen met 3‑fosfoglyceraat — een glycolytisch intermediaat dat normaal stroomafwaarts van PFKM ligt — herstelde veel van de differentiatie‑defecten. Spiermarkers en vezelvorming veerden terug, wat laat zien dat ontbrekende metabolieten, in plaats van het verlies van het PFKM-eiwit zelf, de belangrijkste bottleneck waren. 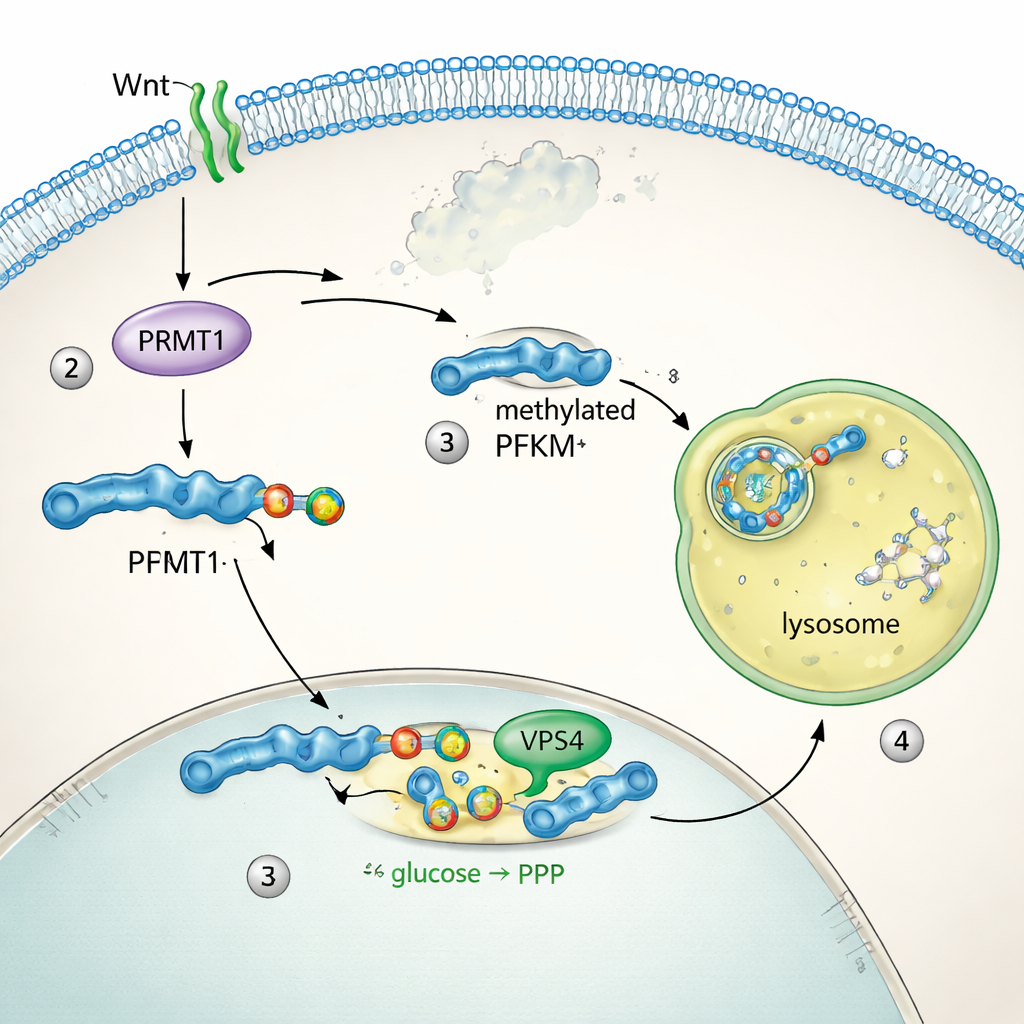
Gevolgen voor spiergezondheid en herstel
Voor niet‑specialisten is de kernboodschap dat spiercellen niet simpelweg meer of minder "suiker verbranden"; ze leiden het zorgvuldig om tussen energieproductie en celbescherming afhankelijk van hun levensstadium. PFKM functioneert als een regelbare klep op deze kruising. In stamcellen richten Wnt-gedreven markering en lysosomale afbraak van PFKM glucose om naar een route die cellen beschermt en voorbereidt op toekomstige groei. Terwijl cellen rijpen tot werkende vezels, bouwen ze PFKM-voorraden weer op en verschuift het metabolisme naar hoge energie-output. Het verstoren van dit evenwicht, zoals gezien bij zeldzame PFKM-tekortstoornissen, verstoort normale spierontwikkeling. Door de moleculaire hendel van deze schakel bloot te leggen, suggereert de studie dat toekomstige therapieën mogelijk de spierregeneratie kunnen bijsturen of spieren kunnen beschermen bij ziekte en veroudering door PFKM-activiteit voorzichtig te moduleren of de juiste downstreammetabolieten te leveren.
Bronvermelding: Campos, M., Nguyen, S.T., Kong, X. et al. PFKM governs metabolic shifts throughout skeletal muscle differentiation. Nat Metab 8, 489–505 (2026). https://doi.org/10.1038/s42255-026-01457-4
Trefwoorden: differentiatie van skeletspier, glucosemetabolisme, PFKM-enzym, pentosefosfaatroute, lysosomale eiwitafbraak