Clear Sky Science · nl
Voeding-gekoppelde glycogeenmetabolisme stuurt ritmische eiwitsecretie door de lever
Waarom het dagelijkse ritme van de lever ertoe doet
De meesten van ons denken na over wat we eten, maar niet over wanneer onze lever stilletjes essentiële eiwitten verpakt en in het bloed afgeeft. Deze studie onthult dat het "verzendschema" van levereiwitten beslist niet constant is: het volgt een dagelijks ritme dat sterk afhangt van wanneer we eten en van hoe de lever opgeslagen suiker, glycogeen, gebruikt. Inzicht in dit tijdmeetsysteem helpt verklaren waarom maaltijdtiming, obesitas en bepaalde zeldzame genetische aandoeningen hormonen, stollingsfactoren en vele andere bloed-eiwitten die het lichaam in balans houden, kunnen ontregelen.
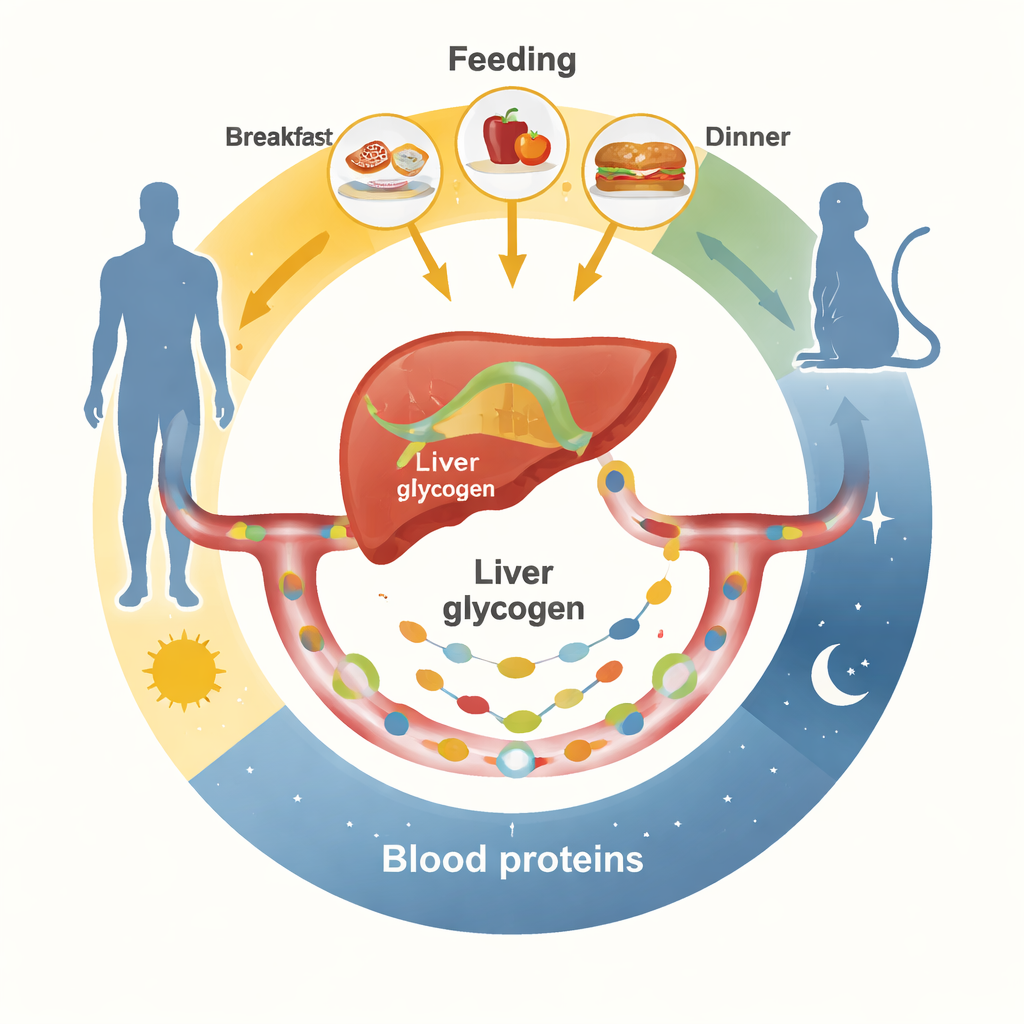
Maaltijden zetten het ritme voor bloedeiwitten
De onderzoekers volgden eerst honderden bloedeiwitten gedurende 24 uur bij gezonde mannen onder twee gecontroleerde voedingspatronen. In het ene patroon aten proefpersonen reguliere maaltijden; in het andere werden dezelfde totale calorieën gelijkmatig over de waakdag verspreid. Bij reguliere maaltijden stegen en daalden veel bloedeiwitten in duidelijke dagelijkse golven, vaak met pieken vroeg in de ochtend en laat in de middag. Tot deze eiwitten behoorden metabolische hormonen, stollingsfactoren, immuuneiwitten en transporteiwitten die grotendeels door de lever worden gemaakt. Wanneer voedsel daarentegen langzaam en continu werd genuttigd, vlakte het merendeel van deze ritmes uit. Vergelijkbare experimenten in muizen, waarbij voedsel óf voortdurend beschikbaar was óf alleen binnen afgebakende dag- of nachtramen, toonden aan dat het wijzigen van het voedingsschema krachtig bepaalt welke eiwitten in het bloed ritmisch zijn en wanneer ze pieken.
De secretielijn van de lever draait op een klok
Om te achterhalen hoe deze patronen ontstaan, keek het team in de lever. Zij vonden dat de eiwitten die betrokken zijn bij de klassieke "secretieweg" — waarbij nieuw gemaakte eiwitten de endoplasmatische reticulum (ER) binnengaan, in het Golgi-apparaat worden gemodificeerd en vervolgens worden vrijgegeven — ook over de dag heen in sterkte variëren. In plaats van een constante lopende band is deze route afgestemd op het tijdstip van de dag. De meeste ritmische bloedeiwitten droegen de moleculaire "signaalpeptiden" die hen voor deze route markeren, en het blokkeren van ER–Golgi transport in muizenleverplakjes verminderde de eiwitafgifte sterk. Markerenz van celschade en eiwitafbraak vertoonden daarentegen geen sterke dagelijkse veranderingen, wat aangeeft dat het juist secretie, niet afbraak, is die hoofdzakelijk de waargenomen bloedritmes drijft.
Glycogeen: opgeslagen suiker die eiwitverpakking voedt
De auteurs koppelden deze timingseffecten vervolgens aan hoe de lever met glycogeen omgaat, haar belangrijkste koolhydraatreserve. Na maaltijden bouwt de lever glycogeen op; tijdens vasten breekt zij glycogeen af, een proces dat glycogenolyse wordt genoemd. De afbraakproducten voeden de "UDP-suikers", de geactiveerde suikereenheden die worden gebruikt om eiwitten met suikerketens te versieren, een modificatie die glycosylering heet. Bij muizen schommelden de UDP-suikerniveaus sterk over de dag, in overeenstemming met de activiteit van enzymen die glycogeen opbouwen en afbreken. Toen het team het sleutelenzym van leverglycogenolyse PYGL met een medicijn blokkeerde, stapelde glycogeen zich op, daalde de bloedglucose tijdens vasten en viel de aanvoer van UDP-suikers terug. Dit leidde tot minder glycosylering van levereiwitten, tekenen van stress in het ER en verminderde secretie van meerdere belangrijke eiwitten in het bloed.
Stresssignalen en verbanden met ziekte
Het verstoren van glycogeenafbraak deed meer dan alleen de eiwitexport vertragen; het triggerde het kwaliteitscontrolesysteem van de cel. Levercellen behandeld met het PYGL-blokkerende middel activeerden de unfolded protein response, een verzameling ER-stressroutes die eiwitafbraak kunnen verhogen en selectief kunnen veranderen welke eiwitten worden uitgescheiden. Bij vette muizen, die van nature een veranderd glycogeenbeheer hebben, waren de normale dagelijkse schommelingen in glycogeen afgezwakt en nam het aantal ritmische bloedeiwitten af. Hetzelfde gold toen normale muizen een tijdgebonden voederregime ondergingen dat effectief de calorie-inname verminderde. Ten slotte liet een grote menselijke genetische studie zien dat mensen die varianten dragen in genen die verband houden met glycogeenopslagziekten of congenitale glycosyleringsstoornissen afwijkende niveaus van veel bloedeiwitten hebben, wat de link tussen glycogeenmetabolisme, eiwitglycosylering en secretie versterkt.
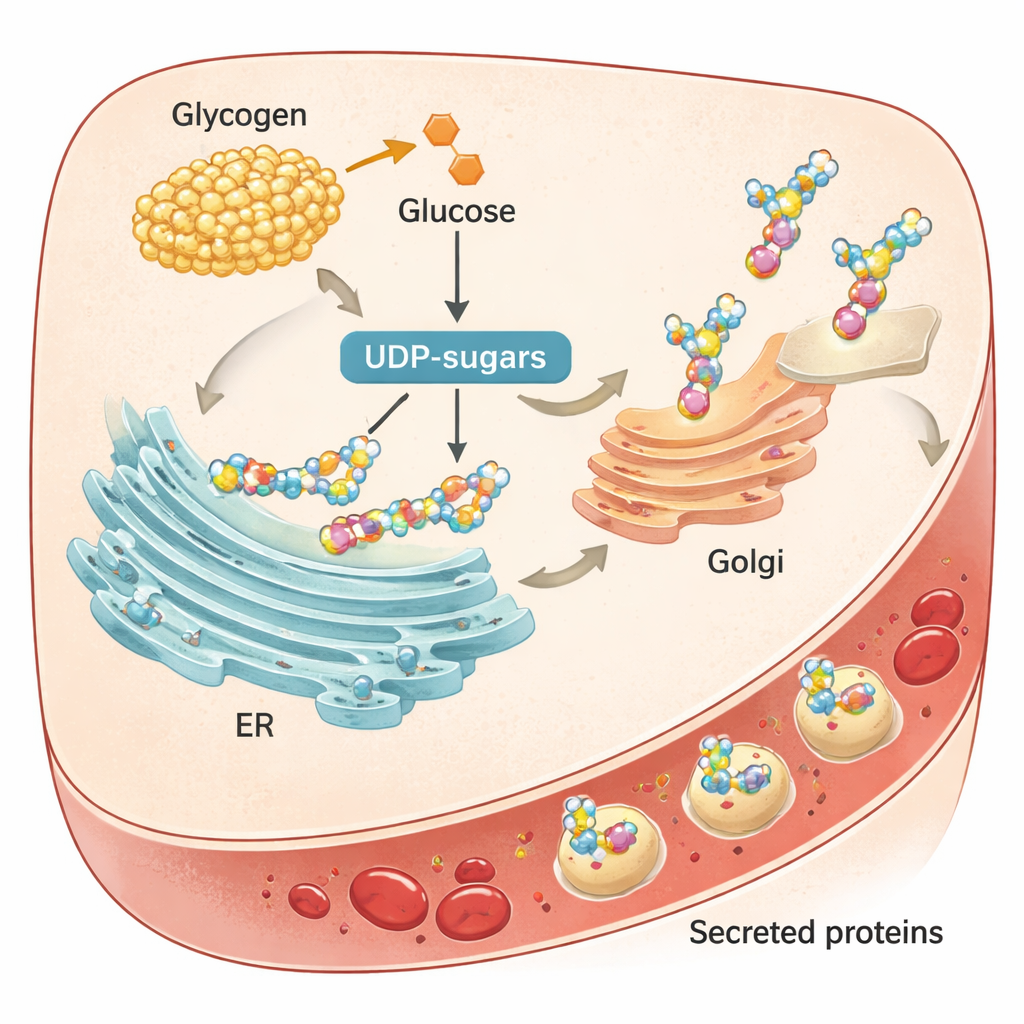
Wat dit betekent voor alledaagse gezondheid
Voor niet-specialisten is de boodschap dat de lever een getimede exportorganisatie runt voor bloedeiwitten, waarbij opgeslagen suiker het brandstof levert die zorgt voor correcte verpakking en vrijgave. Wanneer voedingspatronen, interne klokken of glycogeenverwerkende genen verstoord zijn, hapert dit schema en veranderen de niveaus van hormonen, stollingsfactoren en immuuneiwitten in de bloedbaan. Deze veranderingen kunnen helpen verklaren waarom maaltijdtiming, obesitas en bepaalde zeldzame metabole aandoeningen gekoppeld zijn aan verstrekkende gezondheidsproblemen. Het werk suggereert dat niet alleen wat we eten, maar ook wanneer we eten het dagelijkse verzendritme van de lever kan beïnvloeden — en dat artsen mogelijk rekening moeten houden met het tijdstip van de dag en eetpatronen bij het interpreteren van bloedtests.
Bronvermelding: Weger, M., Mauvoisin, D., Hoyle, D. et al. Feeding-regulated glycogen metabolism drives rhythmic liver protein secretion. Nat Metab 8, 327–349 (2026). https://doi.org/10.1038/s42255-026-01453-8
Trefwoorden: circadiaan ritme, leverglycogeen, eiwitsecretie, maaltijdtiming, metabolisme