Clear Sky Science · nl
Lamin A/C-gereguleerde cysteïne‑catabolische flux moduleert stamcelbestemming via epigenoom‑herprogrammering
Hoe het skelet van de cel met haar metabolisme praat
Waarom blijven sommige cellen jeugdig en flexibel in wat ze kunnen worden, terwijl andere verouderen of vastlopen in de verkeerde identiteit? Deze studie onthult een verrassend gesprek in onze cellen tussen het nucleaire “steigersysteem” dat het DNA vormt en een zwavelhoudend voedingsstof, cysteïne. Door te tonen hoe deze dialoog stamcellen richting gezonde bestemmingen — of naar voortijdige veroudering — stuurt, suggereert het werk dat wat cellen “eten” en hoe ze het verwerken mogelijk kan worden bijgesteld om bepaalde genetische ziekten te voorkomen en misschien zelfs aspecten van veroudering te vertragen.
De verborgen rol van de nucleaire schaal
Diep in elke cel ligt het DNA tegen een eiwitnetwerk aangedrukt dat de nucleaire lamina wordt genoemd, deels opgebouwd uit de eiwitten lamin A en C. Deze laminen geven de kern niet alleen zijn vorm; ze helpen ook bepalen welke genen verzegeld zijn en welke toegankelijk blijven. De auteurs bestudeerden muis-embryonale stamcellen in hun meest flexibele, ofwel “naieve”, staat en vonden dat lamin A/C normaal gesproken twee metabole enzymen, CBS en CTH, in toom houdt, die helpen bij de aanmaak en afbraak van cysteïne. Wanneer lamin A/C aanwezig en actief is, worden deze enzymen geremd en blijft de verwerking van cysteïne laag, wat een stabiele, jeugdige stamceltoestand ondersteunt. 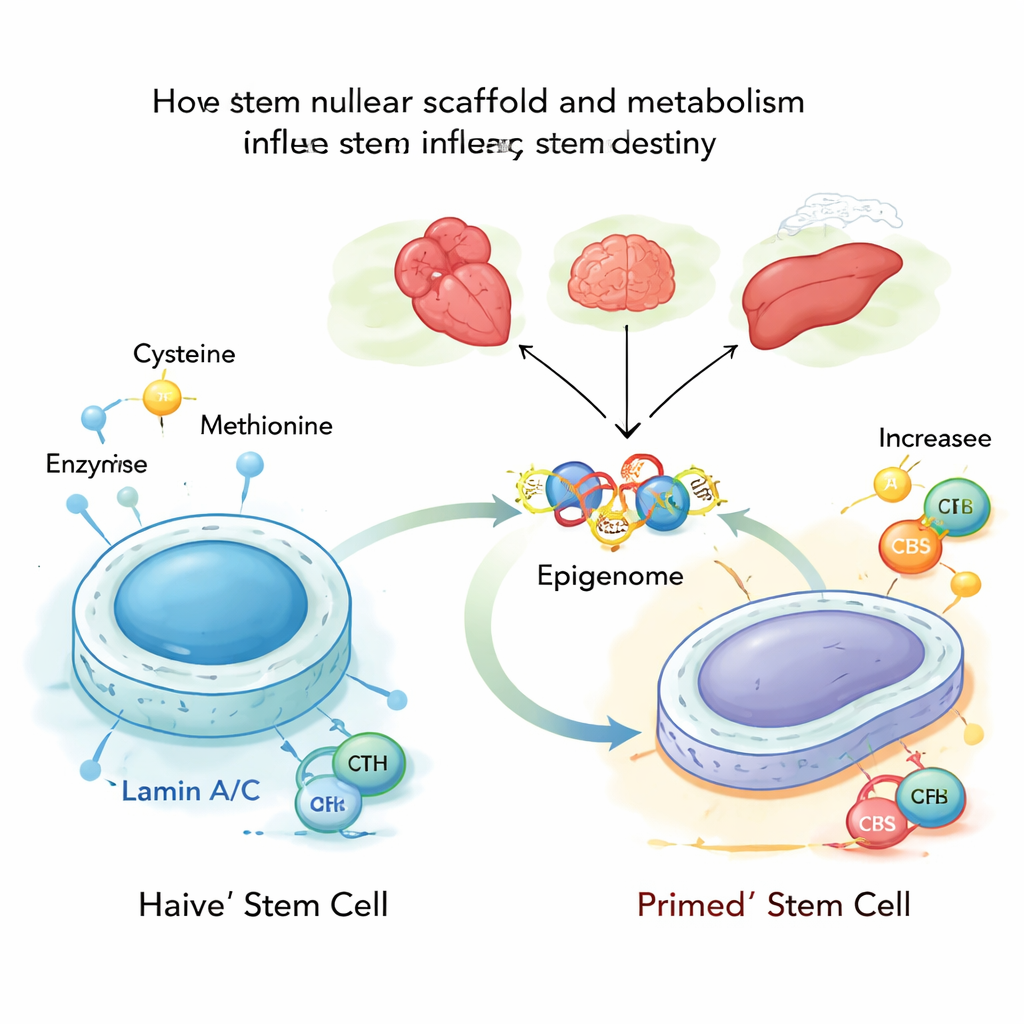
Als structuur faalt, versnelt het metabolisme
Vervolgens verwijderden de onderzoekers lamin A/C of introduceerden ze een ziekte‑gerelateerde mutatie die een menselijke voortijdige‑verouderingsziekte, Hutchinson–Gilford progeria, nabootst. Zonder normaal lamin A/C worden de genen voor CBS en CTH beter toegankelijk en sterker gebonden door een transcriptiefactor genaamd SP1, waardoor ze geactiveerd worden. Die verandering duwt meer cysteïne door een metabolische route die eindigt in acetyl‑CoA, een klein molecuul dat acetylgroepen transporteert die worden gebruikt om DNA‑verpakking losser te maken. Naarmate meer cysteïne wordt omgeleid naar acetyl‑CoA, worden de acetylgroepen bij voorkeur aan specifieke posities op histonen toegevoegd — vooral twee plaatsen op histon H3 bekend als K9 en K27 — waardoor nabijgelegen genen makkelijker aan te zetten zijn.
Van chemische tags naar celbestemmingsbeslissingen
Deze verschuivingen in histon‑“tags” werken als een wereldwijde herkalking van het regelpaneel van de cel. In naieve stamcellen duwt het verhogen van CBS en CTH, of simpelweg het aanleveren van meer cysteïne, cellen naar een meer gevorderde, “gepimeerde” staat die dichter bij het vormen van echte weefsels ligt. Genen die betrokken zijn bij hartontwikkeling en andere lijntjes worden actiever, en de driedimensionale vouwing van DNA verandert om deze programma’s te bevoordelen. Omgekeerd helpt het verminderen van CBS en CTH of het beperken van cysteïne om een meer naieve, jeugdige identiteit te herstellen, zelfs wanneer de nucleaire lamina beschadigd is. In embryonale modellen leidde deze metabole ontregeling tot een scheefvorming bij de vorming van de drie kiemlagen — de vroege bouwstenen van alle organen — en een abnormale voorkeur voor hartspiercellen, tenzij CBS en CTH werden hergebalanceerd. 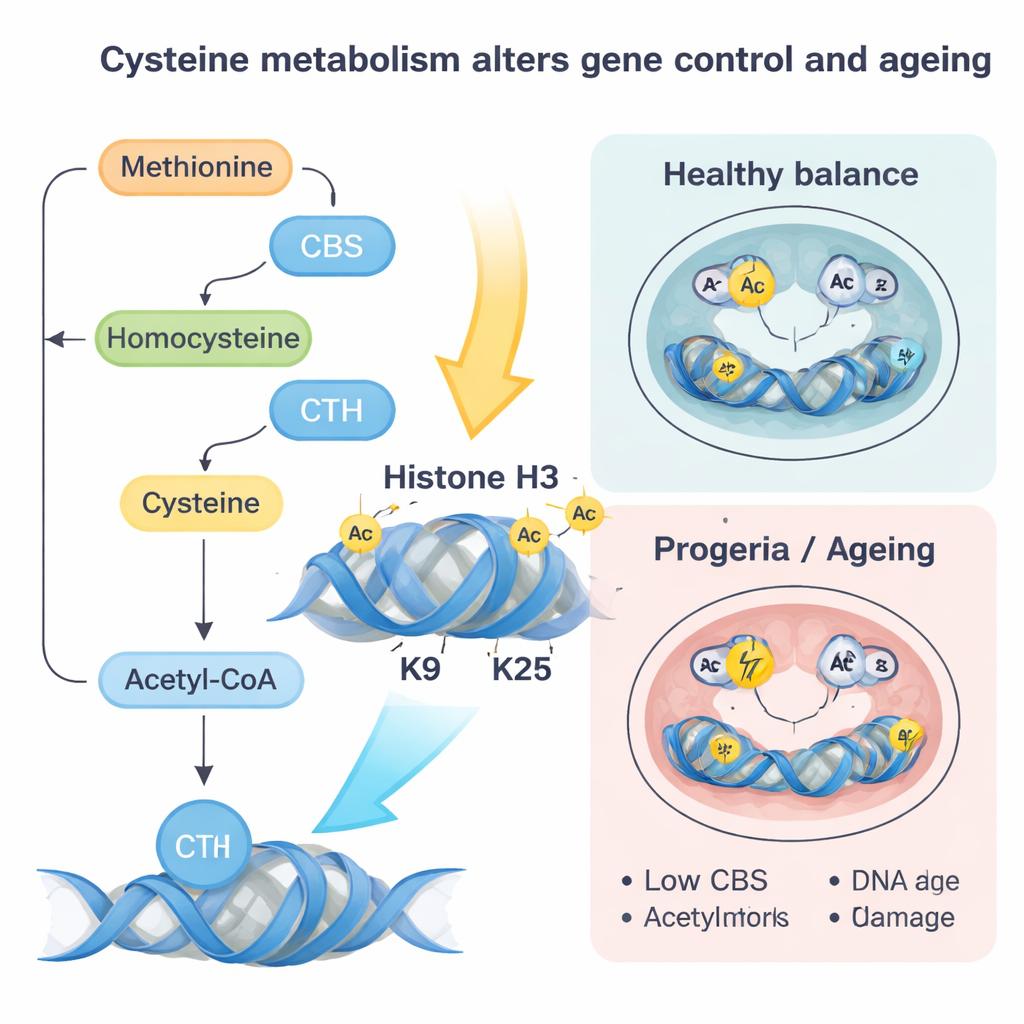
Metabolisme, DNAmethylatie en voortijdige veroudering
De progeria‑achtige laminmutatie vertelde een aanvullend verhaal. Hier dalen CBS‑ en CTH‑niveaus, waardoor de cysteïneflux en acetyl‑CoA via deze route afnemen. Tegelijkertijd wordt homocysteïne teruggeleid naar de methioninecyclus, wat de niveaus van SAM verhoogt, de universele donor van methylgroepen. Dat bevordert extra methyl‑tags, vooral een merkteken genaamd H3K9me3 geplaatst door het enzym SUV39H1, dat chromatine tighter maakt en geassocieerd is met verminderd DNA‑herstel. De auteurs toonden aan dat het voorzichtig herstellen van CBS of het beperken van methionine SAM verlaagde, deze repressieve methylmarks reduceerde, DNA‑herstel verbeterde, oxidatieve stress en senescentiemarkers verlaagde, en gedeeltelijk de differentiatie naar hartcellen redde. Vergelijkbare dalingen in CBS en stijgingen in repressieve marks werden gezien in normaal verouderde muizenharten en in menselijke fibroblasten van oudere mensen en progerie‑patiënten, wat suggereert dat deze schakeling ook tijdens natuurlijke veroudering werkt.
Wat dit betekent voor gezondheid en veroudering
Voor niet‑specialisten is de boodschap dat het structurele raamwerk van de cel en haar metabolisme nauw met elkaar verbonden zijn: wanneer de nucleaire schaal van lamin A/C verstoord raakt, verandert de wijze waarop cysteïne wordt gebruikt, wat op zijn beurt chemische markeringen op DNA‑verpakkende eiwitten herschrijft. Deze markeringen bepalen welke genen worden aangezet terwijl stamcellen het lichaam opbouwen en helpen mee te bepalen hoe goed cellen schade door het leven heen herstellen. Door enzymen zoals CBS en CTH zorgvuldig bij te stellen — of door de aanvoer van voedingsstoffen als methionine en cysteïne te reguleren — zou het mogelijk zijn enkele van de foute aantekeningen in deze marks bij lamin‑gebaseerde ziekten te corrigeren en wellicht aspecten van voortijdige of normale veroudering te milderen.
Bronvermelding: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Trefwoorden: stamcellen, nucleaire lamina, cysteïnemetabolisme, epigenetica, veroudering