Clear Sky Science · nl
ABEL-FRET overbrugt de tijdsschaalgap in enkel-molecuulmetingen van de structurele dynamiek van de A2A-adenosinereceptor
Kleine schakelaars op cellen in realtime volgen
Veel moderne geneesmiddelen werken door moleculaire "schakelaars" op celoppervlakken — receptoren — om te zetten. Deze schakelaars veranderen voortdurend van vorm terwijl ze signalen aan- en uitzetten, maar de meeste instrumenten zien alleen de allersnelste of juist de traagste bewegingen, niet beide. Dit artikel introduceert een manier om één individuele, medicijndoelreceptor in oplossing veel langer te volgen dan voorheen, waardoor duidelijk wordt hoe zij in bepaalde vormen blijft hangen die cruciaal zijn voor medicijnwerking.
Waarom deze vormveranderende eiwitten ertoe doen
De studie richt zich op een grote klasse van celoppervlakte-eiwitten die bekendstaan als G-eiwitgekoppelde receptoren, ofwel GPCR's. Deze eiwitten regelen vitale processen zoals zicht, stemming, bloeddruk en immuunreacties, en meer dan een derde van de goedgekeurde geneesmiddelen werkt via deze receptoren. Een goed bestudeerd lid, de A2A-adenosinereceptor, helpt bij het reguleren van slaap, pijn, ontsteking en hersensignaalgeving, en is een veelbelovend doelwit voor aandoeningen zoals de ziekte van Parkinson en kanker. GPCR's zijn zeer flexibel: wanneer verschillende moleculen binden, duwen ze de receptor in uiteenlopende vormen die bepaalde signaalroutes bevoordelen. Diezelfde flexibiliteit bemoeilijkt echter het ontwerpen van middelen op basis van statische snapshots uit röntgendiffractie of cryo-elektronenmicroscopie.
Een enkele receptor volgen zonder die vast te zetten
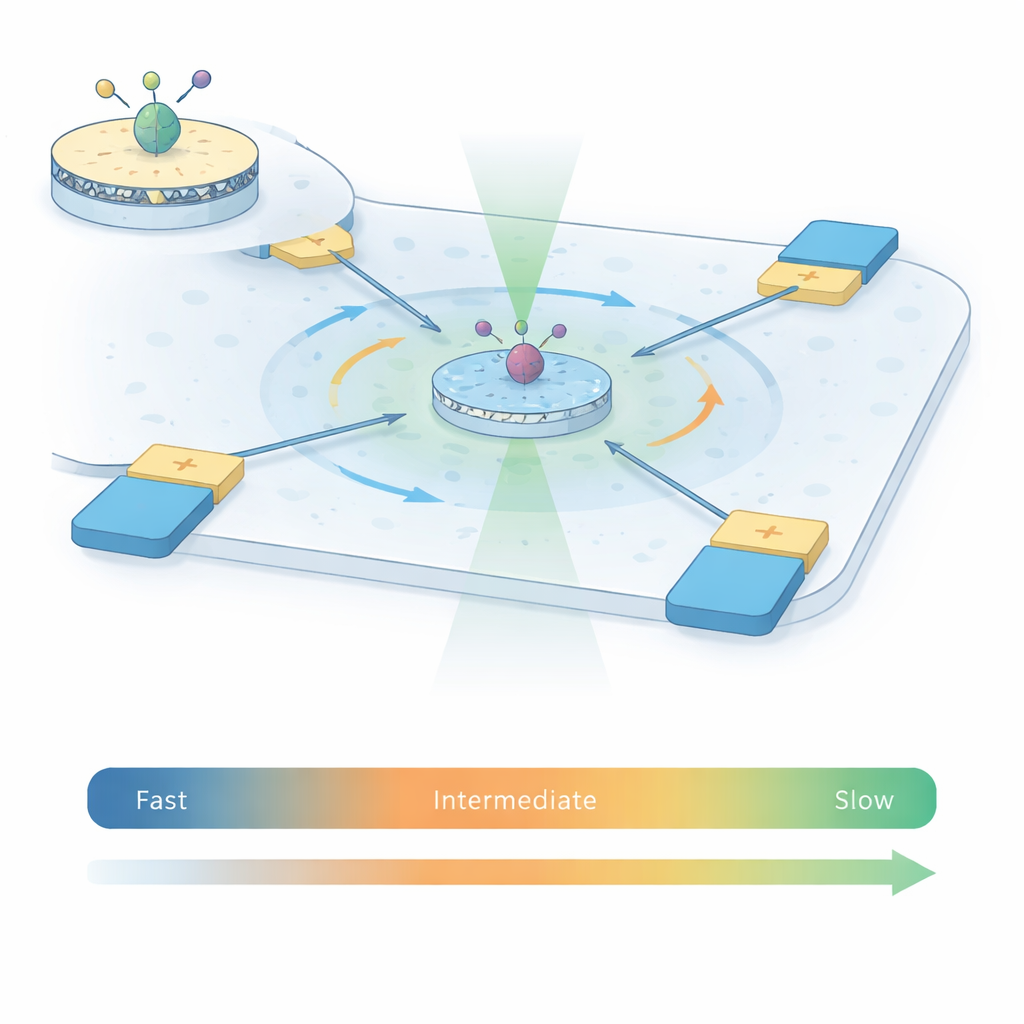
Om de bewegingen van A2A-receptoren vast te leggen combineren de auteurs twee krachtige technieken tot wat zij ABEL‑FRET noemen. Ten eerste brengen ze afzonderlijke receptoren terug in kleine stukken kunstmatig membraan, nanodiscs geheten, waardoor elk eiwit een natuurlijker omgeving krijgt dan in alleen detergent. Ze koppelen een paar fluorescente kleurstoffen aan twee bewegende delen aan de binnenzijde van de receptor. Als de receptor van vorm verandert, veranderen ook de afstand en relatieve oriëntatie tussen deze kleurstoffen, wat de energieoverdracht tussen hen beïnvloedt — een verschijnsel dat bekendstaat als Förster-resonantie-energietransfer (FRET). Ten tweede, in plaats van de receptor op een oppervlak vast te zetten, gebruiken ze een Anti-Browniaanse Elektrokinetische (ABEL) val: een microfluïdisch kamertje met elektroden die voelen waar een fluorescent deeltje zich bevindt en het zachtjes terug naar het midden duwen om willekeurige Brownse beweging tegen te werken.
Het ontbrekende tijdvenster overbruggen
Traditionele enkel-molecuul FRET-experimenten kijken ofwel naar vrij diffunderende receptoren gedurende slechts enkele duizendsten van een seconde, of naar geïmmobiliseerde receptoren op een oppervlak gedurende seconden tot minuten. Elke benadering dekt een ander tijdvenster. Met de ABEL-val houdt dit werk individuele A2A-receptoren gedurende één tot twee seconden in beeld terwijl ze vrij in oplossing blijven, ongeveer 100 keer langer dan bij diffusie-beperkte experimenten. Deze verlengde kijktijd stelt het team in staat te meten hoe het FRET-signaal fluctueert binnen elk gevangen burst en over duizenden receptoren, onder vier condities: zonder ligand, met een antagonist en met twee verschillende activerende moleculen (agonisten). Statistische hulpmiddelen uit de signaalanalyse — variantie-, correlatie- en recidiefanalyse — helpen om willekeurige fotonruis te onderscheiden van echte, trage structurele veranderingen in de receptor.
Verborgen, langlevende vormen blootgelegd
De FRET-signalen tonen aan dat receptoren meerdere duidelijke conformaties bezetten die tijdens typische observatietijden van enkele honderden milliseconden niet volledig in elkaar overgaan. In alle condities is de spreiding van FRET-waarden veel groter dan verwacht op basis van ruis alleen, wat structurele heterogeniteit onthult: verschillende moleculen bevinden zich in verschillende langlevende vormen. Wanneer activerende moleculen binden, verschuift het gemiddelde FRET-niveau omhoog, wat aangeeft dat de receptor meer tijd doorbrengt in een "actief-achtige" rangschikking van zijn binnenste helixen. Toch laten de correlatieanalyses zien dat zodra een receptor zich in een hoge of intermediaire FRET-toestand bevindt, de kans groot is dat hij daar minstens honderden milliseconden blijft. Deze resultaten actualiseren eerdere schattingen gebaseerd op snellere experimenten en verlengen de karakteristieke "verblijftijden" in langlevende toestanden van slechts milliseconden tot ruim meer dan een tiende van een seconde.
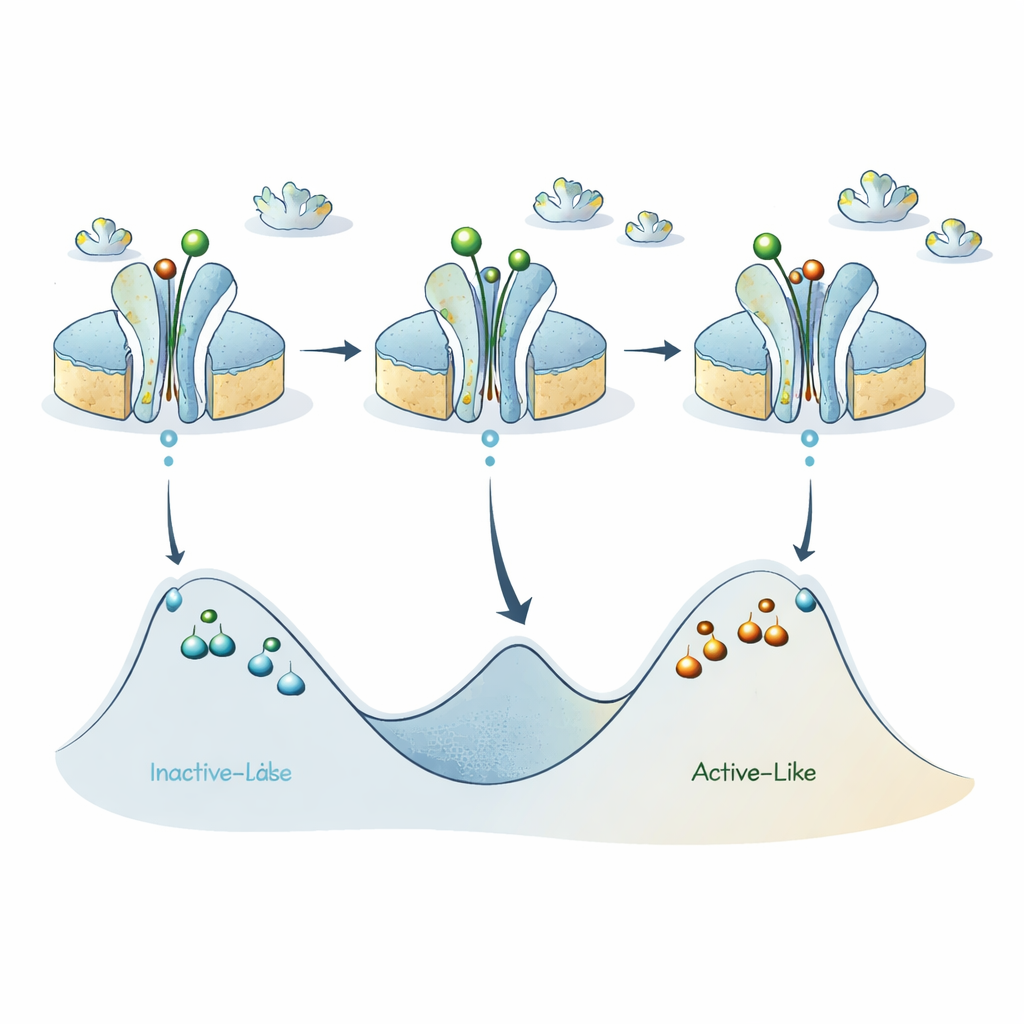
Een nieuwe kaart van het energielandschap van de receptor
Als deze onderdelen worden samengevoegd, verfijnen de auteurs een eerder model waarin de A2A-receptor voornamelijk wisselt tussen een inactief-achtige en een actief-achtige toestand. Hun nieuwe gegevens suggereren dat elk van deze twee brede categorieën eigenlijk meerdere subtoestanden verbergt die worden gescheiden door aanzienlijke energiedrempels, waardoor individuele receptoren lange tijd in een bepaalde versie van actief-achtige of inactief-achtige toestand kunnen blijven "vastzitten". Activerende liganden verlagen de barrière tussen de belangrijkste inactieve- en actieve-achtige basins, wat snelle wisseling op submilliseconde-schaal bevordert, maar de interne barrières binnen elk basin blijven hoog, wat leidt tot de langlevende substaten die ABEL‑FRET detecteert.
Wat dit betekent voor toekomstige geneesmiddelen
Voor niet‑specialisten is de kernboodschap dat een medicijndoel zoals de A2A-receptor niet simpelweg tussen "uit" en "aan" schakelt. In plaats daarvan verkent het een ruw terrein van vormen, waarvan sommige lang genoeg voortduren om van belang te zijn voor hoe signalen in cellen worden doorgegeven en hoe geneesmiddelen in de tijd werken. Door te verlengen hoe lang individuele receptoren in hun natuurlijke, niet-gebonden staat kunnen worden bekeken, vult ABEL‑FRET een cruciale leemte tussen ultrakorte en zeer trage metingen. Deze aanpak kan nu op veel membraaneiwitten worden toegepast en biedt een completer, tijdsopgelost beeld van hoe potentiële medicijndoelen ademen, verschuiven en reageren op therapeutische verbindingen.
Bronvermelding: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Trefwoorden: G-eiwitgekoppelde receptoren, enkel-molecuul FRET, adenosine A2A-receptor, eiwitconformationele dynamiek, ABEL-val