Clear Sky Science · nl
Mechanistische studie naar sulfaatmigratie in glycosaminoglycanen tijdens MS-fragmentatie
Waarom het verschuiven van chemische labels op suikers ertoe doet
Onze cellen zijn bedekt met lange suikerketens die processen regelen variërend van bloedstolling en immuunverdediging tot hoe virussen zich aan cellen hechten. Veel van deze ketens dragen kleine chemische labels, sulfaatgroepen, waarvan de precieze positie langs de suikerruggengraat als een moleculaire streepjescode fungeert en eiwitten vertelt waar ze moeten binden. Wetenschappers vertrouwen sterk op massaspectrometrie, een krachtige weegtechniek, om deze streepjescodes uit te lezen. Deze studie toont aan dat sulfaatlabels tijdens zulke metingen ongemerkt van positie kunnen veranderen, waardoor onderzoekers mogelijk worden misleid over de echte opbouw van deze biologisch essentiële suikers.
Complexe suikerketens met cruciale labels
Glycosaminoglycanen zijn lange, lineaire suikerketens die vaak aan eiwitten op celoppervlakken zitten. Hun sulfaatversiering is niet willekeurig; kleine veranderingen in de plaats van een sulfaatgroep op een suikerunit kunnen drastisch veranderen hoe de keten met groeifactoren, stollingseiwitten of pathogenen interageert. Daarom proberen onderzoekers niet alleen te bepalen hoeveel sulfaten aanwezig zijn, maar ook precies waar ze zitten. Massaspectrometrie, vaak gecombineerd met gecontroleerde fragmentatie van de suikerketens, is een van de belangrijkste methoden hiervoor. Vorige aanwijzingen suggereerden echter dat geladen groepen zoals sulfaten tijdens de meting kunnen verplaatsen, wat het uitlezen van het echte modificatiepatroon bemoeilijkt.
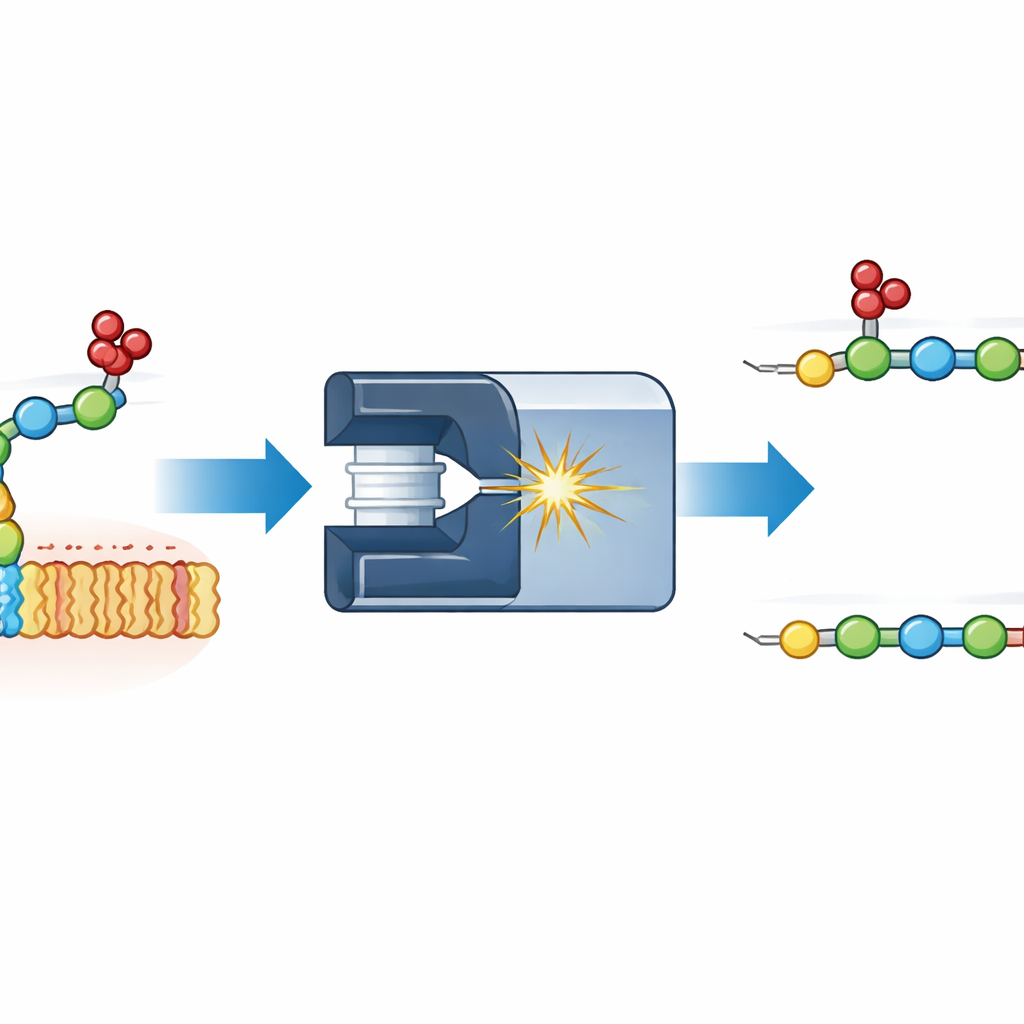
Het volgen van sulfaatverplaatsing tijdens de meting
De auteurs concentreerden zich op een eenvoudig model: een tweesuikerfragment van heparan sulfaat, een van de best bestudeerde glycosaminoglycanen. Ze plaatsten verschillende fluorescente labels aan één uiteinde van het disaccharide en fragmenteerden het in een massaspectrometer. Door te meten hoe de resulterende delen door een gas onder een elektrisch veld daveren — een techniek genaamd ionenmobiliteit — konden ze vormen onderscheiden die anders dezelfde massa hebben. Een onverwacht fragment verscheen dat precies één extra sulfaatgroep droeg op de verkeerde plaats: in plaats van op de eerste suiker te blijven, was het sulfaat naar de tweede gemigreerd. Vergelijking met zorgvuldig gesynthetiseerde referentieverbindingen toonde aan dat het gemigreerde sulfaat op twee verschillende plekken van de tweede suiker terecht kon komen, wat twee verschillende vormen gaf die met ionenmobiliteit duidelijk te scheiden waren.
Het vaststellen van nieuwe landingsplaatsen en het testen van labels
Om beter te begrijpen waar het sulfaat terechtkwam en of andere posities mogelijk waren, combineerde het team hun metingen met gedetailleerde computersimulaties. Ze berekenden vele mogelijke driedimensionale vormen voor de kandidaatstructuren en voorspelden hoe elk zich door de gasfase zou verplaatsen. Alleen sulfaten op twee specifieke plaatsen van de tweede suiker — bij specialisten bekend als de 6O- en 3O-posities — kwamen overeen met het experimentele gedrag, terwijl andere hypothetische locaties onwaarschijnlijk leken. De onderzoekers testten vervolgens of de aangebrachte labels zelf de herschikking konden aansturen door het oorspronkelijke label te vervangen door drie eenvoudigere. In alle gevallen bleef sulfaatmigratie optreden en leverde vergelijkbare fragmenten op, wat aangeeft dat de keuze van het label weinig invloed heeft op of migratie plaatsvindt, hoewel het subtiel kan beïnvloeden hoe goed de verschillende producten van elkaar te onderscheiden zijn.
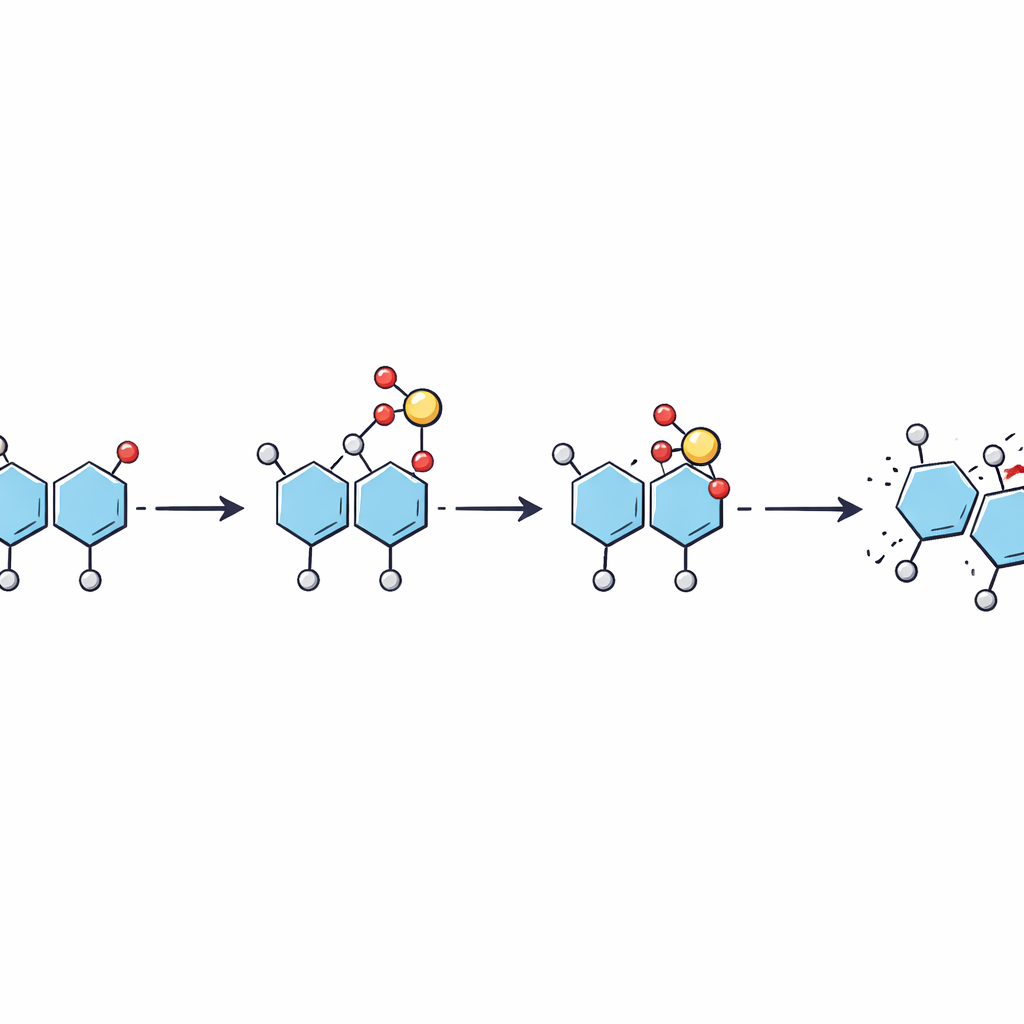
Stapsgewijs hoppen in plaats van één sprong
Met energie-afgestelde fragmentatie-experimenten en verdere simulaties stelden de auteurs een stapsgewijs beeld samen van hoe het sulfaat zich verplaatst. Terwijl het ion in de massaspectrometer geactiveerd wordt, activeert een mobiele proton eerst de sulfaatgroep, die vervolgens van de oorspronkelijke suiker naar een specifieke plaats op de aangrenzende suiker springt terwijl de binding tussen hen breekt. Dit levert een fragment op waarin het sulfaat in een tussenpositie zit. Met extra energie kan het sulfaat opnieuw verschuiven langs dezelfde suiker naar een stabielere plek. Het werk suggereert dat deze herschikkingen kunnen optreden bij lagere energieën dan nodig zijn om de suikerruggengraat te breken, wat betekent dat ze stilletjes kunnen gebeuren tijdens routinematige analyses.
Wat dit betekent voor het ontcijferen van suikerstructuren
Voor niet-specialisten is de kernboodschap dat de chemische labels op belangrijke biologische suikers niet altijd vastzitten tijdens analyse; ze kunnen langs de keten schuiven terwijl het molecuul door de massaspectrometer vliegt. De studie toont gedetailleerd aan dat, althans voor een representatief heparan sulfaatfragment, een sulfaatgroep van de ene suikerunit naar een andere kan migreren en zich vervolgens op nieuwe posities kan vestigen, waardoor misleidende fragmenten ontstaan die echte structurele kenmerken nabootsen. Dit betekent dat sommige eerdere en toekomstige metingen de sulfaatcode verkeerd kunnen lezen tenzij aanvullende technieken, zoals ionenmobiliteit en geavanceerde modellering, worden gebruikt om deze verborgen verschuivingen te detecteren. Het werk pleit voor meer systematische onderzoeken om te bepalen hoe wijdverbreid dergelijke sulfaatmigratie is, zodat onderzoekers suikerpatronen op celoppervlakken betrouwbaarder aan gezondheid en ziekte kunnen koppelen.
Bronvermelding: Polewski, L., Yaman, M., Tokić, M. et al. Mechanistic study on the sulfate migration in glycosaminoglycans during MS fragmentation. Commun Chem 9, 130 (2026). https://doi.org/10.1038/s42004-026-01939-2
Trefwoorden: heparan sulfaat, glycosaminoglycanen, massaspectrometrie, sulfaatmigratie, ionenmobiliteit