Clear Sky Science · nl
De diepte van de bindingshouding beïnvloedt de werkzaamheid van fotoschakelbare liganden op de 5-HT2A-receptor
Licht werpen op schakelbare hersenmedicijnen
Stel je een medicijn voor dat je met een lichtflits aan en uit kunt zetten, waarmee je nauwkeurig hersenreceptoren stuurt en bijwerkingen kunt vermijden. Deze studie onderzoekt precies dat idee voor een belangrijke serotoninereceptor die samenhangt met stemming, waarneming en psychedelische middelen. De onderzoekers doken in de vraag waarom twee bijna identieke lichtgevoelige moleculen zich zo verschillend gedragen—de één bijna als een perfecte aan/uit-schakelaar, de ander die koppig weigert volledig uit te gaan. Hun antwoord komt neer op een verrassend eenvoudige factor: hoe diep het molecuul in de receptor zit.
Lichtgestuurde geneesmiddelen in de hersenen
Licht-geactiveerde geneesmiddelen, ook wel fotofarmacologische middelen genoemd, zijn zo ontworpen dat een lichtstraal een deel van het molecuul tussen twee vormen omzet—zoals een gebogen en een rechte versie. Die vormen kunnen veranderen hoe sterk het middel zijn doel vasthoudt. In dit werk is het doel de menselijke 5-HT2A-receptor, een eiwit op hersencellen dat reageert op serotonine en centraal staat in zowel antipsychotische als psychedelische effecten. De bestudeerde moleculen zijn afgeleiden van N,N-dimethyltryptamine (DMT), gemodificeerd met een lichtgevoelige azobenzeen-eenheid. Twee versies verschillen alleen in waar een klein methoxygroepje op een ring geplaatst is—ofwel in een “para”- of in een “meta”-positie—maar hun biologische gedrag onder licht verschilt dramatisch.
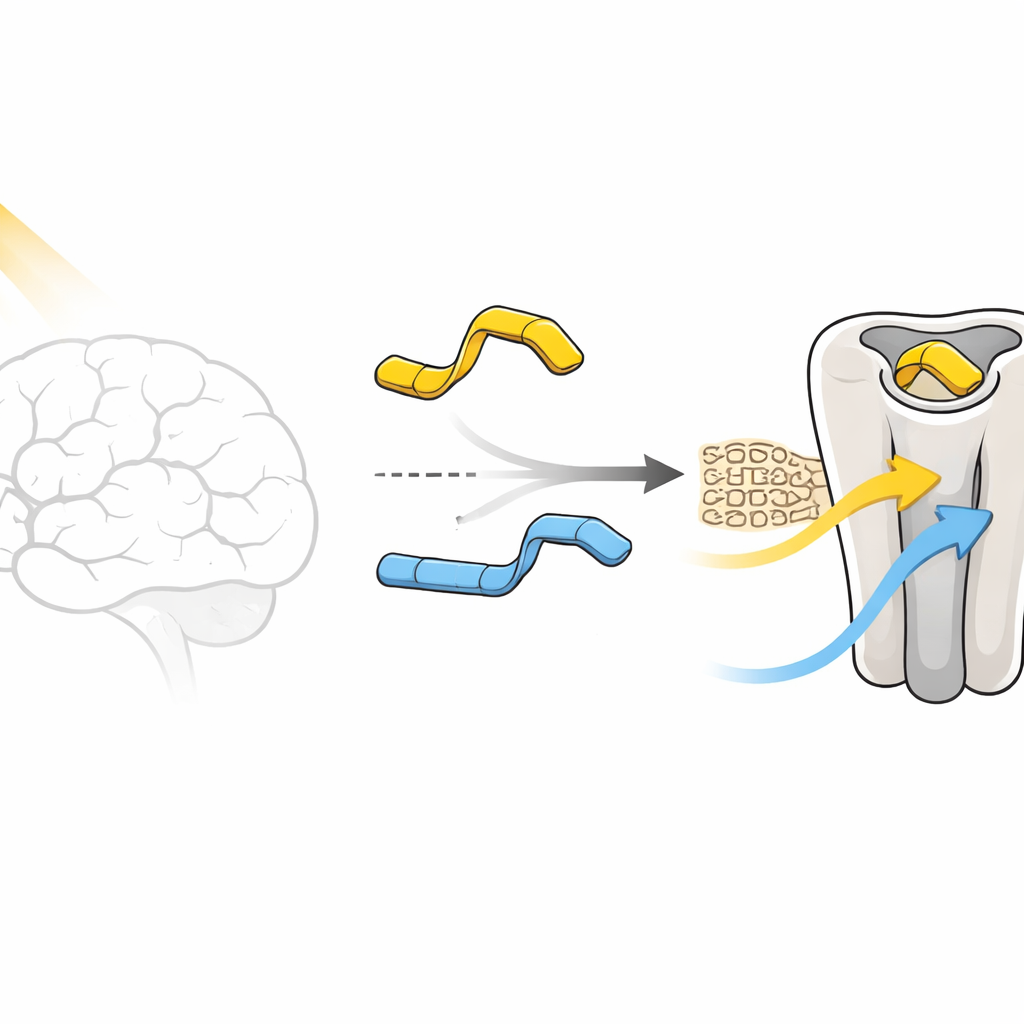
Twee bijna identieke moleculen, heel verschillende schakelaars
In celtesten gedraagt de para-versie, genoemd verbinding 1, zich bijna als een digitale schakelaar. In het donker activeert de “trans”-vorm de receptor nauwelijks en blokkeert deze zelfs licht, werkend als een zwakke antagonist. Wanneer licht het in de “cis”-vorm omkeert, wordt hetzelfde molecuul een matige activator, die de receptor gedeeltelijk aanzet. De meta-versie, verbinding 2, werkt niet op die manier mee: zowel de licht- als de donkervorm houden de receptor tamelijk actief en leveren nooit een echte “uit”-toestand. Het centrale raadsel van dit artikel is waarom zo’n minimale chemische wijziging—slechts het verplaatsen van een klein groepje op een ring—zo sterk verandert hoe de receptor reageert.
Inzoomen met atoomniveaufilms
Om dit op te lossen gebruikte het team uitgebreide all-atom moleculaire dynamica-simulaties, feitelijk gedetailleerde films van elk atoom in de receptor, het omringende membraan, water en elke ligand over in totaal ongeveer 80 microseconden. Ze simuleerden beide moleculen in elk van hun lichtgestuurde vormen, en in zowel inactieve als actieve vormen van de 5-HT2A-receptor. Door bekende structurele “microschakelaars” binnen het eiwit te volgen—zoals een sleutel-tryptofaan dat kantelt, een zoutbrug die breekt, en de beweging van natrium en water diep in de kern—konden ze aflezen wanneer de receptor neigde naar een uit- of aan-toestand. Ze vergeleken ook hoe nauw de nieuwe moleculen de bindingshouding van LSD nabootsten, een goed bestudeerde partiële activator, door de overlap van hun ringsystemen te gebruiken als leidraad.
Diepte telt meer dan vorm alleen
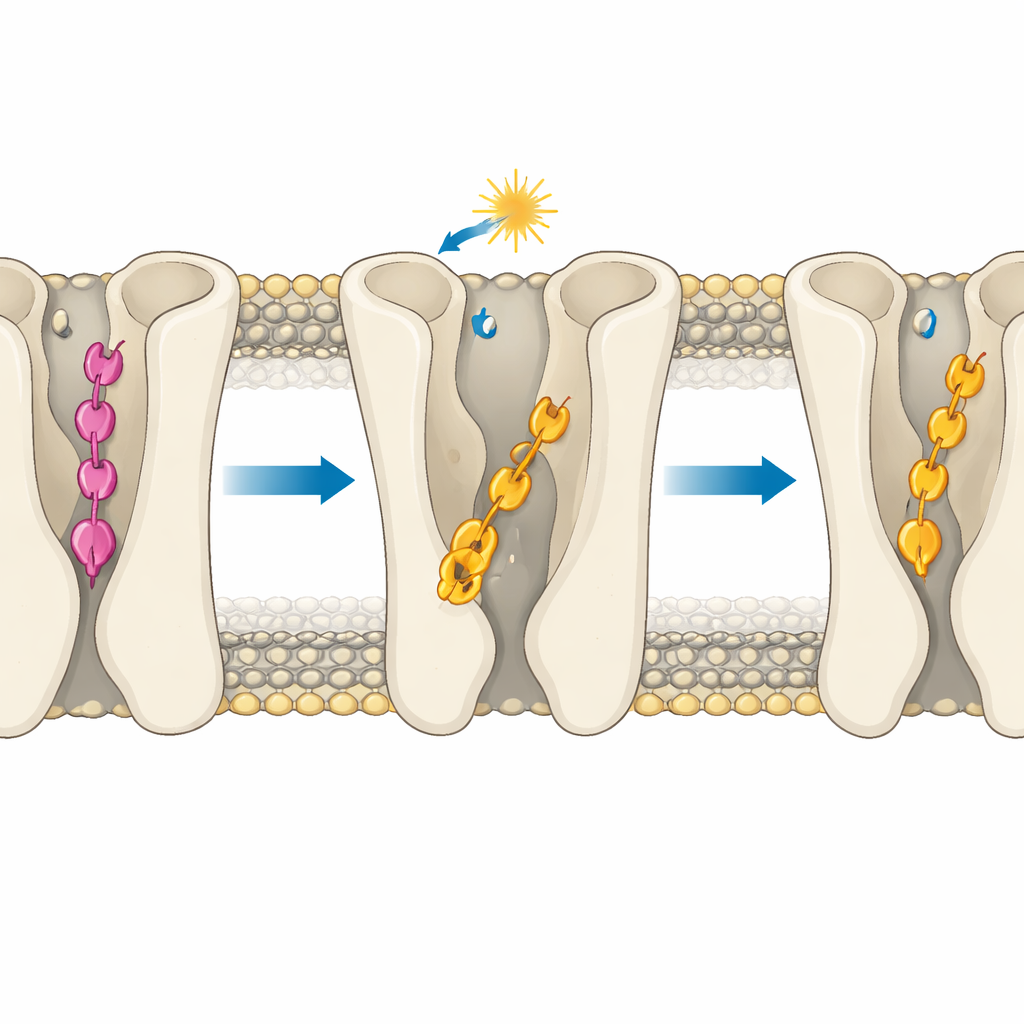
De kerninzich is dat de effectiviteit van de moleculen vooral wordt bepaald door hoe diep ze in het bindingszakje van de receptor binnendringen. In de inactieve receptor vormt de trans-vorm van de para-verbinding een speciale set waterstofbruggen die hem uitzonderlijk diep trekt, onder het gebied waar typische activerende contacten plaatsvinden. Deze “over-insertie” voorkomt dat het contact maakt met sleutelpolare residuen die helpen de receptor aan te zetten, zodat het de uit-toestand stabiliseert. De trans-vorm van de meta-verbinding kan niet dezelfde verankerende contacten maken en zit in plaats daarvan hoger in een meer LSD-achtige houding die compatibel is met activatie, wat zijn resterende activiteit verklaart. Wanneer licht beide moleculen in hun cis-vormen zet, verplaatsen ze zich over het algemeen naar ondiepere, meer activatorachtige posities. Toch blijft geometrie belangrijk: in de actieve receptor kan cis-verbinding 2 dieper glijden in een hydrofoob kanaal tussen twee helices en een blijvende waterstofbrug vormen die zijn sterke agonistische gedrag versterkt, terwijl cis-verbinding 1 hier sterisch van wordt weerhouden.
Fijne regeling van intern water en ionen
De simulaties laten ook zien dat bindingsdiepte subtiel een intern natriumpocket en waterpad afstemt die bekendstaan als beïnvloeders van receptoractivatie. Diepe, rigide binding door de para-verbinding in zijn trans-vorm houdt een natriumion strak ingesloten en maakt de omliggende regio relatief droog—kenmerken die samenhangen met een uit-toestand. Daarentegen laat de meer beweeglijke binding van de meta-verbinding of de cis-vormen meer water binnendringen en versoepelt de natriumomgeving, waardoor de receptor klaarstaat voor activatie. Een belangrijk aromatisch “toggle switch”-residu kan van oriëntatie wisselen wanneer liganden flexibel zijn en niet te sterk verankerd, wat de receptor verder naar een aan-achtige toestand duwt, vooral bij cis-verbinding 2.
Ontwerprichtlijnen voor toekomstige lichtgereguleerde middelen
Voor een niet‑specialist is de boodschap dat de precieze diepte waarop een geneesmiddel in zijn receptorzakje zit het verschil kan maken tussen uit, deels aan en sterk aan—zelfs wanneer de chemische verandering op papier klein lijkt. Door te laten zien hoe één fotoschakelbare ligand te diep kan inschuiven en de receptor kan vergrendelen in een uit-toestand, terwijl een nauw verwante ligand op een activatie‑vriendelijke diepte blijft, biedt de studie een duidelijke ontwerprichtlijn: beheers de inschijdiepte net zo zorgvuldig als je de licht geïnduceerde vormveranderingen beheerst. Deze inzichten kunnen de ontwikkeling sturen van volgende generaties lichtgevoelige verbindingen die hersenaandoeningen met ongekende precisie behandelen, signaleringspaden gecontroleerd en omkeerbaar op- of afschakelen en tegelijkertijd bijwerkingen minimaliseren.
Bronvermelding: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
Trefwoorden: fotofarmacologie, serotonine 5-HT2A-receptor, fotoschakelbare liganden, GPCR-activatie, moleculaire dynamica-simulaties