Clear Sky Science · nl
Scaffold-klantgedrag en structurele organisatie in multicomponent proteïnecondensaten onthuld door het bestuderen van tau/TDP-43 druppels
Proteïnen die zich gedragen als kleine oliedruppels
Binnen onze cellen blijven veel eiwitten niet gelijkmatig opgelost in de waterige binnenzijde. In plaats daarvan verzamelen ze zich in kleine vloeibare druppels, een beetje zoals olie in water. Deze studie onderzoekt hoe twee zulke eiwitten, tau en TDP-43, die nauw verbonden zijn met de ziekte van Alzheimer en andere vormen van dementie, samen druppels vormen. Door te achterhalen hoe deze druppels ontstaan, mengen en zich organiseren, biedt het werk aanwijzingen waarom schadelijke eiwit-aggregaten in verouderende hersenen verschijnen en hoe we die mogelijk ooit kunnen beheersen.
Waarom deze twee hersenproteïnen ertoe doen
Tau en TDP-43 staan beide bekend om het vormen van toxische aggregaten bij neurodegeneratieve ziekten. Traditioneel bestudeerden wetenschappers ze afzonderlijk, maar autopsies van menselijke hersenen tonen steeds vaker aan dat beide eiwitten in dezelfde beschadigde regio’s kunnen samenkomen. Dat werpt een cruciale vraag op: wanneer tau en TDP-43 tegelijk in cellen aanwezig zijn, hoe delen ze dan ruimte binnen druppels, en bevordert die gedeelde omgeving ziektegerelateerde aggregatie? De auteurs kozen voor een vereenvoudigd maar realistisch model met tau en de low-complexity staart van TDP-43 (het LCD), dat deel dat vooral verantwoordelijk is voor druppelvorming en uiteindelijke verharding.
Druppels, “scaffolds” en “clients”
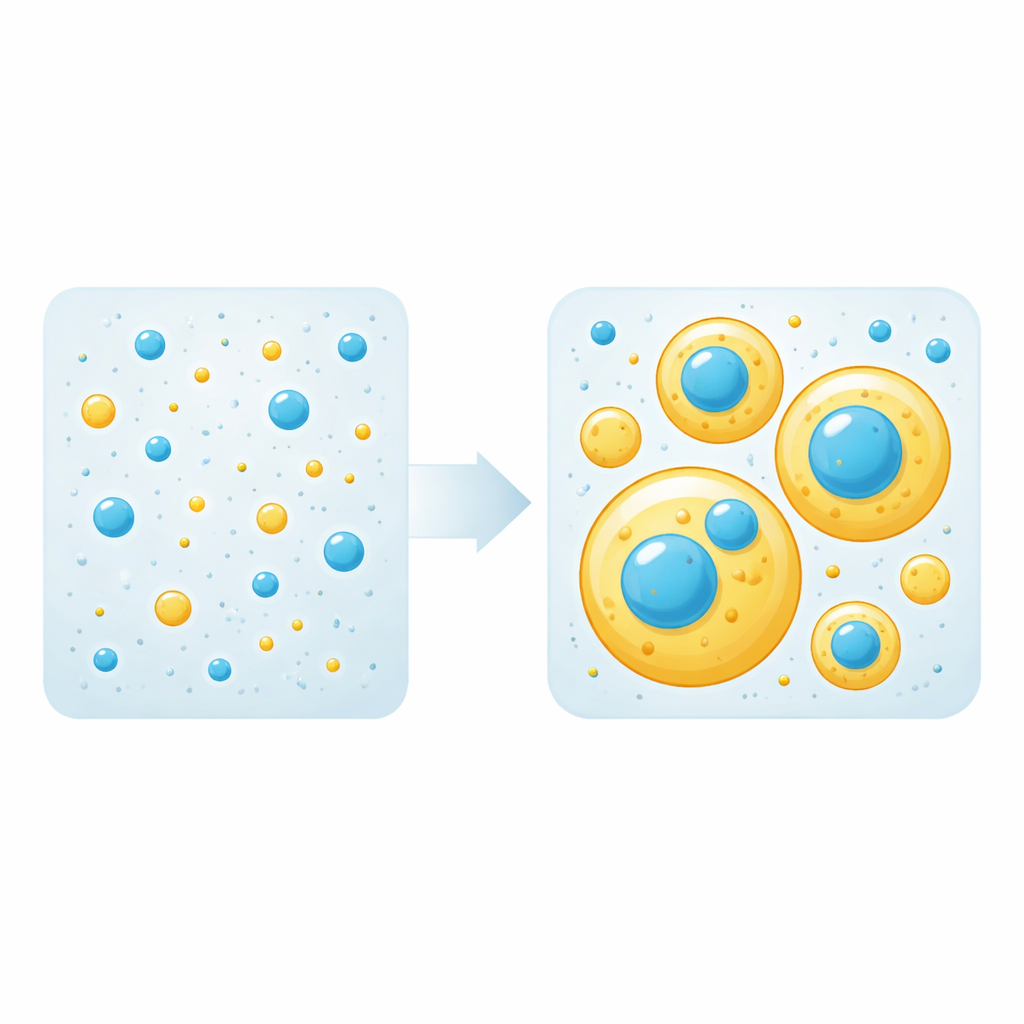
Dergelijke vloeibare druppels ontstaan wanneer eiwit–eiwit aantrekkingskrachten sterker zijn dan eiwit–water aantrekkingskrachten, waardoor een oplossing splitst in een dichte fase (druppels) en een verdunde fase. In mengsels zijn slechts sommige eiwitten nodig om druppels te bouwen; deze noemen we “scaffolds”. Andere worden simpelweg meegevoerd in druppels als “clients”. Het team mat eerst de concentratiedrempel waarbij elk eiwit alleen begint druppels te vormen. Vervolgens mengden ze verschillende hoeveelheden tau en TDP-43 LCD en observeerden met fluorescentiemicroscopie of er druppels verschenen en hoe de eiwitten zich rangschikten. Opmerkelijk genoeg bleek dat elk eiwit zowel de rol van scaffold als van client kan vervullen afhankelijk van alleen zijn concentratie: boven de eigen drempel bouwt het druppels, daaronder wordt het passief gerekruteerd in druppels gevormd door het andere eiwit.
Gelaagde druppels en een mysterieuze halo
Wanneer beide eiwitten voldoende overvloedig waren om op zichzelf druppels te vormen, mengden ze zich niet tot één uniforme druppel. In plaats daarvan omsloten grotere tau-rijke druppels kleinere TDP-43–rijke druppels, waardoor een gelaagde, meerfase-structuur ontstond. Metingen van hoe de druppels uitspreiden op glas toonden dat TDP-43 druppels een hogere oppervlaktespanning hebben, zodat het energetisch gunstig is dat ze binnen de meer natte tau-druppels zitten. Een opvallend kenmerk verscheen op deze interfaces: tau stapelde zich in bijzonder hoge concentraties op als een heldere “halo” die het oppervlak van TDP-43 druppels bekleedde, zelfs wanneer tau zelf onder zijn eigen druppelvormende drempel zat. In de loop van de tijd neigden TDP-43–rijke regio’s te verharden tot een meer vaste stofachtige toestand, terwijl tau-rijke regio’s vloeibaar bleven, wat wijst op verschillende neigingen om in langdurige aggregaten te veranderen.
Het afstemmen van interacties en het onderzoeken van het microscopische mechanisme
De auteurs onderzochten vervolgens hoe specifieke moleculaire krachten bepalen welk eiwit als scaffold of client fungeert. Ze verzwakten selectief hydrofobe (waterafstotende) interacties die condensatie van TDP-43 LCD aansturen met 1,6-hexanediol, en verzwakten apart de elektrostatistische (ladinggebaseerde) interacties die tau-condensatie aandrijven door het zoutgehalte te verhogen. In beide gevallen voorkwam het uitschakelen van de sleutelinteracties van één eiwit dat het zelf druppels vormde en veranderde het in een client binnen druppels van het andere eiwit, wat het effect nabootst van het verlagen van de concentratie. Om de halo diepgaander te begrijpen varieerden ze het zout om te zien hoeveel tau TDP-43 druppels binnendrong en gebruikten ze computersimulaties die elk aminozuur als een vereenvoudigd kraalmodel behandelen. Deze simulaties reproduceerden de halo en toonden dat de eerste ~40 aminozuren van tau’s negatief geladen N-terminale regio zich verankeren aan het druppeloppervlak, terwijl de rest van het molecuul naar buiten uitstrekt in de omringende vloeistof, waardoor een “amfifiele” (deels druppelminnend, deels waterminnend) schaal ontstaat. Experimenten met een verkort tau-fragment dat dit N-terminaal stuk mist, bevestigden dat zonder die stretch de halo verdwijnt.

Wat dit betekent voor hersenziekten
Samen onthullen de resultaten een algemene set regels voor hoe multicomponent proteïnedruppels zich assembleren en organiseren. In dit tau/TDP-43-systeem, dat situaties in zieke neuronen weerspiegelt, bepalen concentratie en interactiesterkte samen welke eiwitten druppels bouwen en welke ze slechts vullen. Oppervlaktespanning en amfifiele ordening vormen vervolgens gelaagde druppels en halo’s die meerdere ziektegerelateerde eiwitten in dezelfde beperkte ruimte kunnen concentreren, wat mogelijk hun verharding tot aggregaten bevordert. Voor een niet-specialist is de kernboodschap dat tau en TDP-43 niet zomaar willekeurig klonteren; ze organiseren zich tot gestructureerde vloeibare druppels waarvan de architectuur wordt bepaald door eenvoudige fysische principes. Het begrijpen en uiteindelijk manipuleren van die principes kan nieuwe wegen openen om schadelijke eiwitophopingen bij neurodegeneratieve ziekten te vertragen of te voorkomen.
Bronvermelding: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
Trefwoorden: proteïnecondensaten, vloeistof-vloeistof fasediagram, tau, TDP-43, neurodegeneratie