Clear Sky Science · nl
Kristallisatie getriggerd door massadiffusie bij een lagere lokale oververzadiging
Waarom dit verder reikt dan het laboratorium
Zoutkristallen lijken misschien alledaags, maar de manier waarop ze ontstaan heeft grote gevolgen — van de productie van geneesmiddelen tot het terugwinnen van grondstoffen uit zoute afvalwaters. Deze studie toont aan dat kristallen eerder en op andere plekken kunnen beginnen te vormen wanneer de vloeistof subtiel uit balans wordt gebracht door temperatuur- en concentratiegradiënten. Inzicht in dit verfijnde gedrag kan helpen bij het ontwerpen van schonere, goedkopere methoden om pekels te behandelen, betere materialen te maken en ongewenste aanslag in leidingen en apparatuur te beheersen.

Hoe kristallen gewoonlijk ontstaan
Kristallisatie treedt op wanneer een opgeloste stof, zoals kaliumchloride (KCl) in water, de hoeveelheid overschrijdt die comfortabel opgelost kan blijven. Deze toestand wordt oververzadiging genoemd. Klassieke theorieën stellen dat kristallen alleen verschijnen wanneer de oververzadiging groot genoeg is om een energiedrempel te overwinnen, en dat nucleatie zou moeten beginnen waar de oplossing het meest oververzadigd is. In de industrie duwt men oplossingen meestal in deze toestand door ze te koelen, oplosmiddel te verdampen of een "antisolvant" toe te voegen. Onder deze conventionele, vrijwel uniforme omstandigheden hebben onderzoekers een metastabiel gebied in kaart gebracht — een venster waarin de vloeistof oververzadigd is maar er nog geen zichtbare kristallen zijn gevormd.
Drie verschillende manieren om hetzelfde zout te laten kristalliseren
De auteurs onderzochten hoe KCl-kristallen verschijnen onder drie zorgvuldig gecontroleerde scenario’s in een op maat gemaakte platte cel met afzonderlijke temperatuurregeling boven en onder. Ten eerste voerden ze standaard koelingsexperimenten uit, waarbij de temperatuur uniform werd verlaagd vanaf 20 °C en ze keken wanneer de eerste kristallen verschenen. Dit gaf een referentiegrens in de concentratie–temperatuurkaart: onder een bepaalde temperatuur vormden kristallen altijd; daarboven bleef de oplossing urenlang kristalvrij. Ze vergeleken deze referentie vervolgens met twee complexere situaties waarin de oplossing richtinggebonden massatransport ervoer in plaats van eenvoudige, uniforme koeling.
Wanneer warmte zout laat bewegen
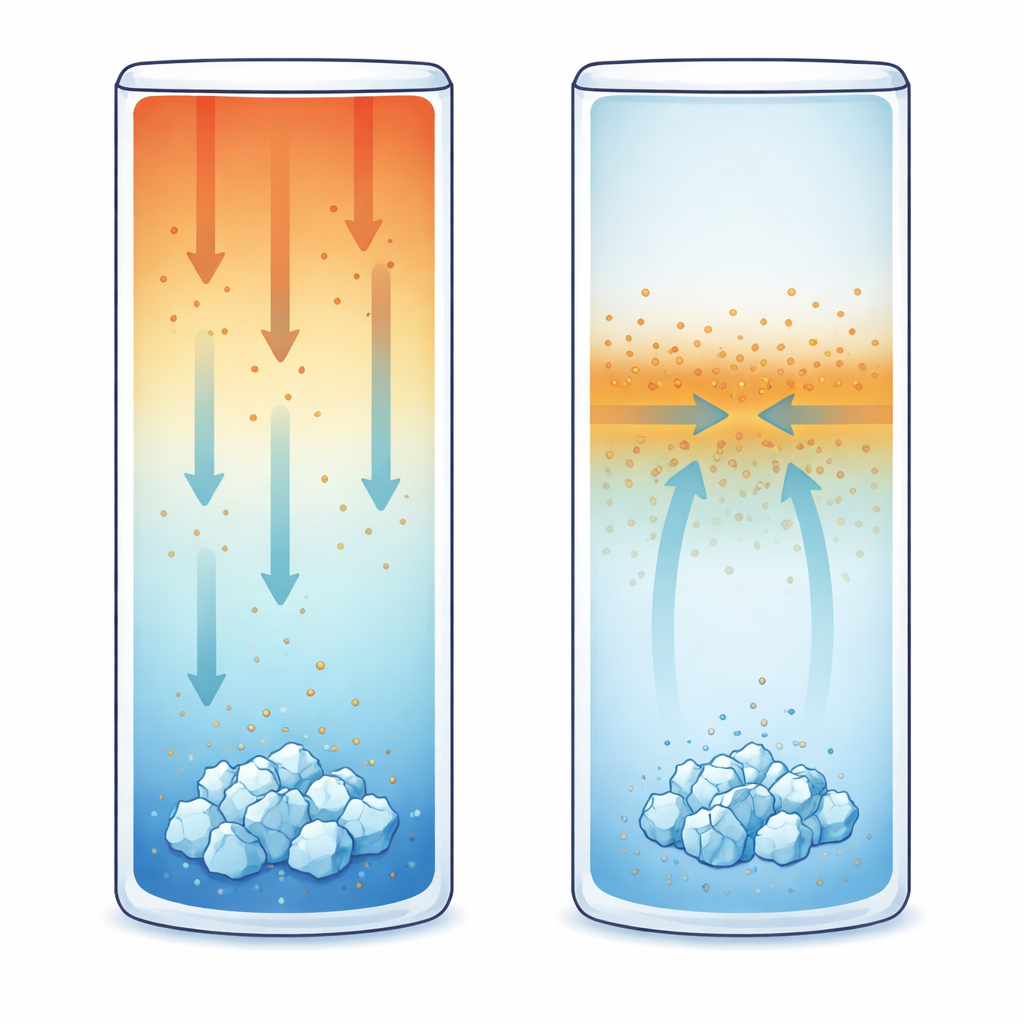
In de tweede reeks experimenten begon de oplossing met dezelfde samenstelling maar werd de bovenkant op 20 °C gehouden terwijl de onderkant werd gekoeld tot 15 °C. Deze verticale temperatuurgradiënt veroorzaakt thermodiffusie, wat betekent dat opgeloste ionen verschuiven als reactie op temperatuur, niet alleen op concentratie. Voor KCl in het onderzochte bereik is het gedrag thermofobisch: ionen neigen naar het koudere gebied te bewegen, waardoor zich meer zout ophoopt nabij de onderkant. Met behulp van een gevoelige optische methode genaamd faseverschuivingsinterferometrie volgden de onderzoekers kleine veranderingen in brekingsindex die onthullen hoe concentratie en temperatuur zich ontwikkelen. Ze vonden dat kristallen consequent gevormd werden aan de koude onderste wand in regio’s waar de concentratiegradiënt het steilst was — en toch was de lokale oververzadiging daar iets lager dan in het geval van uniforme koeling. Met andere woorden, de aanwezigheid van een aanhoudende massastroom maakte het mogelijk dat kristallisatie eerder begon dan verwacht.
Wanneer zout diffundeert bij een volkomen constante temperatuur
Het derde scenario verwijderde temperatuurverschillen volledig. De hele cel werd op een uniforme 17 °C gehouden en aanvankelijk gevuld met de referentieoplossing. Vervolgens werd een kleinere hoeveelheid verdunde KCl-oplossing zachtjes geïnjecteerd vanuit één hoek bovenaan, waarbij een scherpe concentratiecontrastr werd gecreëerd maar vrijwel geen stroming in de vloeistof ontstond. Diffusie egaliseerde deze contrasten toen ionen vanuit het geconcentreerdere gebied naar het verdunde gebied migreerden. Ook nu liet interferometrie zien hoe het concentratieveld in de loop van de tijd veranderde. Verrassend genoeg verschenen de eerste zichtbare kristallen niet waar de oplossing het meest oververzadigd was. In plaats daarvan vormden ze zich grofweg halverwege de cel, nabij de interface waar de concentratiegradiënt — en dus de diffusive massastroom — het sterkst was.
Wat dit betekent voor theorie en technologie
Over alle drie de methoden — koeling, thermodiffusie en isotherme diffusie — zagen de eerste opgekomen kristallen er heel vergelijkbaar uit: voornamelijk kubische KCl-kristallen met bekende groeivormen. Wat veranderde, was niet de kristalstructuur maar de omstandigheden die hun ontstaan veroorzaakten. Onder opgelegde massastromen verschenen kristallen bij een lagere lokale oververzadiging en op locaties bepaald door gradiënten in plaats van door concentratiepieken. Dit suggereert dat directioneel moleculair verkeer in de vloeistof ionen kan helpen zich te ordenen in dichte zones die als vroege kernen fungeren, waardoor het metastabiele gebied effectief smaller wordt. Terwijl de klassieke nucleatietheorie dit gedrag niet volledig kan verklaren, stemmen nieuwere ideeën over multi-stap nucleatie overeen met de bevindingen. In praktische zin wijst het werk op slimmer beheer van kristallisatie in processen zoals zero-liquid-discharge-ontzilting, waar het benutten van thermodiffusie kan helpen om afvalpekel met minder energie en minder chemicaliën in vaste zouten om te zetten.
Bronvermelding: Xu, S., Torres, J.F. Crystallisation triggered by mass diffusion at a lower local supersaturation. Commun Chem 9, 125 (2026). https://doi.org/10.1038/s42004-026-01925-8
Trefwoorden: kristallisatie, thermodiffusie, oververzadiging, ontzilting, massatransport