Clear Sky Science · nl
Synergetische effecten tussen kationen en kristalvlakken versnellen de alkalische waterstofontwikkelingskinetiek op getrapte Pt‑oppervlakken
Waarom dit belangrijk is voor schone energie
Het produceren van schone waterstof uit water is een cruciaal onderdeel van veel netto‑nul‑energieplannen, maar de meest praktische apparaten van vandaag verspillen energie omdat de reactie die waterstofbellen vormt verrassend traag kan zijn in alkalische (basische) oplossingen. Deze studie gaat tot op het niveau van individuele atomen en watermoleculen om uit te leggen waarom sommige platinaoppervlakken beter werken dan andere, en hoe veelvoorkomende opgeloste ionen in de vloeistof met het metaaloppervlak kunnen samenwerken om de waterstofproductie te versnellen.
Metaloppervlakken vormen om water te richten
De onderzoekers concentreren zich op platina, het referentiemateriaal voor watersplitsing, en vergelijken twee soorten atomaire landschappen op het oppervlak. Het ene is vlak, als een glad terras (Pt(111)); het andere is getrapt, als een kleine wenteltrap (Pt(311)). Met geavanceerde quantum‑mechanische simulaties die zowel elektronen als bewegende watermoleculen meenemen, modelleren ze hoe deze verschillende oppervlakken zich gedragen onder realistische bedrijfsspanningen in een alkalische elektrolyser. Het doel is te zien hoe de lokale omgeving direct naast het metaal — waar water, ionen en elektronen elkaar ontmoeten — de snelheid van de eerste stap in de waterstofvorming beheerst.
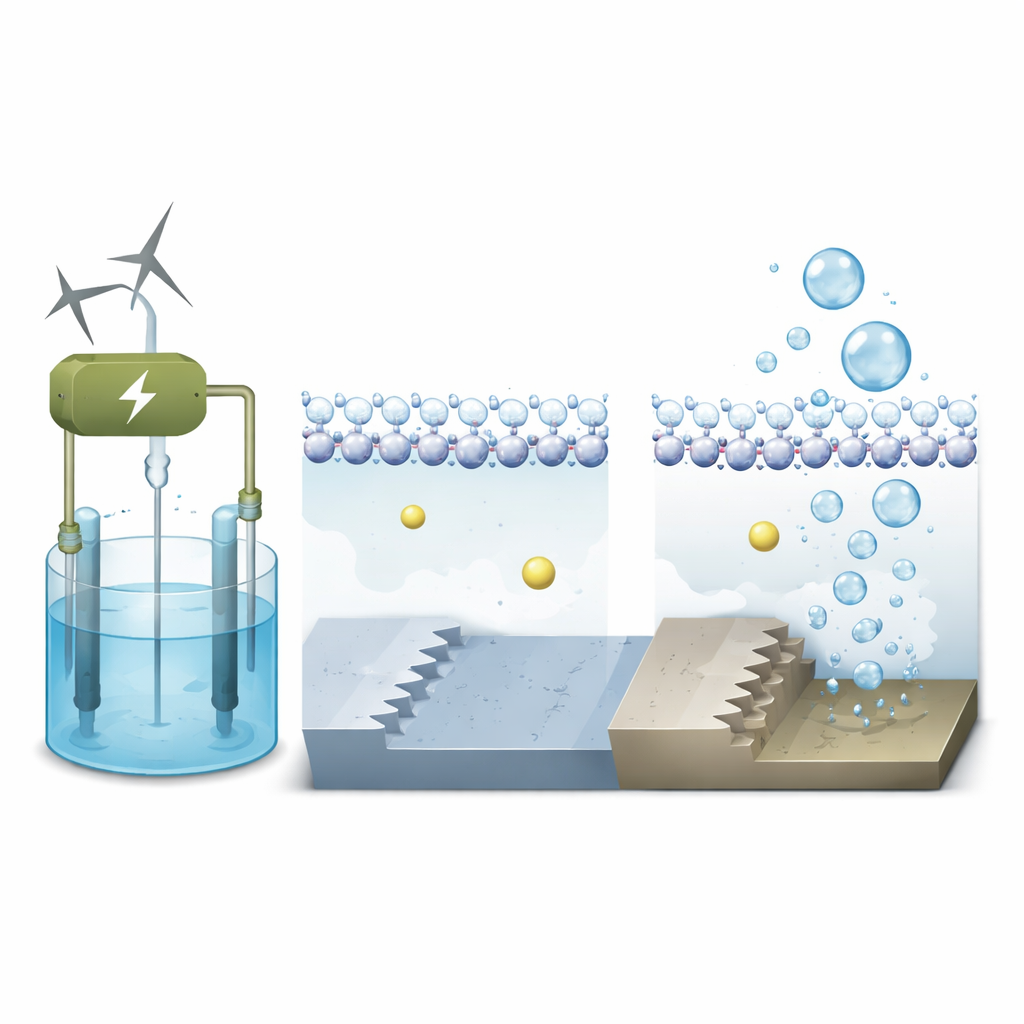
Zoutionen als verborgen helpers
In alkalische elektrolysers bevat de vloeistof alkalimetalkationen zoals natrium. Deze positief geladen ionen doen meer dan alleen rondzwemmen; ze kunnen zich clusteren nabij de elektrode en het elektrische veld bij de interface subtiel hervormen. De simulaties tonen aan dat op het vlakke platinaterras water een dichte, ordelijke laag vormt met waterstofatomen die naar beneden wijzen richting het negatief geladen oppervlak. Natriumionen blijven verder weg, gescheiden van het metaal door dit waterschild, zodat hun invloed op de reactie beperkt is. Op het getrapte oppervlak echter binden de ondergecoördineerde atomen bij de trede water sterker en creëren ze een ruwere, meer ongeordende lokale waterstructuur.
Een speciaal clusters dicht bij het oppervlak dat ionen aantrekt
Bij deze trede‑randen ontdekt het team een terugkerend structureel motief: een watermolecuul dat direct aan de platinatrede gebonden is en op zijn beurt een nabijgelegen natriumion vasthoudt, omringd door extra watermoleculen. Dit compacte platinum–water–natriumcluster trekt het ion effectief ongeveer 2,3 angström dichter naar het metaal dan op het vlakke oppervlak. Dichterbij zijn vergroot het lokale elektrische veld in dit kleine gebied sterk, wat de omliggende watermoleculen krachtig polariseert. De simulaties laten zien dat één O–H‑binding in deze watermoleculen meer uitgerekt is dan gebruikelijk, wat aangeeft dat die al gedeeltelijk op het punt staat te breken nog voordat de reactie formeel begint.
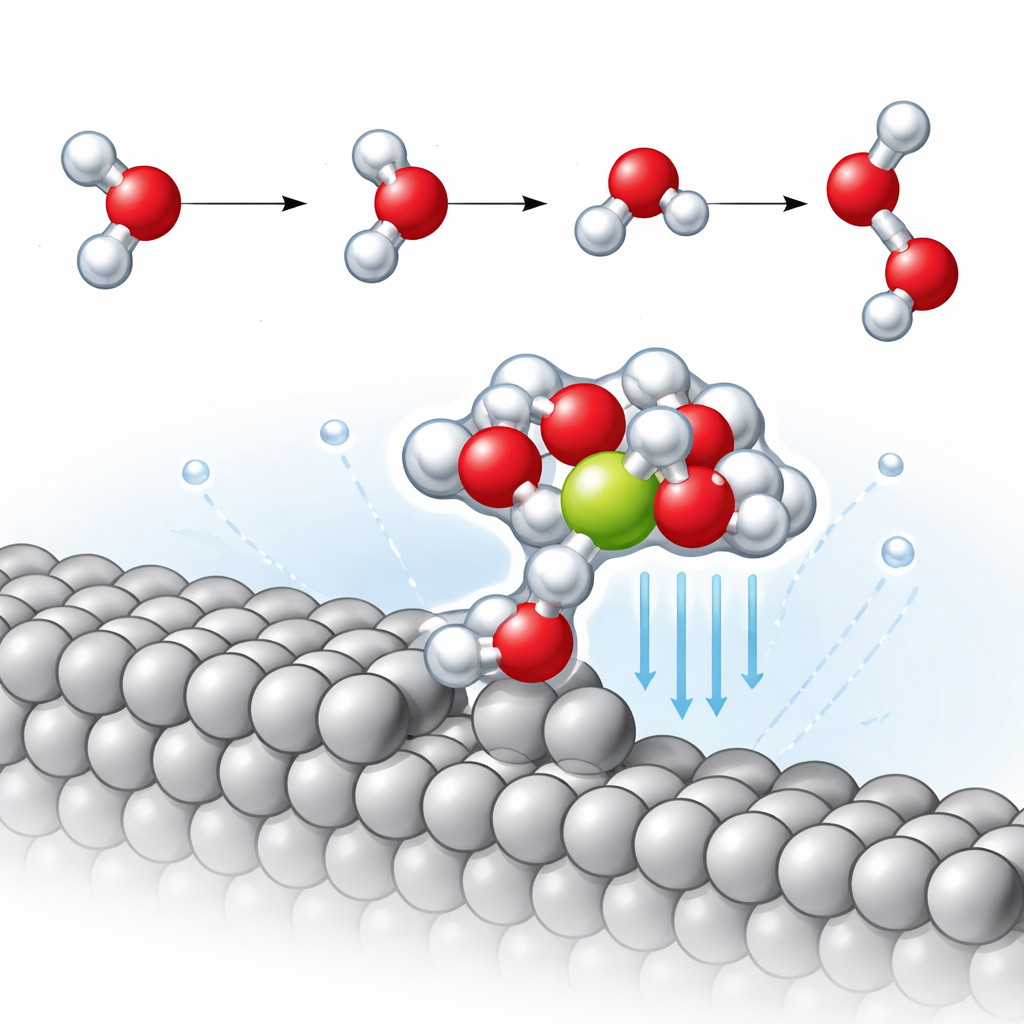
De barrière voor waterstofvorming verlagen
De belangrijkste trage stap in alkalische waterstofontwikkeling staat bekend als de Volmer‑stap, waarbij een watermolecuul splitst: waterstof bindt aan het metaal terwijl de overgebleven hydroxide in de vloeistof wegdrijft. Door het minimalenergie‑reactiepad te volgen vinden de auteurs dat op het vlakke platinavlak natrium slechts een klein effect heeft op de activeringsenergie voor deze stap. Daarentegen verlaagt op het getrapte oppervlak het door natrium gestabiliseerde nabije cluster de activeringsenergie met ongeveer 0,14 elektronvolt — ruwweg drie keer de verbetering die op het vlakke vlak wordt gezien. Gedetailleerde analyse van vibratiebewegingen toont aan dat de O–H‑binding die naar het oppervlak wijst significant verzwakt in aanwezigheid van het dichtbije ion, waardoor die gemakkelijker breekt en de waterstofvorming versnelt.
Een ontwerprichtlijn voor betere waterstofkatalysatoren
Samengevat concluderen de onderzoekers dat de beste prestaties in alkalische waterstofproductie niet alleen voortkomen uit het metaaloppervlak of het elektrolyt, maar uit hun synergie. Getrapte platinaplaatsen die speciale water–ionclusters kunnen verankeren trekken alkalikationen dichtbij, versterken het lokale elektrische veld, breken waterbindingen deels voorgoed en versnellen sterk de cruciale eerste stap van de waterstofontwikkeling. Voor de lezer zonder specialistische achtergrond is de hoofdles dat door zorgvuldig de microscopische vorm van katalysatoroppervlakken te vormen en elektrolyten te kiezen die de juiste ionen naar de juiste plekken brengen, ingenieurs sommige fundamentele vertragingen van alkalische apparaten kunnen overwinnen en efficiëntere, energiezuinige systemen voor schone waterstofproductie kunnen ontwerpen.
Bronvermelding: Zhang, Q., Sun, P., Li, H. et al. Synergistic cation-facet effects boost alkaline hydrogen evolution kinetics on stepped Pt surfaces. Commun Chem 9, 113 (2026). https://doi.org/10.1038/s42004-026-01924-9
Trefwoorden: waterstofontwikkeling, alkalische elektrolyse, platinumkatalysator, interfaciaal water, alkalimetalkationen