Clear Sky Science · nl
Structurele basis voor filamentvorming van menselijk RegIIIα
Hoe onze darmen strijd voeren tegen ziekteverwekkers
Onze darmen worden voortdurend blootgesteld aan miljarden bacteriën, waarvan vele onschadelijk of zelfs nuttig zijn. Wanneer er echter gevaarlijke microben verschijnen, heeft het lichaam snelle en nauwkeurige manieren nodig om ze aan te pakken zonder eigen weefsels te beschadigen. Deze studie bekijkt één dergelijke natuurlijke verdedigingsproteïne, RegIIIα, en laat zien hoe het van vorm verandert om bacteriën te doden en daarna overschakelt naar een veiliger, minder schadelijke toestand. Inzicht in deze vormverandering kan onderzoekers helpen beter te begrijpen hoe we darmmicroben in balans houden en wat er misgaat bij ziekte.
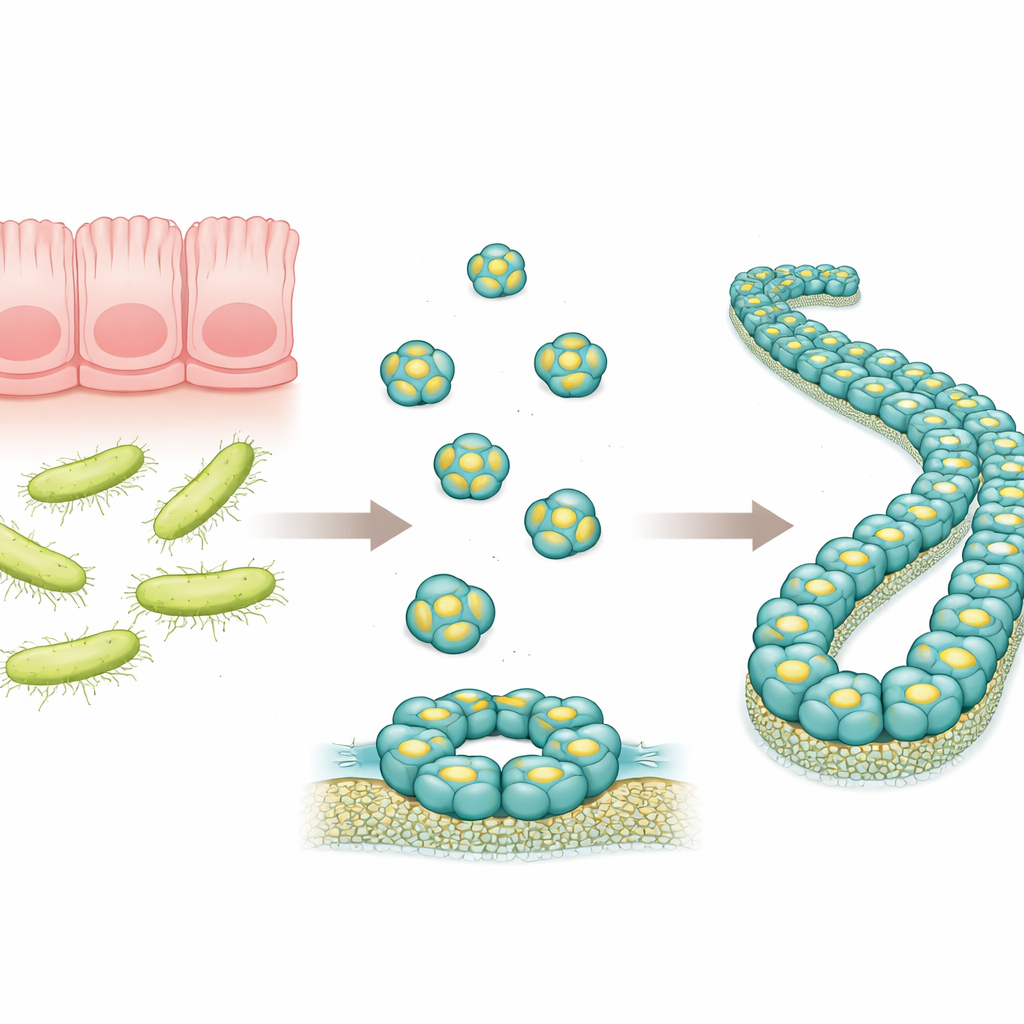
Een kleine verdediger in de darm
RegIIIα is een proteïne dat in het spijsverteringskanaal wordt gemaakt en bepaalde bacteriën target, vooral die met dikke buitenwanden die bekendstaan als Gram-positieve bacteriën. Eerder werk suggereerde dat RegIIIα gaten in bacteriële membranen kan maken door ringachtige structuren te vormen, waardoor de inhoud van de microbe lekt en deze sterft. Onderzoekers hadden ook gezien dat deze ringstructuren na verloop van tijd kunnen stapelen tot lange filamenten, die de dodelijke werking van het proteïne lijken te verminderen. De precieze rangschikking van RegIIIα-moleculen in deze grotere assemblages was echter niet in detail bekend, wat het lastig maakte te begrijpen hoe het proteïne werkt en hoe de activiteit ervan wordt gereguleerd.
Het filament in atomaire detail zien
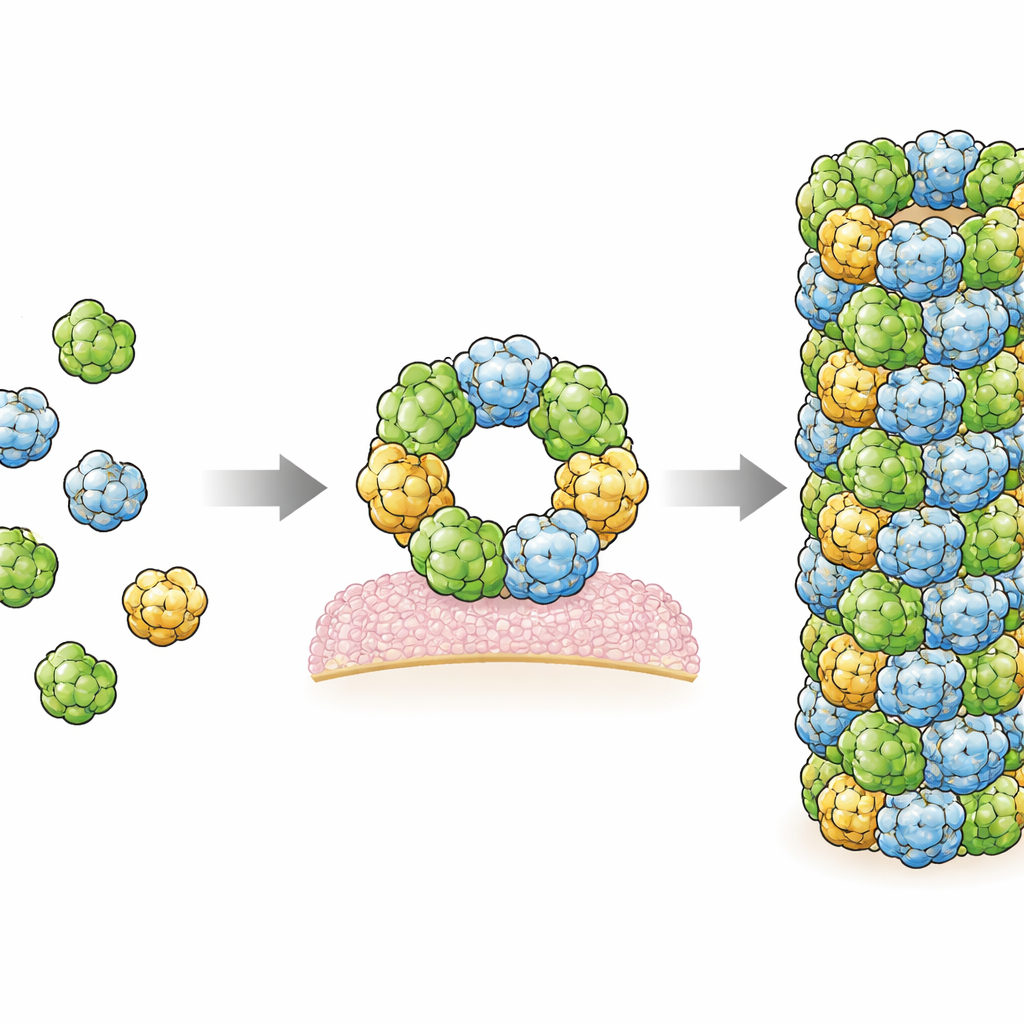
In deze studie produceerden de auteurs menselijk RegIIIα in bacteriën en brachten het vervolgens onder gecontroleerde omstandigheden tot assemblage in filamenten. Ze gebruikten een krachtige beeldvormingstechniek, kryo-elektronenmicroscopie, die biologische moleculen bevroren in een dunne ijslaag tot bijna atomaire resolutie kan visualiseren. Ze vonden dat de filamenten zijn opgebouwd uit herhalende sets van drie identieke RegIIIα-eenheden, trimers genoemd, die in een regelmatige spiraalpatroon stapelen. Elk individueel RegIIIα-molecuul lijkt sterk op wat eerder in kristalstructuren was gezien, maar hun oriëntatie binnen het filament verschilt van die in een eerder, lager-resolutiemodel. Deze gecorrigeerde oriëntatie verandert hoe wetenschappers denken over de interactie van het proteïne met bacteriële membranen en met zijn eigen regulerende segment.
Hoe proteïnen aan elkaar koppelen en waarom lipiden ertoe doen
Door de structuur nauwkeurig te onderzoeken, identificeerden de onderzoekers twee hoofdcontactgebieden, of interfaces, waar aangrenzende RegIIIα-moleculen elkaar raken en het filament bij elkaar houden. Ze veranderden vervolgens specifieke aminozuren op deze interfaces en toonden aan dat deze wijzigingen filamentvorming voorkwamen, wat bevestigt dat deze contactplaatsen essentieel zijn. Interessant genoeg toonden de cryo-EM-kaarten in beide interfaces extra vage regio’s die waarschijnlijk kleine, langwerpige moleculen vertegenwoordigen die tussen eiwitoppervlakken geklemd zitten. Hun vorm en chemische omgeving suggereren dat het lipiden kunnen zijn — hetzelfde soort vette moleculen waar celmembranen uit bestaan. Dit ondersteunt eerdere aanwijzingen dat lipiden helpen bij het bevorderen van RegIIIα-assemblage, mogelijk door te fungeren als moleculair lijm die de verbindingen tussen subunits stabiliseert.
De aan/uit-schakelaar: pH en een verborgen segment
Het team onderzocht ook wat bepaalt wanneer RegIIIα kan assembleren. Voordat het actief wordt, draagt het proteïne een kort “pro-segment” dat door spijsverteringsenzymen moet worden weggesneden. In hun hoogresolutie filamentstructuur is er geen ruimte in het midden van de assemblage om dit extra stukje te herbergen, wat impliceert dat het pro-segment de mogelijkheid van RegIIIα blokkeert om eerst pore-vormende ringen en filamenten te vormen. Ze ontdekten dat de neiging om filamenten te vormen ook afhankelijk is van zuurgraad: filamenten vormen zich gemakkelijk bij een pH vergelijkbaar met die van de dunne darm, maar slecht bij een meer zure pH. Eén enkel aminozuur, histidine 50, lijkt te fungeren als een pH-gevoelige schakelaar; wanneer dit wordt veranderd in een ander residu, wordt filamentvorming veel minder pH-gevoelig. Samen creëren deze eigenschappen — enzymknippen, lipidebinding en pH — een gelaagd regelsysteem dat afstemt wanneer en waar RegIIIα actief is.
Wat dit betekent voor darmgezondheid
Alles bij elkaar biedt dit werk het meest gedetailleerde beeld tot nu toe van hoe RegIIIα-moleculen zich assembleren tot grotere structuren die verband houden met zowel hun antibacteriële werking als hun zelfbeperkende gedrag. Dezelfde interfaces die de filamenten bouwen, vormen ook de hexamerische ringen waarvan wordt gedacht dat ze poriën in bacteriële membranen vormen, wat wijst op een delicate balans tussen een krachtige dodelijke vorm en een veiligere, ingetogener staat. Het in kaart brengen van ziektegerelateerde mutaties op deze structuur toont aan dat veel daarvan op sleutelcontactpunten liggen, wat suggereert dat verstoringen in assemblage ten grondslag kunnen liggen aan bepaalde darm- of pancreasaandoeningen. Door te verduidelijken hoe dit natuurlijke antibioticum wordt geactiveerd, geleid door lipiden en gevormd door lokale pH, legt de studie een basis voor toekomstige inspanningen om onze aangeboren afweer te moduleren — ofwel door deze te versterken tegen infectie of door ze te kalmeren wanneer ze ontregeld raken.
Bronvermelding: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
Trefwoorden: RegIIIα, darmimmuniteit, kryo-elektronenmicroscopie, proteïnefilamenten, antibacteriële peptiden