Clear Sky Science · nl
Azobenzeen-gekoppelde ioniseerbare amfifiele Janus-glycosiden voor lichtgestuurde, enkelcomponent- en orgaan-moduleerbare pDNA-afgifte
Het verlichten van slimmer gentransport
Gentherapieën beloven aandoeningen bij de wortel te behandelen door stukjes genetische code rechtstreeks in onze cellen af te leveren. Maar het veilig sturen van deze kwetsbare lading door de bloedbaan, naar de juiste organen en in doelcellen blijft een grote uitdaging. Deze studie introduceert een nieuwe klasse van kleine, suikergebaseerde deeltjes waarvan het gedrag met licht kan worden geschakeld voordat ze het lichaam binnengaan, waardoor onderzoekers kunnen bepalen waar een therapeutisch gen terechtkomt en hoe sterk het tot expressie komt, terwijl de cellen grotendeels ongeschonden blijven. 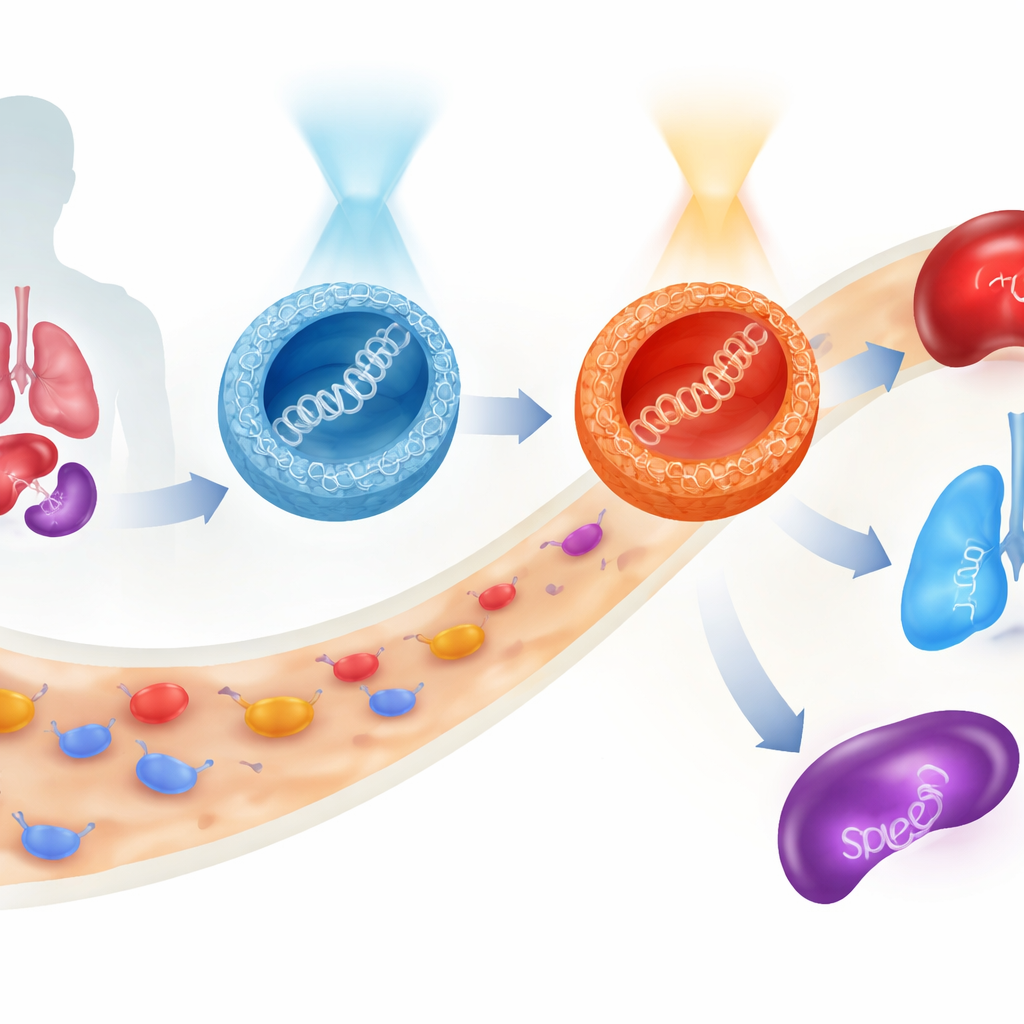
De behoefte aan precieze genetische koeriers
De meest succesvolle genafgifte-voertuigen van vandaag zijn lipide-nanodeeltjes, die hebben bijgedragen aan de ontwikkeling van mRNA-COVID-19-vaccins. Deze multi-component druppels wikkelen en beschermen nucleïnezuren, maar ze hopen zich meestal hoofdzakelijk in de lever op en geven slechts een klein deel van hun lading vrij binnen cellen. Het aanpassen van hun samenstellingen kan veranderen welke organen ze bevoordelen, maar de mengsels zijn complex en moeilijk precies te beheersen. Het team achter dit werk wilde in plaats daarvan enkelvoudige, goed gedefinieerde moleculen ontwerpen die zich assembleren tot nanodeeltjes met voorspelbare vormen en eigenschappen—en die van buitenaf actief kunnen worden bijgesteld met een eenvoudige lichttrigger.
Een moleculaire schommel, gecontroleerd door licht
In de kern van het nieuwe systeem staan dubbele “Janus”-glycosiden: moleculen opgebouwd uit twee glucosenheden, voorzien van waterminnende geladen koppen en vetminnende staarten, verbonden door een centraal azobenzeen-"scharnier." Azobenzeen kan omslaan tussen twee spiegelachtige vormen, E en Z genoemd, wanneer het wordt blootgesteld aan verschillende kleuren licht. In water met DNA aanwezig, verzamelen veel kopieën van deze moleculen zich spontaan tot zachte, gelaagde deeltjes die zich om plasmide-DNA-strengen wikkelen. De onderzoekers maakten twee versies—één met zuurstofbruggen en één met zwavelbruggen tussen de suiker en het scharnier—om stabiliteit en biologisch gedrag subtiel af te stemmen. Door oplossingen vooraf te belichten konden ze de E- of Z-vorm verrijken en bestuderen hoe elke toestand de resulterende genafgifte-deeltjes vormt.
Hoe vormveranderende deeltjes zich gedragen
Metingen van deeltjesgrootte, oppervlaktelading en interne structuur toonden aan dat lichtgeïnduceerde schakeling tussen E- en Z-toestanden duidelijke fysieke gevolgen heeft. Over het algemeen gaf de Z-vorm kleinere, uniformer gevormde nanodeeltjes met een meer geordend, gelaagd interieur dan de E-vorm. Microscopen toonden dat deze interne ordening lijkt op afwisselende lagen van lipide-achtig materiaal en DNA. Belangrijk is dat beide toestanden DNA beschermden tegen enzymatische afbraak. In gekweekte cellen uit nier-, lever- en immuunweefsel produceerden de verschillende isomere toestanden opvallend verschillende niveaus van genexpressie, hoewel het onderliggende DNA identiek was. Herhaalde lichtpulsen toegepast nadat de deeltjes cellen waren binnengedrongen verhoogden de genexpressie meerdere keren, wat suggereert dat de mechanische schok door schakelen helpt deeltjes losser te maken en hun lading vrij te geven, en mogelijk ook helpt bij ontsnapping uit intracellulaire compartimenten. 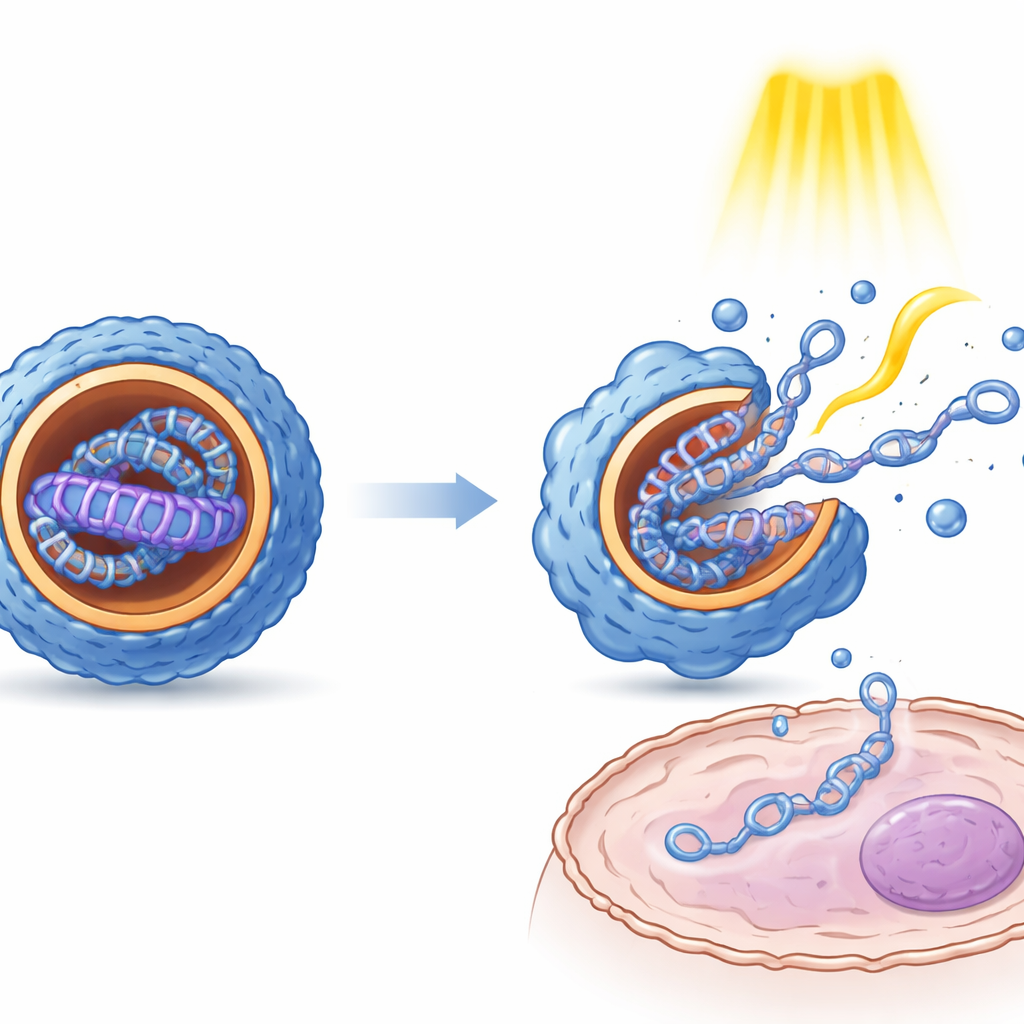
Genen naar specifieke organen leiden
Het meest verrassende gedrag trad op bij muizen. Wanneer de zuurstof-gekoppelde deeltjes in hun E-rijke vorm werden toegediend, vond expressie van een markergene voornamelijk in de lever plaats en deels in de longen. Door ze voor injectie naar de Z-vorm te schakelen nam niet alleen de totale expressie toe, maar verschoof ook het evenwicht richting de longen. De zwavel-gekoppelde deeltjes vertelden een ander verhaal: hun Z-vorm begunstigde de milt, een belangrijk immuunorgaan. Zo konden de onderzoekers, met hetzelfde basale moleculaire raamwerk—en zonder het DNA-cargo te veranderen—genactiviteit hoofdzakelijk naar lever, long of milt dirigeren door simpelweg de verbinding (zuurstof of zwavel) en de licht-geactiveerde vorm (E of Z) van de drager te kiezen. Gedurende deze testen bleef de celviabiliteit hoog, wat suggereert dat het systeem relatief zacht is.
Een licht-afstembare route naar toekomstige genmedicijnen
In alledaagse termen heeft het team een kleine, lichtschakelbare shuttle voor DNA gebouwd. Voor injectie "programmeert" een korte lichtbehandeling de shuttles in één van twee vormen. Elke vorm assembleert tot nanodeeltjes met karakteristieke grootte en oppervlaktesensatie, die op hun beurt bepalen hoe sterk ze aan verschillende celtypes hechten en waar ze in het lichaam terechtkomen. Omdat hetzelfde chemische skelet op veel kleine manieren kan worden aangepast, en omdat de schakeling reversibel is en het DNA zelf niet verandert, biedt dit platform een flexibele manier om te verfijnen waar en hoe gentherapieën werken. Hoewel er nog veel werk nodig is vóór klinisch gebruik, toont de studie aan dat zorgvuldig ontworpen, enkel-molecuul dragers die door licht worden gecontroleerd krachtige hulpmiddelen kunnen worden voor veiligere, preciezere genetische geneesmiddelen.
Bronvermelding: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Trefwoorden: genafgifte, lichtgevoelige nanodeeltjes, azobenzeen-schakelaars, gerichte DNA-therapie, nanogeneeskunde