Clear Sky Science · nl
S9-protease WprP2 katalyseert uniforme knip op het voorloperpeptide in RiPP-biosynthese
Waarom kleine kniptangen in cellen ertoe doen
In bacteriën knippen gespecialiseerde moleculaire scharen lange ketens van aminozuren in kleinere, actieve stukken die vaak antibiotica of andere nuttige natuurlijke producten worden. Deze studie onthult een eerder onbekend knipgereedschap — een protease genaamd WprP2 — dat zijn doelpeptide met opmerkelijke precisie afknipt. Inzicht in hoe dit enzym werkt kan onderzoekers helpen nieuwe bioactieve peptiden en volgende‑generatie antibiotica te ontwerpen.
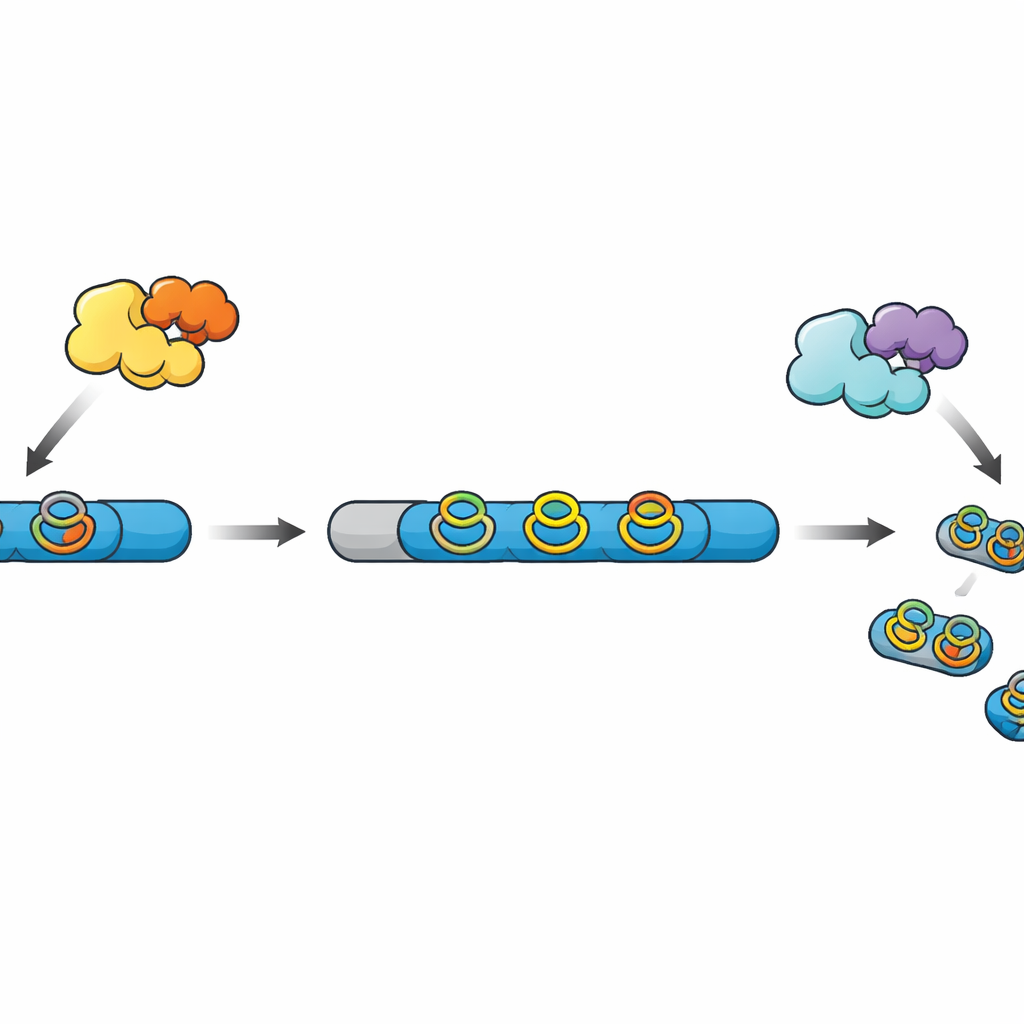
Van ruwe ketens naar afgewerkte mini‑geneesmiddelen
Veel moderne peptidegebaseerde natuurlijke producten, gezamenlijk bekend als RiPPs, beginnen als eenvoudige ketens die op het ribosoom worden gemaakt. Deze ketens bevatten een leader‑regio die als handvat fungeert en een core‑regio die het uiteindelijke product zal worden na een reeks chemische bewerkingen. Andere enzymen voegen crosslinks en ringen toe die het peptide stabieler en actiever maken, en uiteindelijk knipt een protease het leader weg en geeft het rijpe molecuul vrij. In een recent ontdekte familie van RiPPs bouwen radicale SAM‑enzymen compacte “cyclofaant” ringen rond aromatische aminozuren, maar in de meeste bekende genclusters ontbreekt de corresponderende protease, waardoor de laatste verwerkingsstappen mysterieus blijven.
Een ontbrekende partner‑enzym opsporen
De auteurs bestudeerden eerder een radicale SAM‑enzym genaamd WprB1 dat identieke crosslinks installeerde op drie herhalende WPR‑segmenten in een voorloperpeptide. In het nieuwe werk zochten ze in bacteriële genomen naar verwanten van dit enzym en keken ze in de buurt naar genen die een protease zouden kunnen coderen. In Streptomyces venezuelae vonden ze een veelbelovend cluster met een soortgelijk crosslink‑enzym, een helpereiwit, een bijpassend voorloperpeptide met drie WPR‑herhalingen en een kandidaat serine‑protease uit de S9‑familie, die ze WprP2 noemden. Dit maakte het systeem tot een ideaal testveld om te achterhalen hoe het peptide uiteindelijk wordt geknipt om de actieve fragmenten vrij te geven.
Kijken hoe het peptide wordt doorgesneden
Om WprP2 te onderzoeken produceerde het team het voorloperpeptide in bacteriën, zowel met als zonder het crosslink‑enzym, zuiverde het en mengde het vervolgens met de protease in gecontroleerde in vitro‑reacties. Massaspectrometrie toonde aan dat WprP2 eerst de keten meteen na elk WPR‑segment afknipt, en vervolgens een tweede knip uitvoert op een vaste afstand vóór een bepaalde proline‑residu verderop in de sequentie. Deze twee stappen creëren een serie kleinere, uniforme fragmenten. Opmerkelijk genoeg voerde WprP2 dit knippatroon uit ongeacht of het crosslink‑enzym al de cyclofaant‑ringen had aangebracht, wat aantoont dat die ringen niet nodig zijn voor herkenning. Vergeleken met commercieel trypsine, dat niet kan knippen op bepaalde gekruisdisde sites, functioneerde WprP2 nog steeds, wat zijn ongebruikelijke robuustheid benadrukt.
Ontcijferen wat het enzym herkent
De onderzoekers vroegen vervolgens welke kenmerken van het peptide WprP2 feitelijk leest. Door systematisch individuele aminozuren rond de knipplaatsen te veranderen, vonden ze dat het veranderen van veel nabijgelegen residuen weinig effect had, maar dat wijziging van een sleutel‑arginine binnen het WPR‑segment of de glutamine of proline op de tweede knipplaats die specifieke stap kon blokkeren. Experimenten met een verwant voorloperpeptide met andere flankresiduen toonden aan dat de protease nog steeds na WPR‑herhalingen knipte, maar alleen de tweede knip uitvoerde wanneer een glutamine‑proline‑paar aanwezig was. Computergestuurde structurele modellen met AlphaFold3 ondersteunden dit beeld: in de voorspelde complexen lagen de WPR‑gebaseerde en glutamine‑proline‑plaatsen elk om de beurt uitgelijnd met het katalytische centrum van het enzym, wat consistent is met een sequentieel twee‑staps mechanisme.
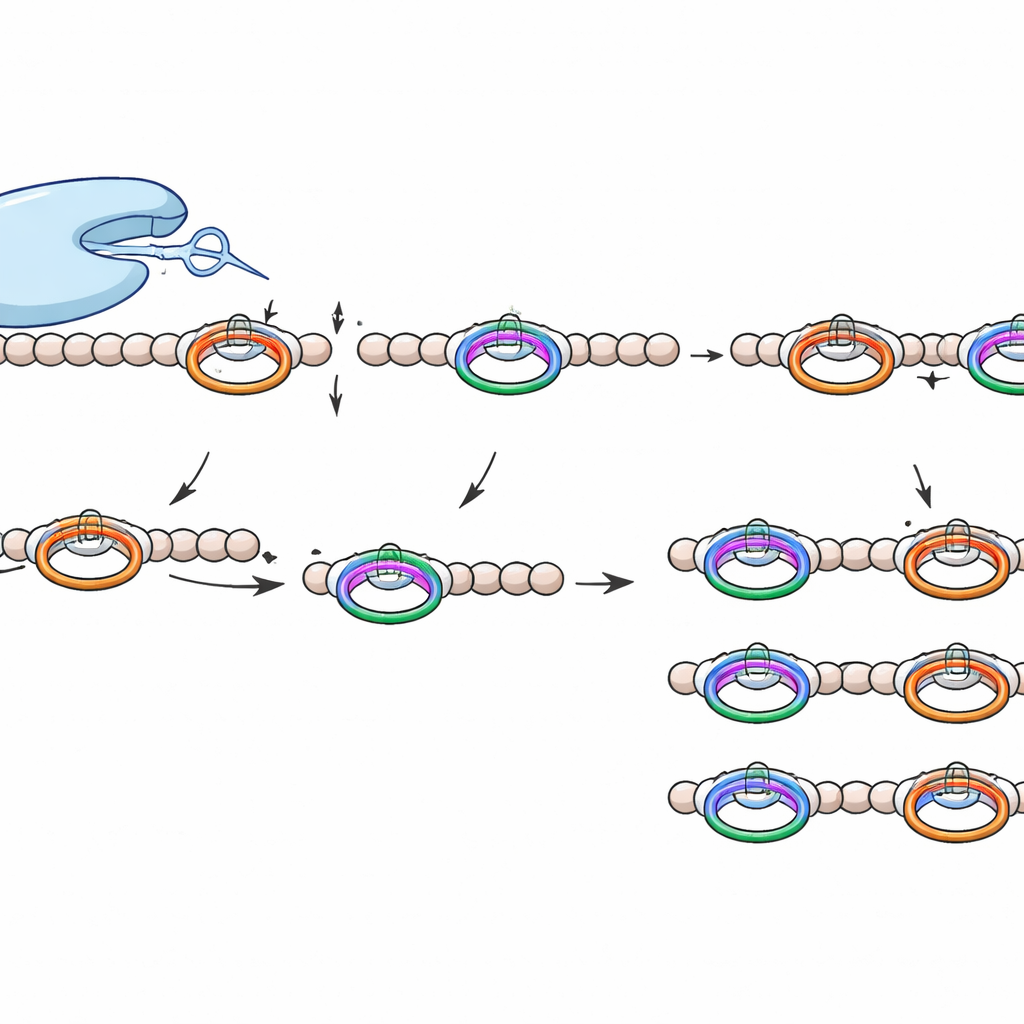
Wat dit knipgereedschap bijzonder maakt
WprP2 behoort tot een bredere S9‑familie van proteases die al medisch relevante enzymen omvat, maar het onderscheidt zich op meerdere manieren. Het knipt aan de N‑terminaalkant van een proline‑residu in plaats van erna, het werkt op een herhalend motief om gelijkmatig gedimensioneerde fragmenten over de hele voorloperketen te genereren, en het toont een brede tolerantie voor de aminozuren die tussen zijn twee herkenningsplaatsen liggen. Deze combinatie van precisie en flexibiliteit is nog niet eerder gezien bij RiPP‑gerelateerde proteases.
Hoe deze ontdekking kan worden gebruikt
Door een protease te onthullen die eenvoudige sequentiecues herkent en uniforme, herhaalde knipsels uitvoert, voegt dit werk een krachtig nieuw instrument toe aan het groeiende arsenaal voor peptide‑engineering. In praktische termen zou WprP2 kunnen worden ingezet om ontwerppeptiden vrij te geven of te hervormen, inclusief die met complexe crosslinks die standaardenzymen zoals trypsine weerstaan. Voor niet‑specialisten is de belangrijkste conclusie dat wetenschappers een nieuw soort moleculaire schaar hebben ontdekt die lange peptideketens in precieze, gelijkmatig gedimensioneerde stukjes snijdt, wat de deur opent naar meer gecontroleerde productie van potentiële antibiotica en andere bioactieve moleculen.
Bronvermelding: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Trefwoorden: RiPP-peptiden, serine-protease, WprP2, cyclofaangewassen, peptide-engineering