Clear Sky Science · nl
Sterische begrenzing-geïnduceerde emissieprobe voor het volgen van eiwitconformaties in levende cellen
Vormen- veranderende eiwitten realtime observeren
In iedere levende cel veranderen eiwitten voortdurend van vorm terwijl ze signalen doorgeven, hun omgeving waarnemen en essentiële taken uitvoeren. Veel ziekten ontstaan wanneer deze vormveranderingen mislopen, maar het is opvallend lastig geweest om zulke bewegingen direct in levende cellen te volgen, vooral over zowel zeer snelle als trage tijdschalen. Dit artikel introduceert een nieuwe lichtgevende probe, BIOSCE genoemd, die kleine eiwitbewegingen omzet in zichtbare flitsen, waardoor onderzoekers individuele eiwitten kunnen volgen terwijl ze buigen, draaien en in realtime in levende cellen met elkaar omgaan. 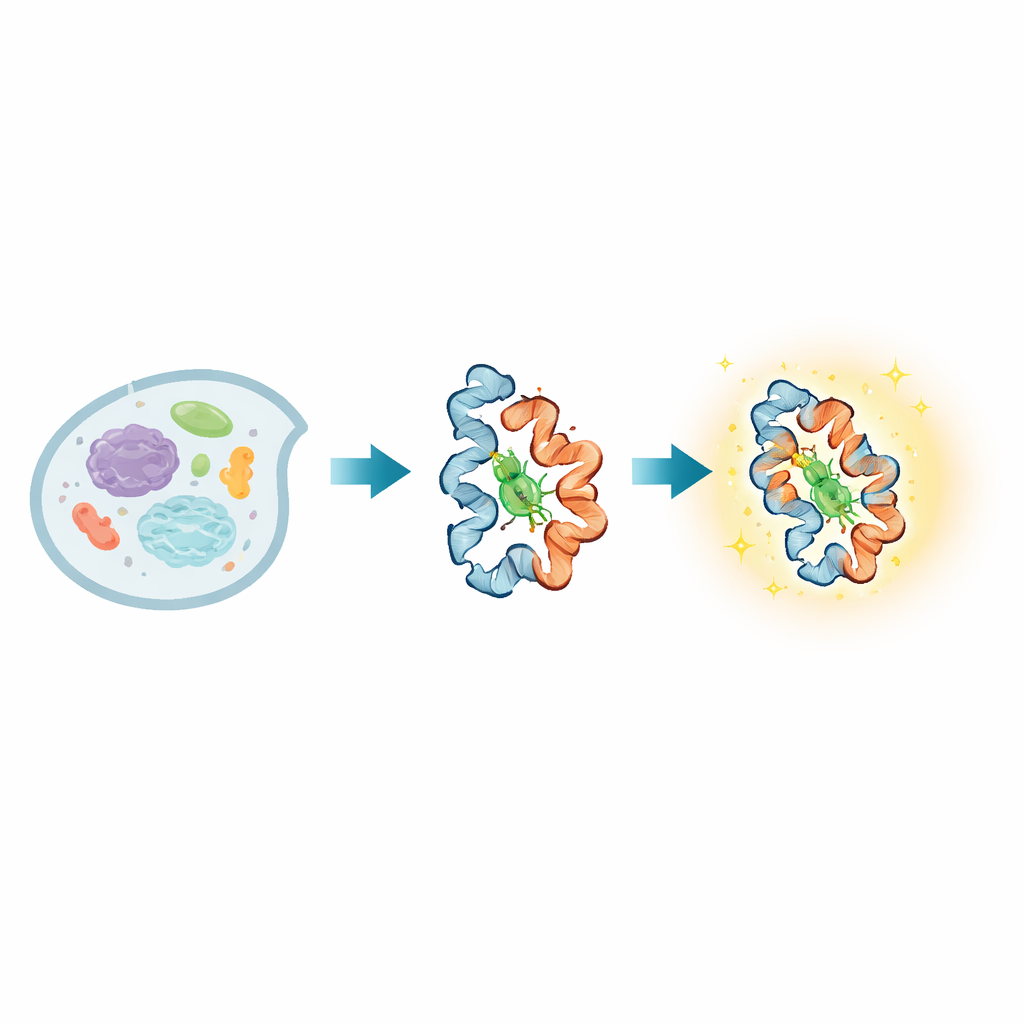
Een nieuwe lichtschakelaar voor bewegende eiwitten
In het hart van BIOSCE bevindt zich een klein kleurstofmolecuul, MTPABP-Cl, dat helderder wordt wanneer het wordt samengedrukt. De onderzoekers hechten deze kleurstof aan een veelgebruikt eiwitlabel genaamd HaloTag, dat genetisch met vrijwel elk doelwit-eiwit kan worden gefuseerd. Wanneer het gelabelde eiwit van vorm verandert of strakker met buren verpakt raakt, verandert de ruimte die de kleurstof heeft om te bewegen. In een losse omgeving kunnen de interne delen van de kleurstof vrij draaien en gaat het geabsorbeerde licht grotendeels verloren door beweging; in een nauwere pocket worden die bewegingen geblokkeerd en geeft de kleurstof die energie in plaats daarvan meer als licht vrij. Deze “sterische begrenzing-geïnduceerde emissie” zet subtiele veranderingen in lokale dichtheid rond een enkel eiwit om in een vloeiende helderheidsverandering, in plaats van een eenvoudige aan/uit‑schakelaar, waardoor de probe zeer gevoelig is voor kleine conformationele veranderingen.
Ontwikkelen en testen van de drukgevoelige kleurstof
Het team ontwierp en synthetiseerde eerst MTPABP-Cl zodat het zwak zou zijn in oplossing maar op zou lichten wanneer het door HaloTag of door een compacter fusie-eiwit op zijn plaats wordt gehouden. Zorgvuldige metingen lieten zien dat de kleurstof blauw licht absorbeert en verrood emitteert, wat gunstig is voor beeldvorming diep in cellen en voor langdurige observatie. Wanneer het alleen aan HaloTag gebonden is, nam de lichtopbrengst toe; wanneer HaloTag gefuseerd was met een partner-eiwit dat zich om de kleurstof heen vouwde, nam de helderheid nog verder toe. Computersimulaties bevestigden dat de kleurstof bij compactere eiwitarrangementen sterke dichtheid, een kleinere blootgestelde oppervlakte en meer stabiliserende contacten ervaart, die allemaal beweging beperken en emissie versterken. De kleurstof bindt ook snel en specifiek aan HaloTag, toont een zeer lage achtergrond in cellen zonder het label en blijft niet-toxisch bij werkconcentraties, wat het gebruik in experimenten met levende cellen ondersteunt. 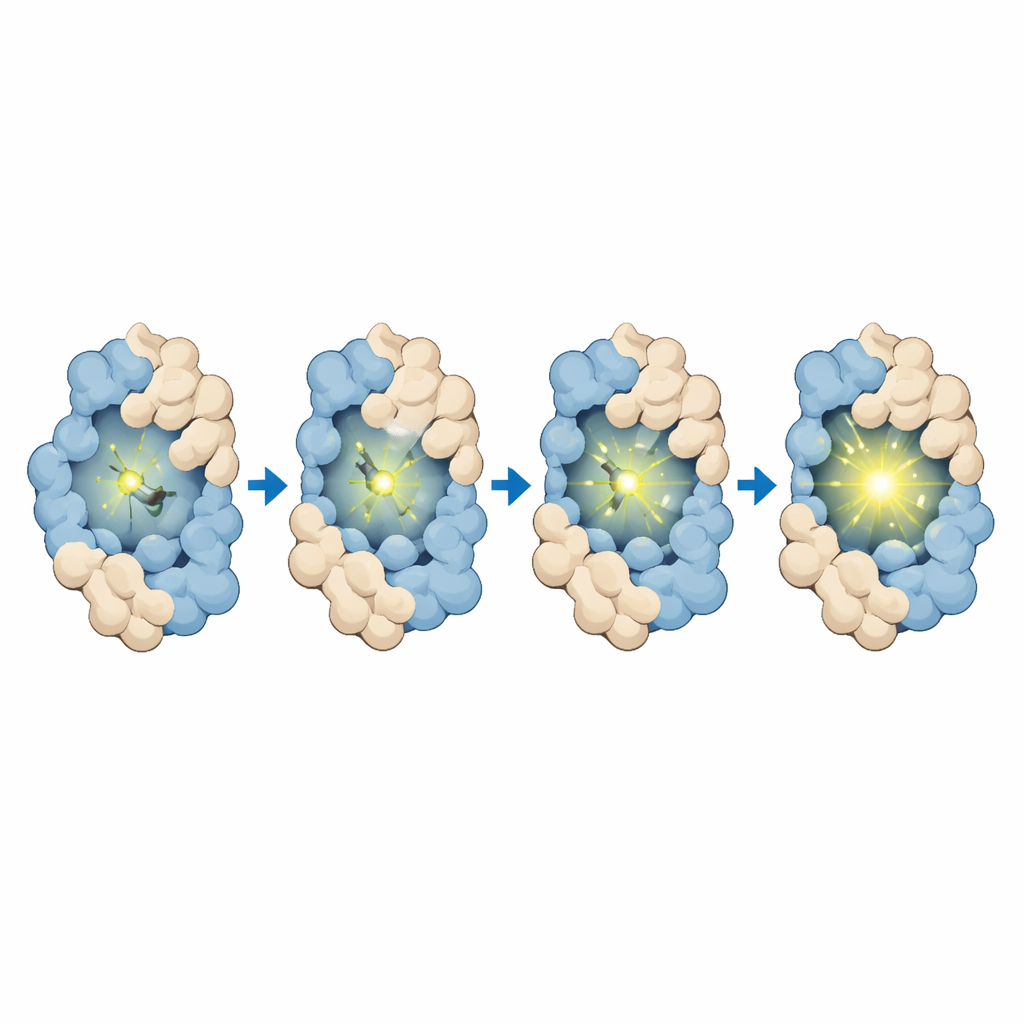
Snelle signalen en eiwitontmoetingen volgen
Om te demonstreren wat BIOSCE kan, pasten de auteurs het toe op verschillende bekende cellulaire processen. Eerst pasten ze het toe op een calciumsensor gebaseerd op calmoduline, een eiwit dat van vorm verandert wanneer het calciumionen bindt — centrale boodschappers bij zenuwontlading en vele andere cellulaire gebeurtenissen. Door calmoduline aan HaloTag te fuseren en te labelen met MTPABP-Cl, creëerden ze een chemigenetische indicator genaamd SCECaMP. In humane cellen en neuronachtige cellen werd deze indicator helderder en zwakker in overeenstemming met calciumpieken veroorzaakt door kaliumstimulatie, met reactiesnelheden vergelijkbaar met de veelgebruikte fluorescerende eiwitten GCaMP. Omdat het BIOSCE-signaal direct afhangt van lokale dichtheid rond de kleurstof, kan het trouw calmodulines structurele veranderingen weerspiegelen terwijl het ook stabiele, langdurige fluorescentie biedt die geschikt is voor uitgebreide beeldvorming.
Interacties door geneesmiddelen en toxines waarnemen
De onderzoekers onderzochten vervolgens of BIOSCE kon volgen wanneer twee eiwitten door een geneesmiddel bijeengebracht worden. Ze gebruikten een klassiek systeem waarin rapamycine twee partners, FKBP en FRB, samenbrengt in een belangrijke groeiregulerende route. Door HaloTag aan FKBP of FRB te bevestigen en te labelen met MTPABP-Cl, zagen ze snelle, milliseconde-schaal stijgingen in fluorescentie toen rapamycine deze eiwitten naar elkaar toe liet bewegen en herschikken. De toename in helderheid weerspiegelde een strakker micro‑milieu rond de kleurstof toen de partners dicht bij elkaar kwamen. In een complexere test bestudeerden ze SNAP25, een zenuweindeiwit cruciaal voor de afgifte van neurotransmitters en het belangrijkste doelwit van botulinum neurotoxine A. Door HaloTag aan weerszijden van het knippunt van het toxine te plaatsen en te labelen met de kleurstof, konden ze afzonderlijk de bewegingen van de N- en C‑terminale fragments na knippen volgen. Single-particle tracking toonde dat het ene fragment verankerd bleef nabij het celmembraan, terwijl het andere vrijer door het cytoplasma diffundeerde, en dat het exacte patroon afhing van of de labeling vóór of na blootstelling aan het toxine plaatsvond. De probe rapporteerde zelfs snelle, zink-geïnduceerde conformationele aanpassingen in SNAP25 tijdens dit proces.
Wat dit betekent voor biologie en geneeskunde
Gezamenlijk laten deze resultaten zien dat BIOSCE een veelzijdige nieuwe manier is om te visualiseren hoe individuele eiwitten bewegen, vouwen en interageren in levende cellen over een breed scala aan tijdschalen. Omdat de methode steunt op een algemene HaloTag-fusie en een enkele klein-molecuul kleurstof, kan ze in principe worden toegepast op vele verschillende eiwitten zonder elke keer het hele sensorontwerp te hoeven herzien. De continue, begrenzingsafhankelijke helderheidsverandering stelt onderzoekers in staat om subtiele structurele verschuivingen te detecteren in plaats van alleen grote, binaire gebeurtenissen. Vooruitkijkend willen de auteurs de toediening van de probe en afbeeldingsdiepte verbeteren zodat BIOSCE in weefsels en hele dieren kan worden gebruikt. Als dat lukt, kan deze aanpak een krachtig instrument worden om te koppelen waar eiwitten zich bevinden, hoe ze bewegen en wat ze doen in gezondheid en ziekte, en kan het uiteindelijk bijdragen aan gedetailleerde computermodellen van cellulair gedrag.
Bronvermelding: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
Trefwoorden: eiwit conformationele dynamiek, beeldvorming in levende cellen, fluorescerende biosensoren, HaloTag-probes, botulinetoxine