Clear Sky Science · nl
Gereduceerd verbruik van monstermateriaal voor tijdsresolvede seriële kristallografie toegepast op de redoxcyclus van humane NQO1
Enzymen in actie kijken met veel minder kostbaar materiaal
Moderne biologie vertrouwt vaak op krachtige röntgenlasers om te zien hoe de moleculen van het leven bewegen en van vorm veranderen, maar deze experimenten verbruiken normaal gesproken enorme hoeveelheden zorgvuldig bereid eiwit. Deze studie introduceert een nieuwe manier om piepkleine eiwits kristallen veel efficiënter naar een X-ray vrije-elektronenlaser te “voeden”, waardoor de benodigde hoeveelheid materiaal met wel 97% kan afnemen. Ze toont ook aan dat deze zuinigere methode toch vroege stappen in de activiteit van een medisch relevant humaan enzym kan vastleggen, wat de deur opent naar routinematiger ‘films’ van eiwitten in actie. 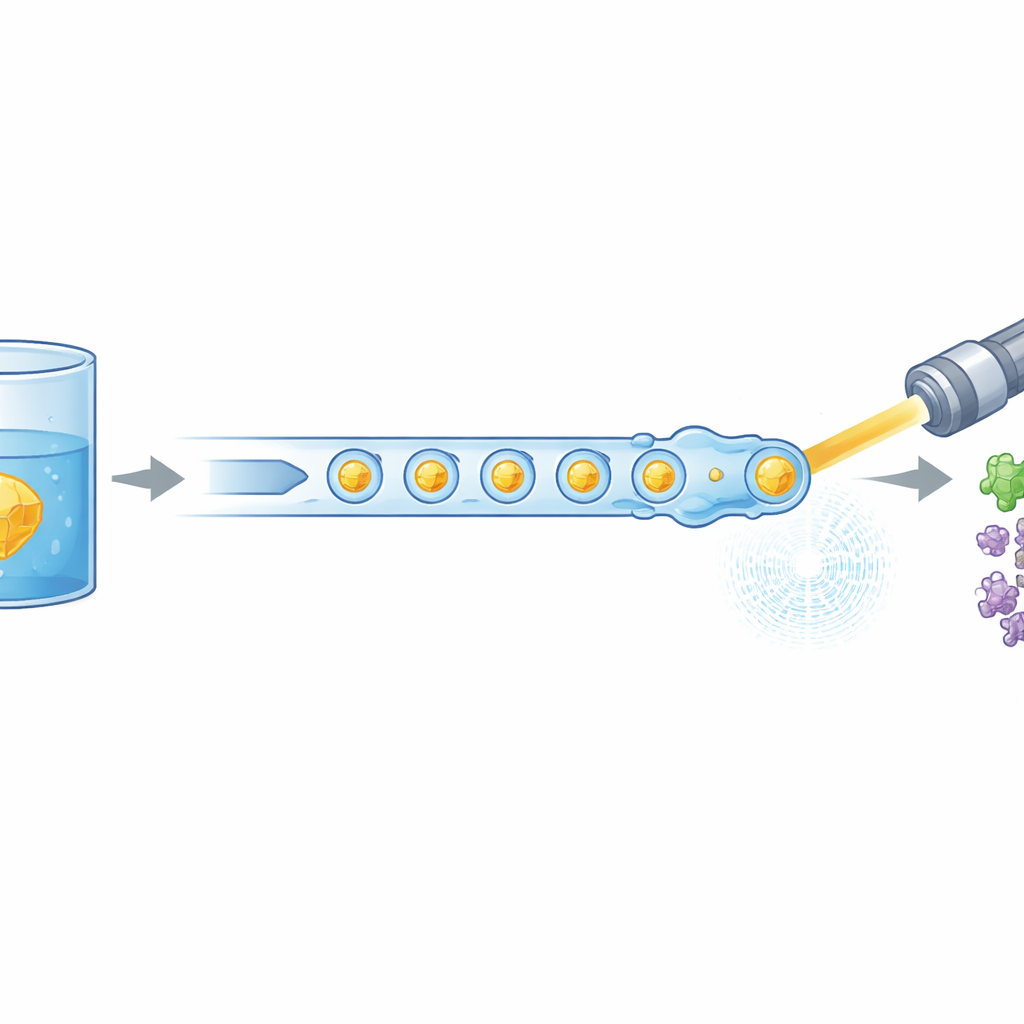
Waarom moleculaire films zo duur zijn
Om te begrijpen hoe eiwitten hun werk echt doen, stappen wetenschappers steeds vaker over van statische momentopnamen naar timelapse-“films” die reacties in real time volgen. Een toonaangevende aanpak, tijdsresolvede seriële kristallografie, verstuift miljoenen microscopische eiwitkristallen door een extreem heldere röntgenbundel. Elk kristal wordt slechts één keer geraakt, waardoor men een schadevrije blik op de structuur krijgt, en duizenden van zulke beelden worden gecombineerd tot het volledige plaatje. Het probleem is dat elk moment tijdens een reactie—tienden van een seconde, een volle seconde, enzovoort—een verse partij kristallen vereist. Omdat eiwitbereiding langzaam en duur kan zijn, is monsterverbruik een grote bottleneck geworden, vooral bij geavanceerde faciliteiten zoals de European XFEL, waar röntgenpulsen in snelle treinen met megahertz-snelheden aankomen.
Een nieuwe manier om piepkleine druppels op het juiste moment aan te leveren
De onderzoekers pakten dit probleem aan door de manier waarop kristallen naar de röntgenbundel worden gebracht opnieuw te ontwerpen. In plaats van een continue vloeistofstroom genereren ze een nauwkeurig gescheiden trein van microscopische druppels, elk met eiwitkristallen, gescheiden door een olie-fase. Een miniatuur 3D-geprint apparaat combineert twee stromen—eiwitkristallen en een opgeloste reactiedeelnemer—tot kleine gemengde volumes, die vervolgens worden afgesnoerd tot druppels. Deze druppels worden geleid door een gasgefokusseerde nozzle die een smalle straal vormt die compatibel is met het vacuüm en de snelheid van de XFEL. Cruciaal is dat de druppelproductie elektrisch wordt gesynchroniseerd met de timing van de röntgenpulse-treinen, zodat bijna elke bruikbare puls een druppel raakt in plaats van lege vloeistof.
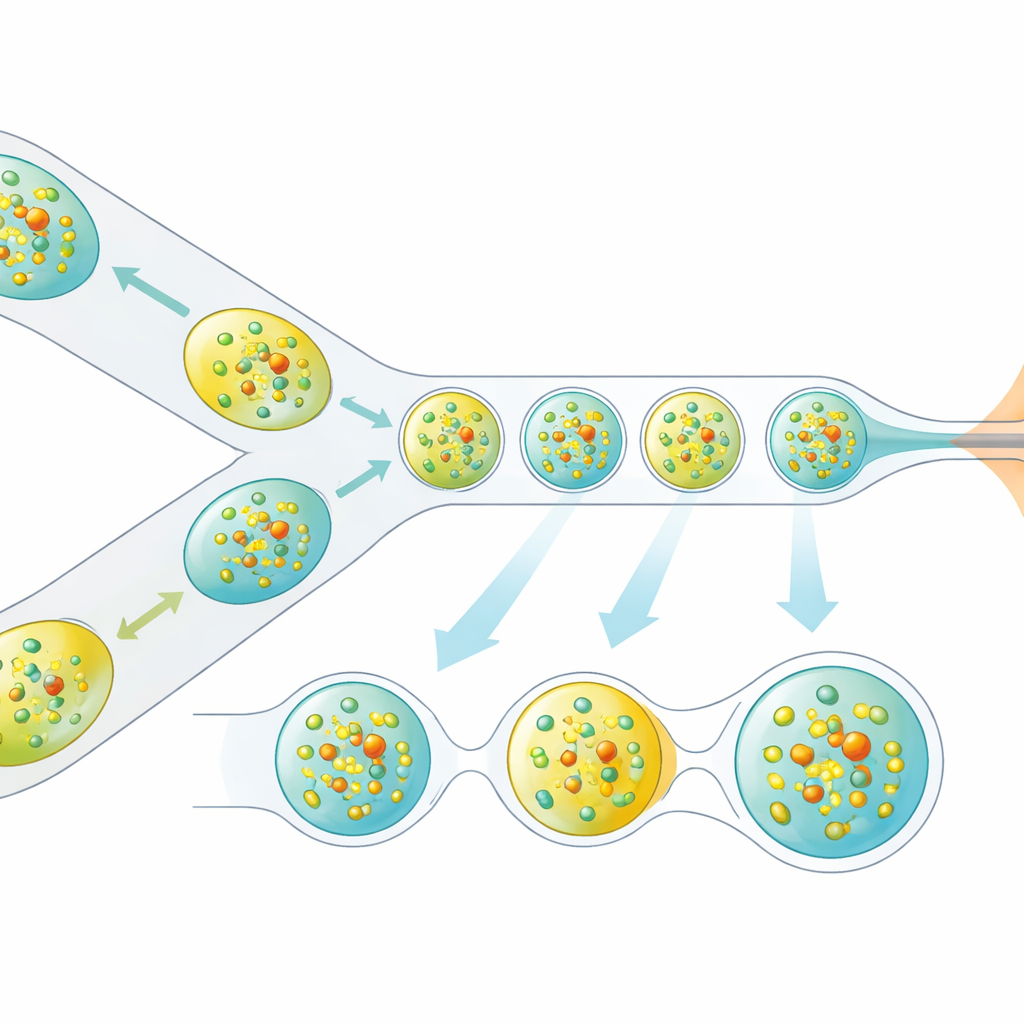
De methode testen met een humaan enzym
Om aan te tonen dat deze druppelgebaseerde aanpak werkt voor echte biologische vragen, bestudeerde het team NAD(P)H:chinon oxidoreductase 1 (NQO1), een humaan enzym dat betrokken is bij het beheer van de redoxbalans in de cel en gekoppeld is aan ziekte. Ze mengden microkristallen van NQO1 met zijn natuurlijke cofactor, NADH, en onderzochten het systeem op twee vroege tijdstippen: 0,3 seconden en 1,2 seconden na het mengen. Door de resulterende röntgendiffractiepatronen te analyseren, reconstrupeerden ze driedimensionale structuren van het enzym voor elke vertraging. Ondanks dat ze veel minder eiwit gebruikten dan conventionele continue-stroomexperimenten, was de datakwaliteit voldoende om subtiele elektrondichtheidskenmerken in de actieve centra van het enzym te onthullen, in lijn met NADH-moleculen die beginnen te binden met lage bezetting.
Wat de vroege structurele momentopnamen onthullen
De structuren tonen dat kort na het mengen niet alle actieve centra in het kristal hetzelfde gedrag vertonen. Bij 0,3 seconden duiden signalen voor NADH duidelijk aanwezig te zijn in drie van de vier actieve centra in de eenheidscel, en vaak in meer dan één conformatie, wat suggereert dat de cofactor meerdere posities verkent voordat hij zich settelt. Na 1,2 seconden verscherpen sommige van deze kenmerken tot een dominante bindingsmodus, maar het algemene beeld blijft dat van een flexibele en slechts gedeeltelijk bezette interactie. Dit ongelijkmatige, verschuivende gedrag komt overeen met eerder biochemisch bewijs dat NQO1’s twee partner-eenheden in een dimer niet perfect synchroon werken, maar eerder een ‘half-of-the-sites’-activiteit vertonen, waarbij de ene kant eerst engageert terwijl de andere achterblijft. De tijdsresolvede gegevens bieden daarmee een vroege structurele inkijk in hoe deze asymmetrie zich in de ruimte afspeelt.
Monster besparen zonder in te leveren op wetenschap
Praktisch gezien verkleinde de gesegmenteerde druppelmethode het eiwitverbruik met ongeveer een factor zes voor de 0,3-secondenmetingen en tot 97% voor de 1,2-secondenexperimenten, vergeleken met traditionele continue jets onder vergelijkbare omstandigheden. Toch leverde het betrouwbare structurele informatie bij kamertemperatuur, compatibel met de veeleisende pulsstructuur van de European XFEL. Voor niet-specialisten is de kernboodschap dat onderzoekers nu enzymen zoals NQO1 bijna in real time kunnen zien beginnen met hun werk, terwijl ze slechts milligrammen van kostbaar materiaal per tijdpunt gebruiken. Dit maakt het veel realistischer om veel reactietijden en veel verschillende eiwitten te onderzoeken, en helpt uiteindelijk te onthullen hoe medisch belangrijke enzymen bewegen, buigen en samenwerken terwijl ze de chemie van het leven uitvoeren.
Bronvermelding: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
Trefwoorden: seriële kristallografie, X-ray vrije-elektronenlaser, druppel-microfluidica, enzymdynamica, NQO1