Clear Sky Science · nl
Oncogene PI3Kα-varianten onthullen gegradueerd conformationeel spectrum met mutatie-specifieke cryptische pockets
Wanneer één DNA-verandering niet genoeg is
Kanker wordt vaak omschreven als een ziekte van mutaties, maar deze studie laat zien dat niet alle mutaties op zichzelf werken. De onderzoekers bestudeerden een sleutelenzym voor groeiregulatie, PI3Kα, en vonden dat wanneer twee specifieke DNA-veranderingen samen in hetzelfde exemplaar van het gen voorkomen, ze dit eiwit in veel actievere vormen kunnen brengen dan een van beide veranderingen alleen. Dat is belangrijk omdat overactieve PI3Kα niet alleen kanker aanstuurt, maar ook betrokken is bij goedaardige overgroei-syndromen en ontwikkelingsstoornissen van de hersenen — en het helpt verklaren waarom sommige tumoren slecht reageren op huidige medicijnen.
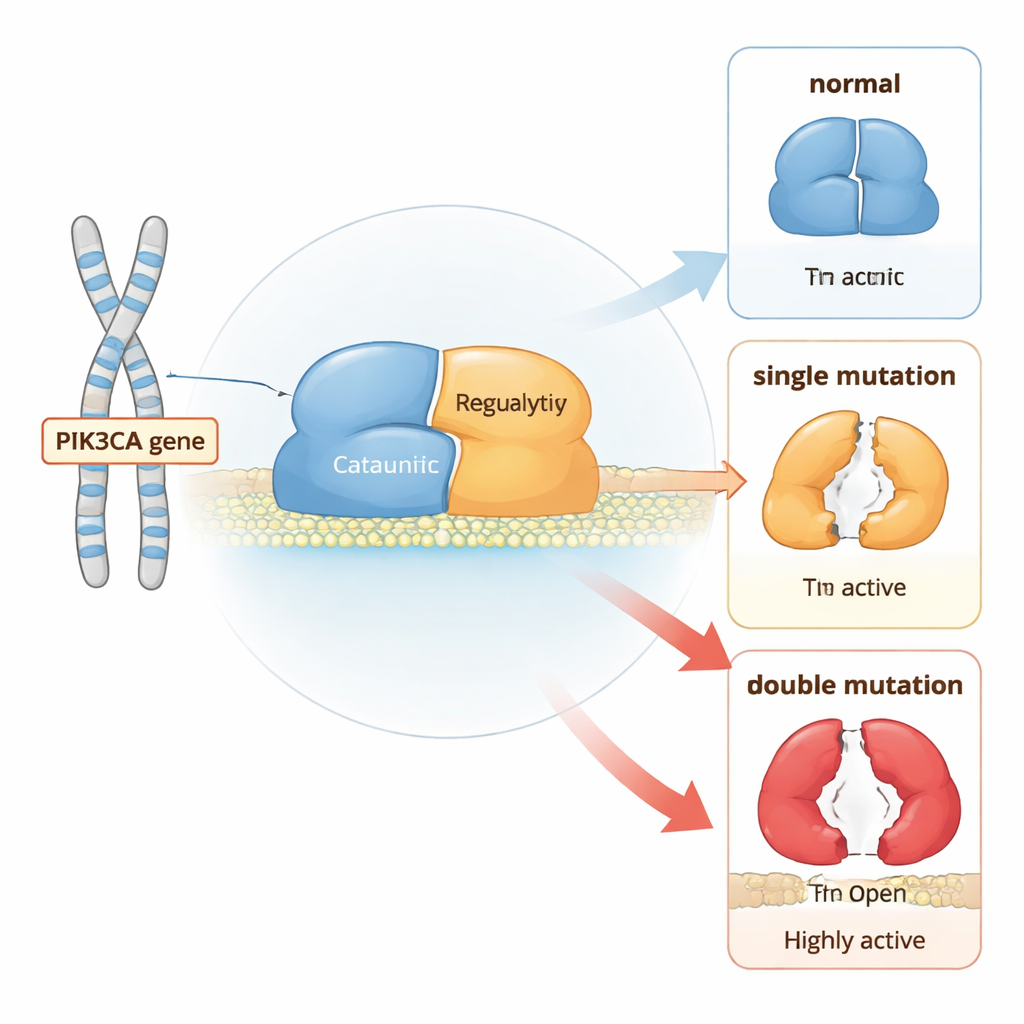
Een moleculaire schakelaar voor celgroei
PI3Kα is een eiwit met twee delen dat vlak bij het celmembraan zit en groeisignalen doorgeeft. Onder normale omstandigheden staat het grotendeels in een „uit”‑stand totdat receptoren op het celoppervlak geactiveerd worden. Vervolgens beweegt PI3Kα naar het membraan en zet een lipide genaamd PIP2 om in PIP3, dat de cel aanzet tot groeien en delen. Om ongecontroleerde groei te voorkomen, werken verschillende delen van het eiwit als ingebouwde remmen: één regio klemt de katalytische kern vast, een andere houdt een flexibele activatielus dicht bij, en een partner-subunit helpt het hele complex onder controle te houden.
Hoe enkele en dubbele mutaties het evenwicht verschuiven
Met behulp van lange, atomaire computersimulaties vergeleken de auteurs normale PI3Kα met varianten die ofwel enkele „hotspot” kankermutaties droegen of combinaties van een hotspot met een zwakkere mutatie in hetzelfde molecuul. Ze ontdekten dat elke mutatie verandert hoe vaak het eiwit meer open, actieve vormen bezoekt, maar dubbele mutanten duwen het evenwicht veel verder dan enkele. In het bijzonder werken sommige mutatieparen samen om de contacten losser te maken die een regulerend stukje (genoemd nSH2) op zijn plaats houden en om een ander segment (iSH2) van zijn dokplaats weg te schuiven. Deze gecoördineerde beweging ontgrendelt de katalytische kern, waardoor het voor het eiwit gemakkelijker wordt naar het membraan te bewegen en signalen te starten.
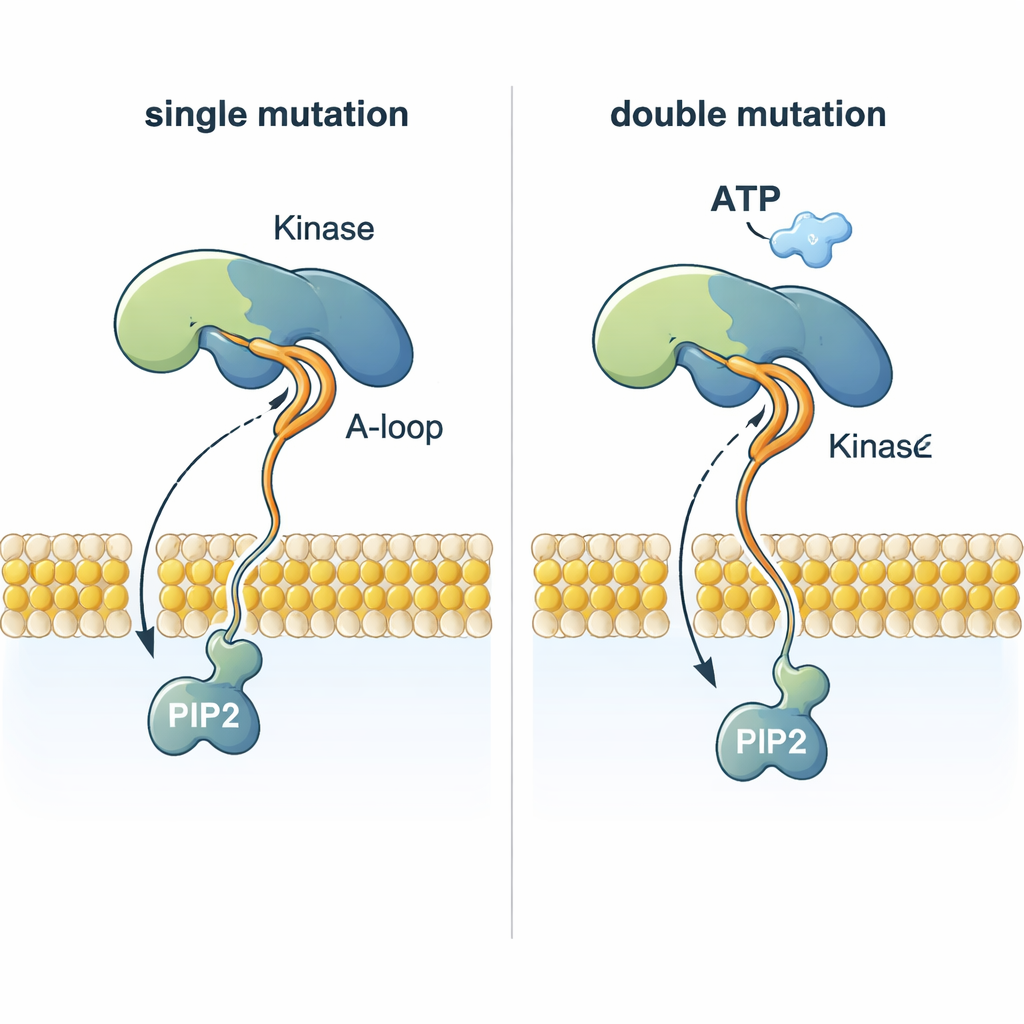
Helpen dat het substraat de reactielocatie bereikt
Een opvallend raadsel is hoe PI3Kα een fosfaatgroep van ATP — dat bijna 2 nanometer boven het membraan ligt — kan overbrengen op PIP2, dat in het membraan is ingebed. De simulaties tonen dat bepaalde mutaties een flexibele activatielus zodanig hervormen dat een sterk positief geladen streek naar het membraan uitsteekt. Deze lus kan de negatief geladen kop van PIP2 grijpen, uit de lipidelaag trekken en naar ATP geleiden. Dubbele mutanten die een membraanankerende mutatie combineren met een mutatie die deze lus verandert, coördineren PIP2 veel efficiënter dan normale PI3Kα of enkele mutanten, wat een structurele verklaring biedt waarom tumoren met twee PI3Kα-mutaties bijzonder agressief kunnen zijn.
Verborgen geneesmiddellocaties onthuld door beweging
Omdat PI3Kα groot en flexibel is, worstelt een enkel geneesmiddel dat gericht is op de actieve plaats vaak om effectief te zijn tegen alle mutante vormen en kan het bijwerkingen veroorzaken, zoals ernstige veranderingen in de bloedsuikerspiegel. Door te volgen hoe het eiwit over tijd ademt en buigt, ontdekten de onderzoekers „cryptische” pockets — tijdelijke groeven die alleen in bepaalde mutante vormen opengaan en onzichtbaar zijn in statische kristalstructuren. Deze pockets verschijnen op mutatie‑specifieke locaties, bijvoorbeeld nabij regio’s die het sterkst bewegen in bepaalde dubbele mutanten. Dat suggereert dat zorgvuldig ontworpen allosterische medicijnen, die binden weg van de actieve plaats, kunnen worden afgestemd om individuele mutante varianten terug te vergrendelen in veiligere, minder actieve conformaties.
Op weg naar slimmer combinatiebehandelingen
Samenvattend ondersteunt dit werk een „one-two punch” kijk op de genetica van kanker: een sterke hotspotmutatie plus een zwakkere partner in hetzelfde PI3Kα-molecuul kan een gegradueerd spectrum van actievere vormen creëren, vaak gekoppeld aan ernstigere klinische uitkomsten. Voor therapie bepleiten de auteurs dat het, in plaats van te vertrouwen op één enkele remmer, effectiever kan zijn geneesmiddelen te combineren die verschillende pockets targeten — één in de actieve plaats en één of meer allosterische plaatsen die alleen in specifieke mutanten bestaan. Zulke cocktails zouden in principe de PI3Kα-activiteit preciezer kunnen verlagen, toxische bijwerkingen verminderen en de behandeling beter afstemmen op het exacte mutatiepatroon in de tumor van een patiënt.
Bronvermelding: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Trefwoorden: PI3K alpha, oncogene mutaties, allosterische remmers, moleculaire dynamica, signaaltransductie