Clear Sky Science · nl
Dynamica van CO-foto-oxidatie naar CO2 op rutiel (110)
Waarom het belangrijk is om moleculen in een biljoenste van een seconde te volgen
Het moderne leven is afhankelijk van chemische reacties die onze lucht en ons water reinigen en zonlicht omzetten in bruikbare energie. Veel van deze reacties vinden plaats op de oppervlakken van vaste materialen die fotokatalysatoren worden genoemd en aangedreven worden door licht. Deze studie kijkt naar een van die reacties — hoe het giftige koolmonoxide (CO) op een titaniumdioxide-oppervlak wordt omgezet in kooldioxide (CO2) — op tijdschalen van slechts biljardsten van een seconde. Inzicht in deze ultrasnelle stappen kan wetenschappers helpen slimmere materialen te ontwerpen voor vervuilingsbestrijding, zelfreinigende oppervlakken en zonne-energietechnologieën.
Een door licht aangestuurde opruimploeg
Titaniumdioxide is een veelzijdig materiaal dat voorkomt in zelfreinigende ramen, luchtzuiverende coatings en experimentele systemen voor zonnebrandstoffen. Het is goedkoop, stabiel en kan licht gebruiken om krachtige reinigingsreacties op het oppervlak te activeren. Maar niet alle vormen van titaniumdioxide gedragen zich gelijk. Twee veelvoorkomende vormen, anatase en rutiel, verschillen in hoe efficiënt ze reacties aandrijven zoals de omzetting van CO in CO2. Terwijl anatase over het algemeen actiever is, bleef de gedetailleerde timing van de individuele reactiestappen — vooral hoe zuurstof uit de lucht geactiveerd wordt — onduidelijk. Deze studie richt zich op de rutielvorm met een specifieke oppervlakteoriëntatie, bekend als (110), om precies te zien hoe snel CO wordt geoxideerd zodra licht het materiaal raakt.
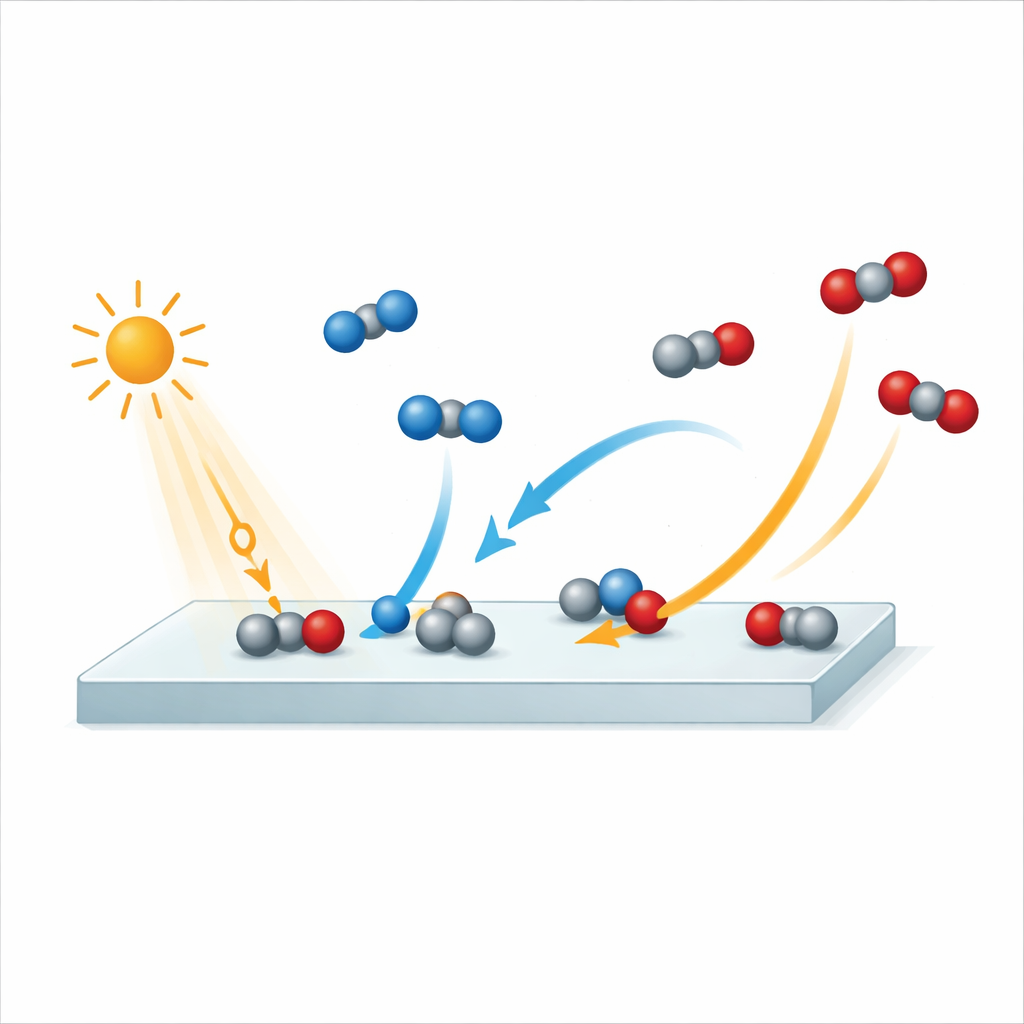
Een reactie filmen met extreem hoge snelheid
Om dit proces vast te leggen gebruikten de onderzoekers een free-electron laserfaciliteit in Hamburg die extreem korte röntgenflitsen produceert. Eerst raakten ze het rutieloppervlak met een infraroodlichtpuls, die fungeerde als een klein cameraflitsje dat de reactie startte. Een zorgvuldig getimede röntgenpuls onderzocht vervolgens hoe de atomen en elektronen op het oppervlak veranderden. Door deze volgorde te herhalen met verschillende vertragingen tussen de licht- en röntgenpulsen, bouwden ze als het ware een "moleculaire film" van de reactie op met een tijdresolutie van ongeveer 250 femtoseconden — een femtoseconde is een miljoenste van een miljardste van een seconde. Het team volgde signalen van zuurstofatomen op het oppervlak en in de gasmoleculen, waardoor ze CO, CO2, water en het oxide zelf konden onderscheiden terwijl de reactie verliep.
CO2 vangen in minder dan een biljoenste van een seconde
De belangrijkste waarneming is dat nieuw gevormde CO2 op het rutieloppervlak verschijnt binnen slechts 200 tot 800 femtoseconden na de lichtpuls. Dat betekent dat zuurstof van nabijgelegen O2-moleculen wordt geactiveerd, bindingen worden verbroken en CO wordt omgezet in CO2 in minder dan één biljoenste van een seconde. Na ongeveer 0,8 picoseconde vervaagt het verse CO2-signaal wanneer het product van het oppervlak desorbeert. Opmerkelijk genoeg verloopt deze hele sequentie sneller op rutiel dan op anatase, waar eerder werk aantoonde dat het eerste CO2 pas na ongeveer 1,2 tot 2,8 picoseconden verscheen onder verder vergelijkbare condities. Hoewel anatase uiteindelijk meer CO2 produceert en als de sterkere fotokatalysator wordt beschouwd, voert rutiel de cruciale oxidatiestap sneller uit.
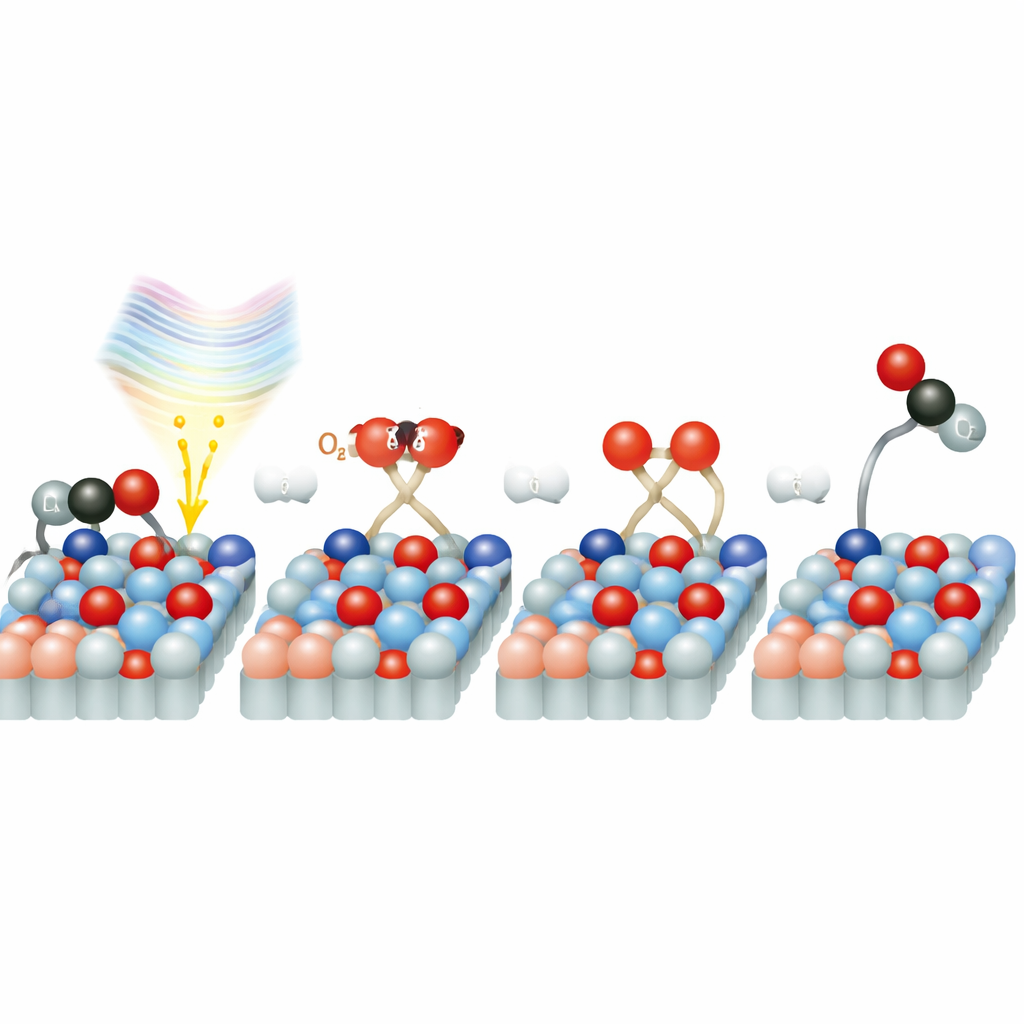
Een verkorte route voor zuurstof
Waarom is de reactie zo snel op rutiel? Gedetailleerde computersimulaties suggereren dat zuurstofmoleculen die op het oppervlak zitten speciale elektronische toestanden creëren die als een brug fungeren tussen het vaste materiaal en de O2. Wanneer het 770-nanometer laserlicht wordt geabsorbeerd, kan het direct een elektron van het titaniumdioxide naar het zuurstofmolecuul verplaatsen, waardoor een geladen, geactiveerde zuurstofsoort ontstaat. Deze "kortsluiting" vermijdt de tragere route waarbij elektronen eerst door het bulkmateriaal reizen en vervolgens naar het oppervlak driften. Eenmaal geactiveerd splitst de zuurstof snel en combineert een zuurstofatoom met CO om CO2 te vormen. De studie toont ook aan dat sporen van water op het oppervlak zowel reactielocaties kunnen blokkeren als, in lage concentraties, mogelijk kunnen helpen bij deze ladingsoverdracht en zuurstofactivatie, wat een extra complexiteitslaag toevoegt.
Elektronische structuur koppelen aan prestaties in de praktijk
Al met al laat het werk zien dat kleine details in hoe elektronen bewegen tussen een oppervlak en nabije moleculen de reactiesnelheden dramatisch kunnen veranderen, zelfs tussen twee nauw verwante materialen. Hoewel anatase nog steeds de voorkeur heeft qua totale fotokatalytische opbrengst, toont rutiel een snellere zuurstofactivatiestap die gekoppeld is aan deze speciale ladingsoverdrachtsroute. Door ultrasnelle metingen te combineren met geavanceerde simulaties, biedt de studie een routekaart voor het afstemmen van oppervlakken zodat lichtgestuurde reacties efficiënter verlopen. Op de lange termijn kunnen dergelijke inzichten ingenieurs helpen betere coatings voor luchtzuivering, effectievere antibacteriële oppervlakken en verbeterde materialen voor zon-aangedreven brandstofproductie en waterstofsplitsing te ontwerpen.
Bronvermelding: Gleissner, H., Wagstaffe, M., Wenthaus, L. et al. Dynamics of CO photooxidation to CO2 on rutile (110). Commun Chem 9, 127 (2026). https://doi.org/10.1038/s42004-026-01901-2
Trefwoorden: fotokatalyse, titaniumdioxide, ultrasnelle spectroscopie, oppervlaktechemie, oxidatie van koolmonoxide