Clear Sky Science · nl
Ontwikkeling van een viervoudig-geconjugeerd carbon dot nanomodel voor gerichte glioma-therapie
Nieuwe hoop voor hardnekkige hersentumoren
Hogegradige hersentumoren zoals glioblastoom behoren tot de moeilijkst te behandelen vormen van kanker. Veel geneesmiddelen die elders in het lichaam werken, kunnen ofwel de beschermende bloed-hersenbarrière niet passeren of beschadigen langs de weg gezond weefsel. Deze studie beschrijft een in het laboratorium vervaardigde "slimme" nanopartikel dat erop gericht is nauwkeuriger in hersentumoren te glippen, een krachtig medicijnmix te vervoeren en het direct vrij te geven in de kernen van tumorcellen, waar het het meeste schade aan kanker kan toebrengen terwijl normale cellen gespaard blijven.
Een klein vervoersfabriekje gemaakt van koolstof
Centraal in de nieuwe benadering staan carbon dots—nanometergrote deeltjes gemaakt van koolstof die goedkoop te produceren zijn, goed mengbaar met water en onder bepaalde lichtsoorten oplichten. Omdat hun oppervlakken rijk zijn aan chemische haakjes, kunnen ze tegelijk met meerdere biologische componenten worden voorzien. In dit werk creëerden de onderzoekers een "viervoudig-geconjugeerd" nanomodel: elke carbon dot werd chemisch gekoppeld, in één enkele one-pot reactie, aan twee verschillende targetende peptiden en twee anticancermiddelen. Dit modulaire ontwerp verandert elke dot in een klein vrachtauto‑achtige drager die tumorcellen kan herkennen, door cellulaire barrières kan dringen en medicijnen naar het juiste intracellulaire adres kan brengen.
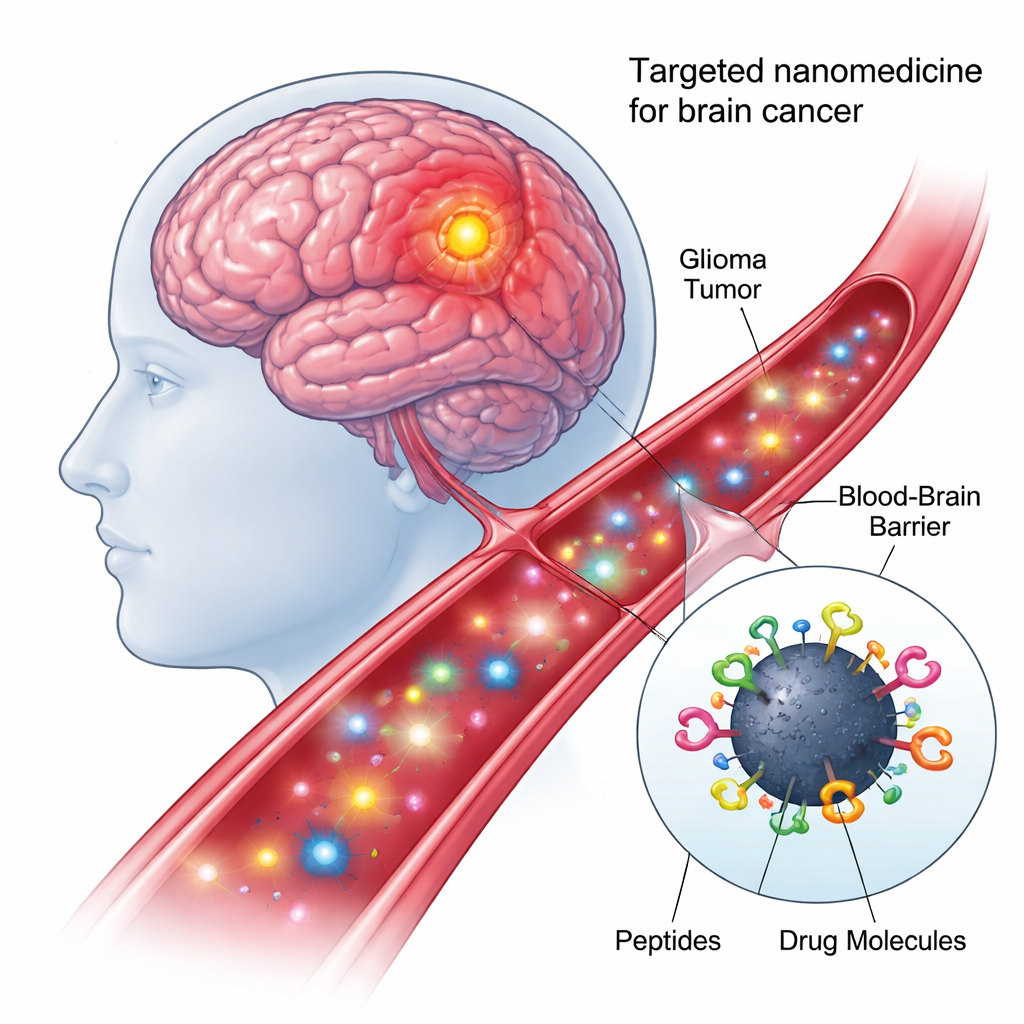
De juiste hersencellen vinden en binnendringen
Het eerste peptide op het nanopartikel, shPep-1 genoemd, is ontworpen om een receptor genaamd IL13Rα2 te herkennen. Deze receptor komt in hoge mate voor op veel agressieve hersentumoren—waaronder volwassen en pediatrisch glioblastoom en diffuse intrinsieke pontiene glioma—but blijkt alleen zwak aanwezig op normale hersencellen. Door aan IL13Rα2 te binden, helpt shPep-1 de carbon dots zich op tumorcellen te richten en deze binnen te dringen via receptormedieerde opname. Het tweede, langere peptide, lnPep-1, bevat een nucleaire lokalisatiesignaal: een korte sequentie die helpt de lading door het kernmembraan te laten glippen en het controlecentrum van de cel, waar het DNA ligt, te bereiken. Samen geven deze twee peptiden het nanopartikel zowel tumorpreferentie als het vermogen om eenmaal binnen de kern te bereiken.
Het leveren van een gecoördineerde medicijnaanval
De therapeutische lading bestaat uit twee kleine moleculen. De eerste is epirubicine, een bekend chemotherapeuticum dat kankercellen doodt door zich in DNA te inserteren en enzymen te blokkeren die nodig zijn voor het repareren van dubbelstrengsbreuken. De tweede is een metaboliet genaamd 5‑aminoimidazol-4‑carboxamide (AIC), geproduceerd uit het hersentumorgeneesmiddel temozolomide bij fysiologische pH. In eerder werk toonde dezelfde groep aan dat het combineren van epirubicine en AIC op een carbon dot het doden van kankercellen versterkte vergeleken met elk geneesmiddel afzonderlijk. In het nieuwe ontwerp worden beide tegelijk afgeleverd op het dual‑peptide nanopartikel, met het doel een synergistisch effect direct in de celkern van de tumorcel te bereiken.
Krachtig in tumoren, milder voor normale cellen
Om te testen hoe goed het nanomodel werkte, stelde het team meerdere hogegradige glioma-cel lijnen bloot—volwassen glioblastoom, pediatrisch glioblastoom en een model voor diffuse intrinsieke pontiene glioma—aan de viervoudig-geconjugeerde carbon dots. Zelfs bij zeer lage concentraties (zo weinig als 50 nanomolair) daalde de levensvatbaarheid van tumorcellen tot ongeveer de helft van de onbehandelde controles, en bij hogere doses doodden alle geteste geconjugeerden de meeste tumorcellen. Belangrijk is dat het viervoudige nanomodel beter presteerde dan eenvoudigere "single-peptide" versies, ondanks dat het in totaal minder epirubicine droeg. Getest op niet-kankerachtige vasculaire gladde spiercellen was het veel minder toxisch: deze cellen vereisten ruwweg 25–40 keer meer nanopartikel om een vergelijkbaar verlies aan levensvatbaarheid te zien, wat wijst op een bruikbare veiligheidsmarge aangedreven door tumortargeting in plaats van brute force dosering.
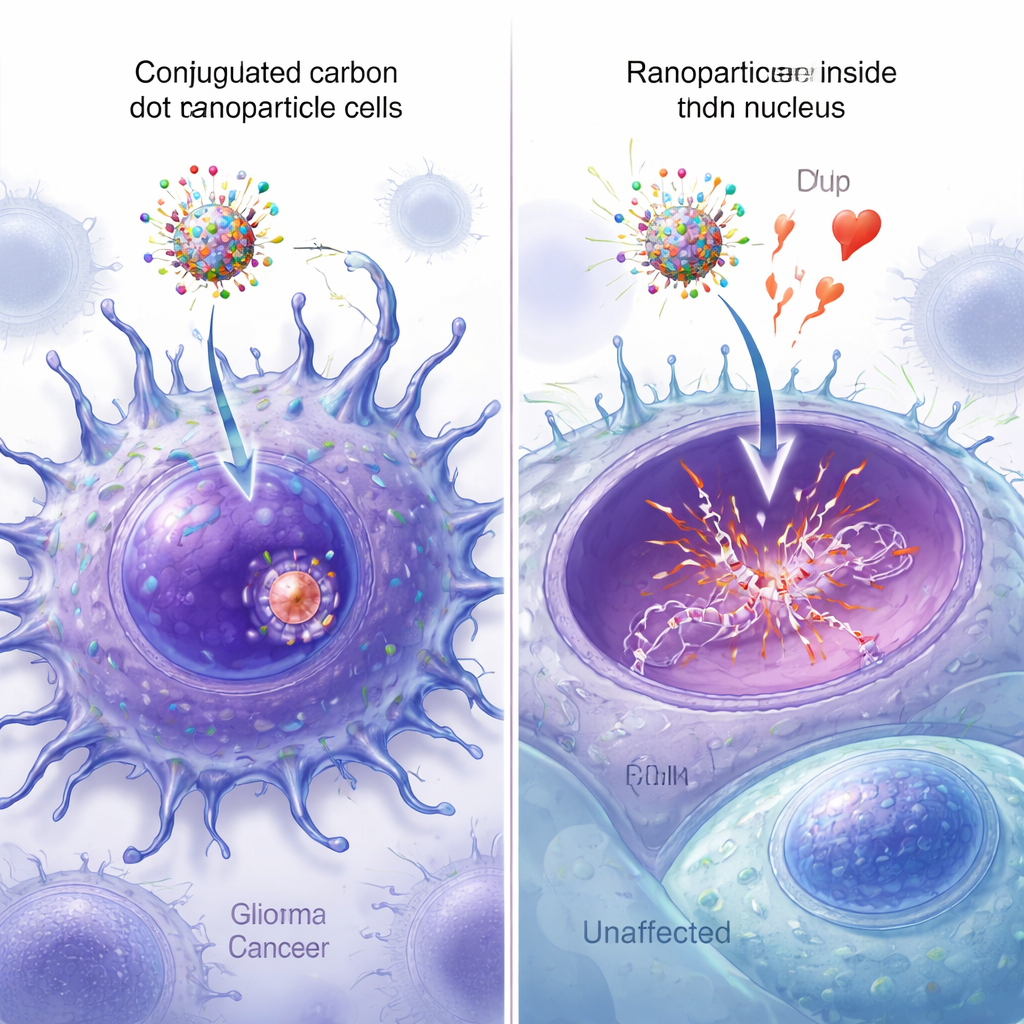
Zien dat de nanopartikels de kern bereiken
Fluorescerende versies van de nanopartikels stelden de onderzoekers in staat te observeren hoe goed elk ontwerp cellen binnenging en de kern bereikte. Onder de microscoop toonden carbon dots uitgerust met beide peptiden het helderste signaal verspreid door de kankercellen, met sterke overlap tussen de groene nanopartikelfluorescentie en de blauwe kernkleuring. Kwantitatieve beeldanalyse bevestigde dat de dual‑peptide deeltjes de hoogste nucleaire colocalisatie hadden, aanzienlijk meer dan de deeltjes die slechts één peptide of geen peptide droegen. Aanvullende spectroscopie-, massaspectrometrie- en atomic force microscopy-metingen bevestigden dat alle vier componenten succesvol aan de carbon dots waren bevestigd en hun grootte licht vergrootten, zonder de belangrijke DNA-bindende functie van epirubicine te verstoren.
Wat dit zou kunnen betekenen voor toekomstige zorg bij hersenkanker
Voor patiënten zijn deze bevindingen nog een vroege, petrischaal-demo en geen directe therapie. Toch laten ze een veelbelovend concept zien: een klein, stabiel en relatief eenvoudig te maken koolstofgebaseerd nanopartikel dat snel kan worden aangepast met targetende peptiden en medicijncombinaties. Door geneesmiddelen specifiek naar tumorcellen die IL13Rα2 overproduceren te sturen en ze in de kern te concentreren, zouden dergelijke nanomedicijnen op termijn lagere doses, minder bijwerkingen en meer gepersonaliseerde behandelstrategieën mogelijk kunnen maken voor sterk dodelijke hersentumoren zoals glioblastoom en diffuse intrinsieke pontiene glioma.
Bronvermelding: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Trefwoorden: glioblastoom, nanotherapie, carbon dots, gerichte medicijnafgifte, hersen tumoren