Clear Sky Science · nl
Het verfijnen van AlphaFold met beperkte cryo-EM-waarnemingen
Waarom eiwitvormen zo moeilijk te zien zijn
Eiwitten zijn kleine moleculaire machines die vrijwel elk proces in ons lichaam aandrijven, van energieproductie tot zenuwimpulsen. Om te begrijpen hoe ze werken — en hoe medicijnen ze kunnen beïnvloeden — moeten wetenschappers hun precieze driedimensionale vormen kennen. Twee krachtige hulpmiddelen zijn hiervoor naar voren gekomen: cryo‑elektronenmicroscopie (cryo‑EM), die veel vage momentopnames maakt van bevroren eiwitten, en AlphaFold, een kunstmatig‑intelligentiesysteem dat eiwitstructuren uit aminozuurvolgordes voorspelt. In veel echte experimenten zijn de cryo‑EM‑gegevens echter onvolledig en komen AlphaFold‑voorspellingen niet altijd overeen met de werkelijkheid. Dit artikel introduceert CoCoFold, een methode die AlphaFold leert rechtstreeks naar moeilijke cryo‑EM‑gegevens te luisteren en zijn voorspellingen dienovereenkomstig te verbeteren.
Wanneer de camera te weinig ziet
Cryo‑EM werkt door eiwitten snel in te vriezen en enorme aantallen individuele deeltjes vanuit vele hoeken te fotograferen, en die beelden vervolgens te combineren tot een 3D‑kaart. In de praktijk hebben onderzoekers echter vaak niet genoeg goede beelden om mee te werken. Soms verschijnt het eiwit slechts kortstondig in een hoge‑energie‑toestand, waardoor maar weinig deeltjes worden vastgelegd. In andere gevallen nemen eiwitten op het ijsoppervlak de voorkeur aan bepaalde oriëntaties, waardoor veel aanzichten ontbreken. Beide problemen leiden tot vage, onvolledige kaarten die moeilijk te vertalen zijn naar betrouwbare atomaire modellen. Bestaande software kan AlphaFold‑voorspelde structuren in zulke kaarten passen, maar het succes hangt sterk af van het hebben van scherpe, hoge‑resolutiegegevens vanaf het begin.
AlphaFold leren uit ruwe beelden
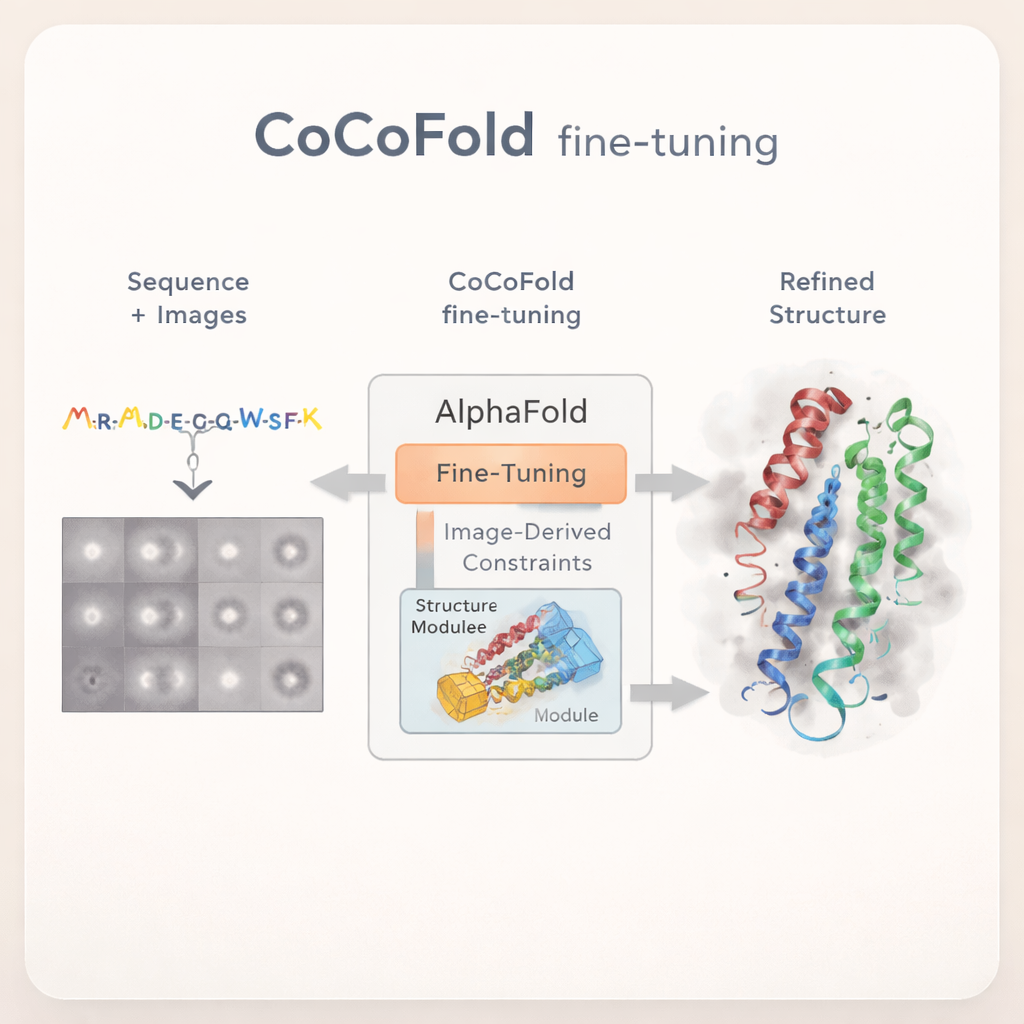
CoCoFold kiest een andere aanpak: in plaats van te vertrouwen op een volledig gereconstrueerde 3D‑cryo‑EM‑kaart, gebruikt het direct de ruwe 2D‑deeltjesbeelden om AlphaFold fijn af te stemmen. De methode begint met een AlphaFold‑Multimer‑voorspelling en houdt het grootste deel van het originele netwerk bevroren, waarmee de brede kennis over eiwitvouwing behouden blijft. Alleen het laatste structuurbouwende deel mag veranderen. Een lichtgewicht "adapter" wordt toegevoegd om informatie afgeleid uit de cryo‑EM‑beelden naar deze structuurmodule te voeren, waarbij het model subtiel wordt bijgestuurd richting vormen die compatibel zijn met de experimentele gegevens, zonder grote afwijkingen van bekende eiwitfysica toe te staan.
Beelden omzetten in structurele terugkoppeling
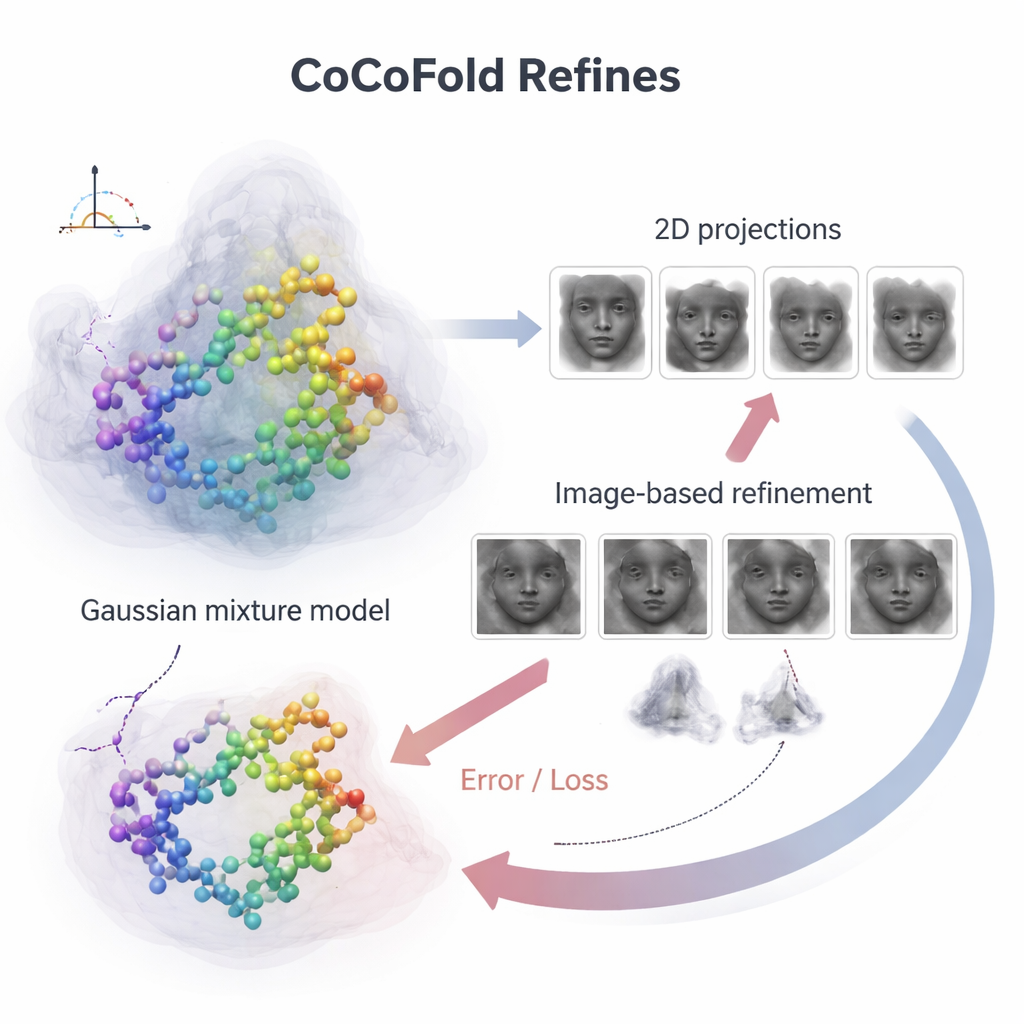
Om individuele eiwitatomen te koppelen aan de ruisige microscoopbeelden bouwt CoCoFold een glad, flexibel beeld van de voorspelde structuur met behulp van overlappende driedimensionale blobs, bekend als een Gaussische mengselrepresentatie. Vanuit deze weergave simuleert het hoe het eiwit er in de microscoop zou uitzien bij dezelfde kijkrichtingen en beeldcondities als het echte experiment. Deze gesimuleerde snapshots worden vervolgens vergeleken met de werkelijke cryo‑EM‑deeltjes, ring voor ring in het frequentiedomein, om te beoordelen hoe goed ze overeenkomen. Elke mismatch wordt een terugkoppelingssignaal dat door het netwerk terugstroomt en zowel het eiwitmodel als de dichtheidsrepresentatie lichtjes aanpast. Na het trainen wordt het atomaire model verder opgeschoond met een fysica‑gebaseerde verfijningsstap om lokale geometrische botsingen te verwijderen.
Accuraat blijven wanneer gegevens schaars of bevooroordeeld zijn
De auteurs testten CoCoFold op meerdere experimentele en gesimuleerde datasets die ontworpen zijn om de twee hoofdproblemen in cryo‑EM na te bootsen: te weinig deeltjes en grote gaten in kijkhoeken. Onder deze zware omstandigheden hadden standaardhulpmiddelen — inclusief andere deep‑learningmethoden die afhankelijk zijn van gereconstrueerde kaarten — de neiging om regio's van het eiwit te missen, helices verkeerd te plaatsen of fijne details te verliezen naarmate de kaarten vager werden. CoCoFold produceerde daarentegen consequent modellen die beter en vollediger overeenkwamen met bekende referentiestructuren. De fouten bleven klein, zelfs wanneer het aantal deeltjes drastisch werd teruggebracht of wanneer grote kegelvormige groepen kijkrichtingen ontbraken, wat suggereert dat direct leren van de ruwe beelden cruciale informatie behoudt die kaartgebaseerde benaderingen weggooien.
Wat dit betekent voor toekomstige structurele biologie
Voor niet‑specialisten is de kernboodschap dat CoCoFold fungeert als een vertaler tussen krachtige AI‑voorspellingen en onvolmaakte experimentele gegevens. In plaats van uitsluitend op AlphaFold of cryo‑EM te vertrouwen, laat het de twee elkaars inzichten aanvullen — vooral in de lastige situaties waarin experimenten slechts een gedeeltelijk beeld bieden. In eenvoudige gevallen met overvloedige, hoogwaardige data werken de bestaande kaartgestuurde hulpmiddelen nog steeds uitstekend. Maar wanneer deeltjes zeldzaam zijn of oriëntaties ontbreken — veelvoorkomende situaties bij het volgen van vluchtige of kwetsbare eiwittoestanden — biedt CoCoFold een manier om betrouwbare atomaire modellen te herstellen uit informatie die anders verloren zou gaan.
Bronvermelding: Liao, J., Zheng, D., Zhang, H. et al. Fine-tuning AlphaFold with limited cryo-EM observations. Commun Chem 9, 95 (2026). https://doi.org/10.1038/s42004-026-01899-7
Trefwoorden: cryo-EM, AlphaFold, eiwitstructuur, deep learning, structurele biologie