Clear Sky Science · nl
Een generaliseerbare test voor intracellulaire accumulatie om cytosolische medicijnafgifte in zoogdiercellen te profileren
Waarom het belangrijk is medicijnen in cellen te krijgen
Veel van de meest veelbelovende geneesmiddelen van vandaag — kleine medicijnmoleculen, korte eiwitfragmenten genaamd peptiden en volledige eiwitten — zijn ontworpen om te werken op doelwitten binnenin onze cellen. Maar het celmembraan fungeert als een strenge beveiligingspoort. Een middel kan aan de buitenkant van een cel blijven plakken of vast komen te zitten in interne blaasje‑achtige structuren genaamd endosomen en toch nooit het waterige binnenste, het cytosol, bereiken waar veel doelwitten wonen. Dit artikel beschrijft een nieuwe laboratoriumtest, de CHAMP‑assay, die onderzoekers niet alleen vertelt of een molecuul een cel binnenkomt, maar of het daadwerkelijk in het cytosol arriveert, waar het zijn werk kan doen.
Een nieuwe manier om medicijntoegang te volgen
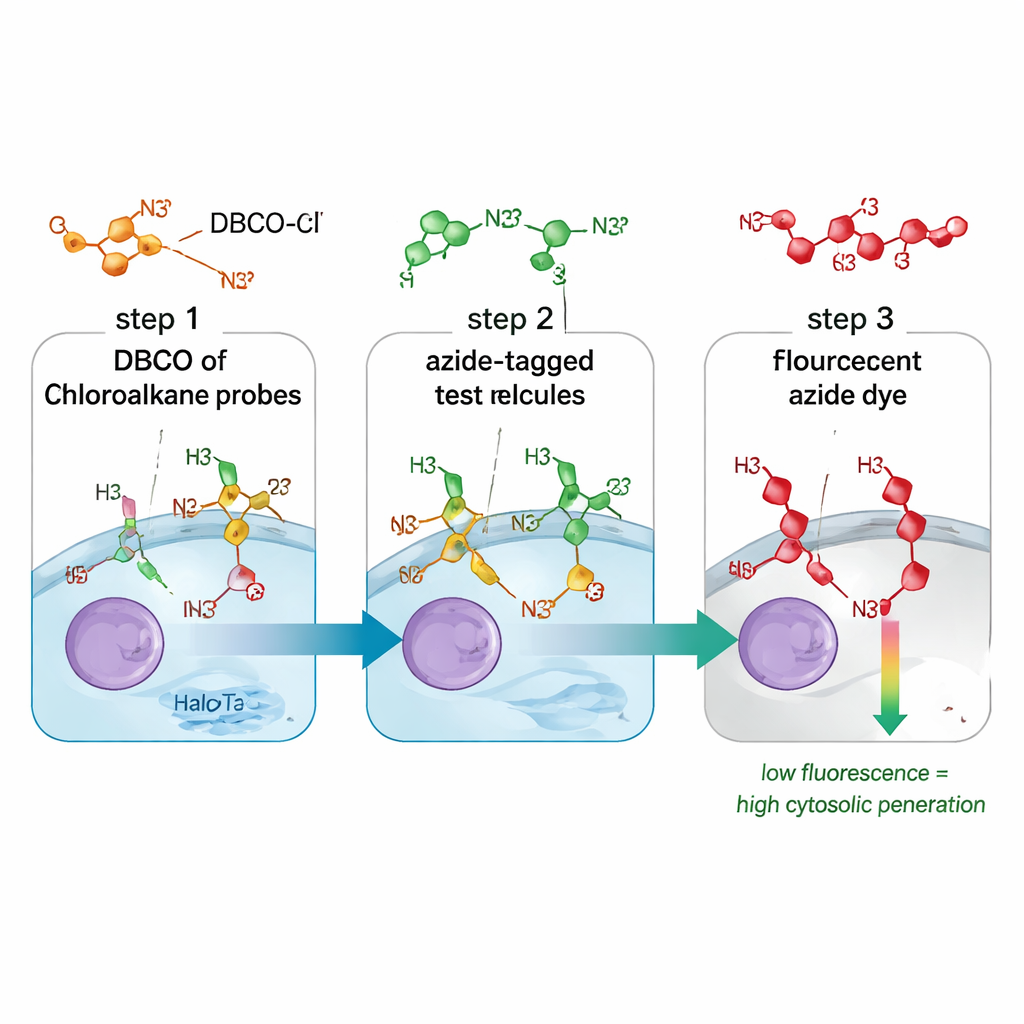
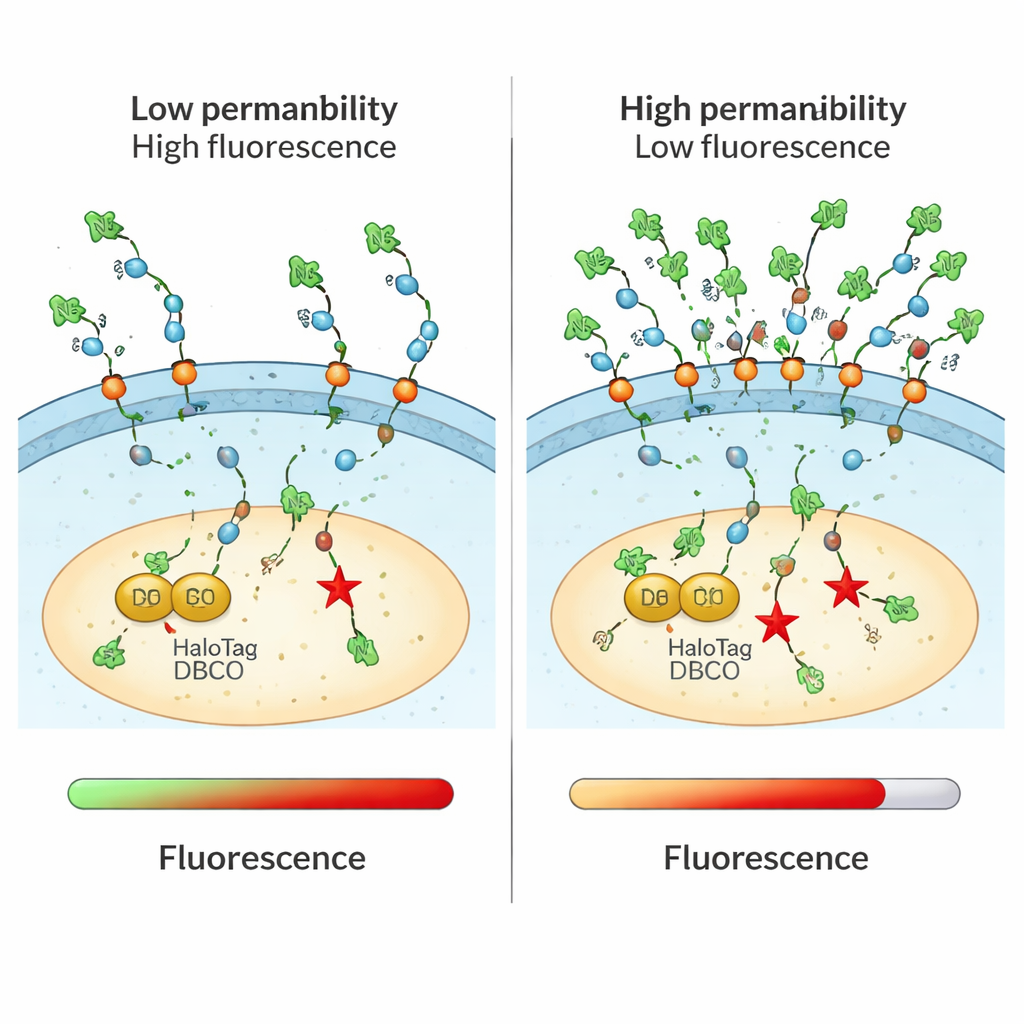
Traditionele methoden om medicijnopname te meten maken vaak geen onderscheid tussen moleculen die slechts de celoppervlakte aanraken, in endosomen zitten of succesvol het cytosol bereiken. Ze vertrouwen mogelijk ook op omvangrijke fluorescente labels die het gedrag van een molecuul veranderen. De CHAMP‑assay lost beide problemen op door een kleine chemische “handgreep” genaamd azide te combineren met een eiwitmarker genaamd HaloTag, die zo is geconstrueerd dat hij vrij in het cytosol van gekweekte humane cellen zweeft. Eerst worden cellen behandeld met een linker die DBCO, een gespannen alkyne‑vorm, aan HaloTag koppelt. Vervolgens voegen wetenschappers hun testverbinding toe, die het kleine azide‑label draagt. Alleen als die verbinding het celmembraan naar het cytosol oversteekt, kunnen azide en DBCO in een zeer selectieve chemische reactie op elkaar ‘clicken’. Een laatste fluorescente azide‑kleurstof maakt zichtbaar hoeveel DBCO‑plaatsen overblijven: zwakke cellen betekenen dat de testverbinding binnenkwam en de meeste plaatsen bezette; felle cellen wijzen op beperkte cytosolische toegang.
Van concept naar werkende test
De auteurs bevestigden eerst dat HaloTag correct werd geproduceerd en in het cytosol van menselijke HeLa‑cellen was gelokaliseerd door een standaard chloroalkaan‑kleurstof te gebruiken en beeldvorming toe te passen. Daarna optimaliseerden ze elk stap van CHAMP: hoeveel DBCO‑linker toe te voegen, hoe lang te incuberen en welke fluorescente azide‑kleurstof een sterk, specifiek signaal gaf zonder cellen te beschadigen. Flowcytometrie — een instrument dat fluorescentie in duizenden individuele cellen meet — toonde dat de assay snel, robuust en instelbaar was. Cruciaal toonden ze aan dat de fluorescentie daadwerkelijk voortkwam uit specifieke reacties op HaloTag‑plaatsen en niet uit kleurstoffen die niet‑specifiek aan celcomponenten plakten, en dat het kleine azide‑label het binnendringen van moleculen in cellen niet merkbaar verstoorde.
Wat de test onthult over kleine medicijnen en peptiden
Met CHAMP in handen testten de onderzoekers honderden met azide gelabelde kleine moleculen en varieerden systematisch eigenschappen zoals lading, grootte en flexibiliteit. Ze observeerden bijvoorbeeld dat het omzetten van een negatief geladen carboxylzuur in een neutrale amide de cytosolische accumulatie vergrootte, en dat de graad en positie van stikstofmethylatie veranderde hoe goed verbindingen binnenkwamen. Door reacties op vrije deeltjes versus levende cellen te vergelijken, konden ze intrinsieke chemische reactiviteit scheiden van de barrière die het membraan zelf oplegt. Het team paste CHAMP ook toe op een paneel van veelvoorkomende antibiotica en liet zien dat sommige veel beter het cytosol bereikten dan andere — belangrijke informatie bij de behandeling van bacteriën die zich verstoppen binnen gastheercellen.
Supergeladen peptiden en eiwitten die de barrière passeren
De assay was bijzonder krachtig voor het bestuderen van grotere, sterk geladen moleculen die lastig te volgen zijn met andere methoden. De auteurs onderzochten celpenetrerende peptiden bestaande uit meerdere arginine‑residuen en bevestigden een duidelijk patroon: langere, positiever geladen ketens leverden meer materiaal in het cytosol af, tot op zekere hoogte. Ze onderzochten hoe het omkeren van de handigheid (stereo‑chemie) van bepaalde aminozuren de opname veranderde, en vonden dat spiegelbeeldversies soms beter accumuleerden, wat wijst op subtiele chirale interacties met het membraan. CHAMP toonde ook dat “supergeladen” eiwitten — ontworpen om veel positieve ladingen te dragen — effectiever het cytosol konden bereiken dan hun normale tegenhangers, wat hun potentieel als drager voor grote therapeutische ladingen ondersteunt.
Ontwerpregels voor toekomstige intracellulaire medicijnen
Door systematisch kleine moleculen, peptiden, macrocyclische peptiden en gewijzigde ruggraten te testen, onthulde de studie algemene ontwerpprincipes. Macrocyclische peptiden, waarvan de ruggraten in ringen worden gesloten, bereikten het cytosol geneigd gemakkelijker dan flexibele lineaire versies. Zorgvuldig geplaatste N‑methylgroepen op peptide‑ruggraten vergrootten de opname bescheiden, maar te veel kon contraproductief zijn. Deze structuur‑permeatie‑relaties, blootgelegd met één gestandaardiseerde assay, bieden praktische richtlijnen voor chemici die moleculen willen ontwerpen die niet alleen aan hun doelen binden, maar die daarbinnen in cellen ook daadwerkelijk kunnen komen.
Hoe dit de geneesmiddelenontwikkeling helpt
In eenvoudige bewoordingen is de CHAMP‑assay een fijn afgestelde verkeersmeter bij de voordeur en binnenhal van de cel. Hij vertelt wetenschappers welke experimentele geneesmiddelen echt voorbij het membraan en in het cytosol komen, zonder te worden misleid door moleculen die aan het oppervlak of in interne compartimenten vastzitten. Omdat hij werkt met een grote verscheidenheid aan moleculaire vormen en groottes en slechts een klein azide‑label gebruikt, kan CHAMP worden geïntegreerd in high‑throughput ontdekkingstrajecten. Na verloop van tijd zou dit het ontwerp van effectievere behandelingen moeten versnellen voor ziektes waarvan de belangrijkste doelwitten binnenin onze cellen opgesloten zitten.
Bronvermelding: Bhandari, S., Ongwae, G.M., Dash, R. et al. A generalizable assay for intracellular accumulation to profile cytosolic drug delivery in mammalian cells. Commun Chem 9, 94 (2026). https://doi.org/10.1038/s42004-026-01898-8
Trefwoorden: intracellulaire medicijnafgifte, membraanpermeabiliteit van cellen, cytosolische accumulatie, celpenetrerende peptiden, bioorthogonale clickchemie