Clear Sky Science · nl
Door metaaloppervlak geïnduceerde DNAzym-catalyse voor efficiënte DNA-splitsing
Metalen die DNA zichzelf laten knippen
De meesten van ons zien metaal als iets vasts en inert—goed voor munten, pannen en bedrading, maar niet voor chemie in een glas water. Deze studie zet die intuïtie op zijn kop door te laten zien dat kale stukken metaal kleine DNA-gebaseerde katalysatoren, DNAzymen genoemd, kunnen inschakelen met niets meer dan puur water en lucht. Het werk onthult een onverwachte manier waarop alledaagse materialen zoals koper en andere metalen complexe, biologisch aandoende reacties aan hun oppervlakken kunnen aandrijven, en wijst op nieuwe instrumenten voor sensoren, geneeskunde en zelfs oorsprong-van-het-leven-chemie. 
Wat zijn DNA-schaar?
DNAzymen zijn korte DNA-strengen die zich vouwen tot vormen die bepaalde chemische reacties kunnen versnellen, vergelijkbaar met eiwitenzymen. Veel bekende DNAzymen fungeren als moleculaire scharen die andere DNA- of RNA-strengen knippen, maar ze hebben bijna altijd opgeloste metaalionen—zoals koper, zink of magnesium—in oplossing nodig om te werken. Eén dergelijke DNAzym, genoemd PL, is een zelfknippende streng die normaal afhankelijk is van koperionen en bepaalde hulpstoffen zoals vitamine C of waterstofperoxide. Deze hulpstoffen nemen deel aan redox- (elektronoverdrachts-) reacties die zeer reactieve zuurstofsoorten genereren, die vervolgens het DNA-ruggengraat op precieze plaatsen aanvallen en breken.
Wanneer een koperdraad een cofactor wordt
Bij het onderzoeken van een elektochemische opstelling om PL-activiteit te regelen, merkten de onderzoekers iets verrassends op: het simpelweg dopen van een kale koperdraad in een oplossing met PL en gedestilleerd water leidde tot efficiënte DNA-splitsing, zelfs zonder toegevoegde koperionen, buffers of zouten. Het koperen oppervlak op zich was net zo goed of beter dan traditionele mengsels van koperionen plus vitamine C of waterstofperoxide, en het knipte het DNA precies op dezelfde plaats. Vervolgtests toonden aan dat veel koperen voorwerpen—platen, trechters, pannen en zelfs munten uit verschillende valuta—PL konden activeren, waarbij de mate van reactie afhing van hoeveel oppervlak van het metaal in contact kwam met de druppel. Vers gepolijst koper werkte iets minder goed dan geoxideerd, ouder koper, wat suggereert dat een dun laagje gevormd door blootstelling aan lucht de reactie juist kan bevorderen.
Welke oppervlakken werken—en waarom
Om te bepalen of dit een koper-specifieke toevalligheid was, screende het team 24 metalen en 10 niet-metalen materialen. Ze vonden dat alleen bepaalde metalen, zoals koper, tantaal en vanadium, PL sterk activeerden, terwijl glas, kunststof, hout en andere niet-metalen niets deden. Metingen toonden aan dat kleine hoeveelheden metaalionen in het water uitlekken van actieve oppervlakken, maar dat deze ionen op zichzelf te zwak waren om de sterke DNA-splitsing te verklaren. Het ontbrekende ingrediënt bleek reactieve zuurstof afkomstig van opgelost lucht te zijn. Met behulp van chemische vangers en enzymen toonden de auteurs aan dat superoxide—een energierijke vorm van zuurstof met een extra elektron—essentieel is. Wanneer opgelost zuurstof werd verwijderd door te bubbelen met stikstof, verdween de PL-activiteit vrijwel; zuurstof terugbrengen herstelde de splitsing. Gezamenlijk ondersteunen de gegevens een cyclus waarbij het metaaloppervlak en de uitlekende ionen opgelost zuurstof omzetten in superoxide en waterstofperoxide precies aan het vaste–vloeibare grensvlak, en dat deze soorten vervolgens de DNA-splitsing aandrijven. 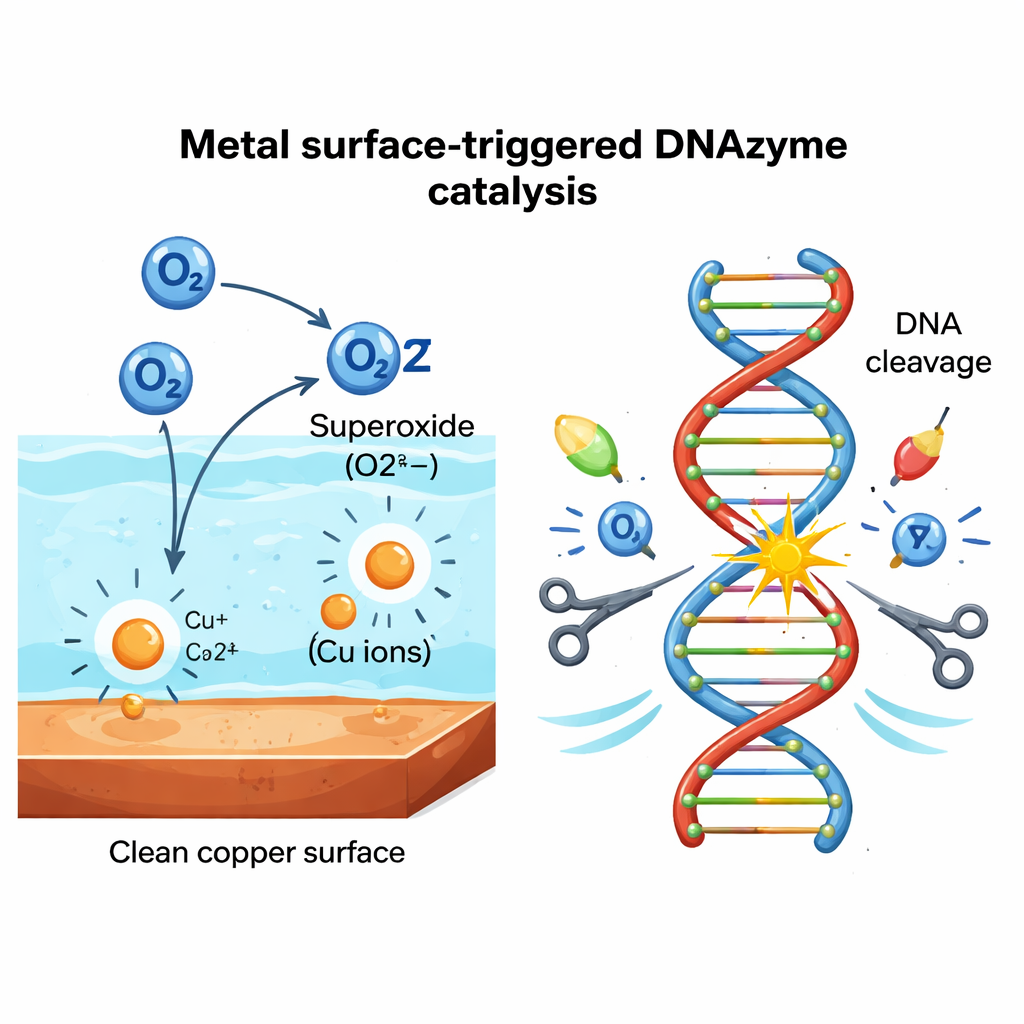
Hulpstoffen, blokkeringen en andere DNA-enzymen
De oppervlak-geïnduceerde chemie kon worden opgeregeld of afgeremd met behulp van bekende moleculen. Chelatoren zoals EDTA, die metaalionen binden, vertraagden de reactie. Catalase, een enzym dat waterstofperoxide afbreekt, en kleurstoffen die superoxide opnemen, verminderden ook de DNA-splitsing, wat de rol van deze reactieve zuurstofsoorten bevestigt. Daarentegen versterkten kleine verbindingen zoals vitamine C, glutathion en catechol de activiteit door de redoxcyclus te voeden die superoxide nabij het metaaloppervlak maakt. Opmerkelijk genoeg was het effect niet uniek voor PL: andere DNAzymen die DNA of RNA knippen, waaronder F-8, Ag10c en I-R3, werden ook geactiveerd door de corresponderende bulkmetalen (bijvoorbeeld zilvermetaal voor een Ag-afhankelijke DNAzym en zinkmetaal voor een Zn-afhankelijke). Dit suggereert dat "door metaaloppervlak geactiveerde" DNA-katalyse een breed verschijnsel kan zijn in plaats van een eenmalige curiositeit.
Waarom dit buiten het laboratorium belangrijk is
Voor lezers buiten de chemie is de kernboodschap dat vaste metaaloppervlakken kunnen fungeren als onzichtbare chemische partners voor DNA-gebaseerde katalysatoren, waarbij alleen lucht en water worden gebruikt om de reactieve soorten te genereren die nodig zijn om DNA te knippen. In plaats van nauwkeurige hoeveelheden metaalionen op te lossen, kan men eenvoudig een geschikt metaaloppervlak in aanraking brengen met een DNA-oplossing en het grensvlak het werk laten doen. Dit opent mogelijkheden voor goedkope sensoren die op metaalobjecten wijzen, hulpmiddelen om schadelijke zuurstofradicalen in cellen te monitoren of op te ruimen, en nieuwe manieren om te bestuderen hoe levenachtige reacties op mineraal- of metaaloppervlakken zouden kunnen plaatsvinden. Kortom, je koperen munt is niet alleen los geld—het kan ook een klein chemisch fabriekje voor DNA-schaar zijn.
Bronvermelding: Jiang, F., Dong, Y., Yu, W. et al. Metal surface-triggered DNAzyme catalysis for efficient DNA cleavage. Commun Chem 9, 91 (2026). https://doi.org/10.1038/s42004-026-01893-z
Trefwoorden: DNAzym, katalyse door metaaloppervlak, reactieve zuurstofsoorten, koperoppervlakchemie, DNA-splitsing