Clear Sky Science · nl
Eerste kristalstructuur van een adduct gevormd bij de reactie van een vanadiumverbinding met menselijke serumtransferrine
Waarom een bloedproteïne en een metalen medicijn ertoe doen
Veel experimentele geneesmiddelen bevatten metaalatomen die kunnen helpen bij de behandeling van aandoeningen variërend van diabetes tot kanker. Zodra deze metalen medicijnen echter in de bloedbaan terechtkomen, moeten ze meeliften op de natuurlijke transporteiwitten van het lichaam. Deze studie onderzoekt hoe één zo’n eiwit, menselijke serumtransferrine — de belangrijkste draagster van ijzer in ons bloed — omgaat met een veelbelovende vanadiumverbinding, en werpt licht op hoe metalen geneesmiddelen door het lichaam worden vervoerd en hoe ze mogelijk veiliger en effectiever kunnen worden afgestemd.
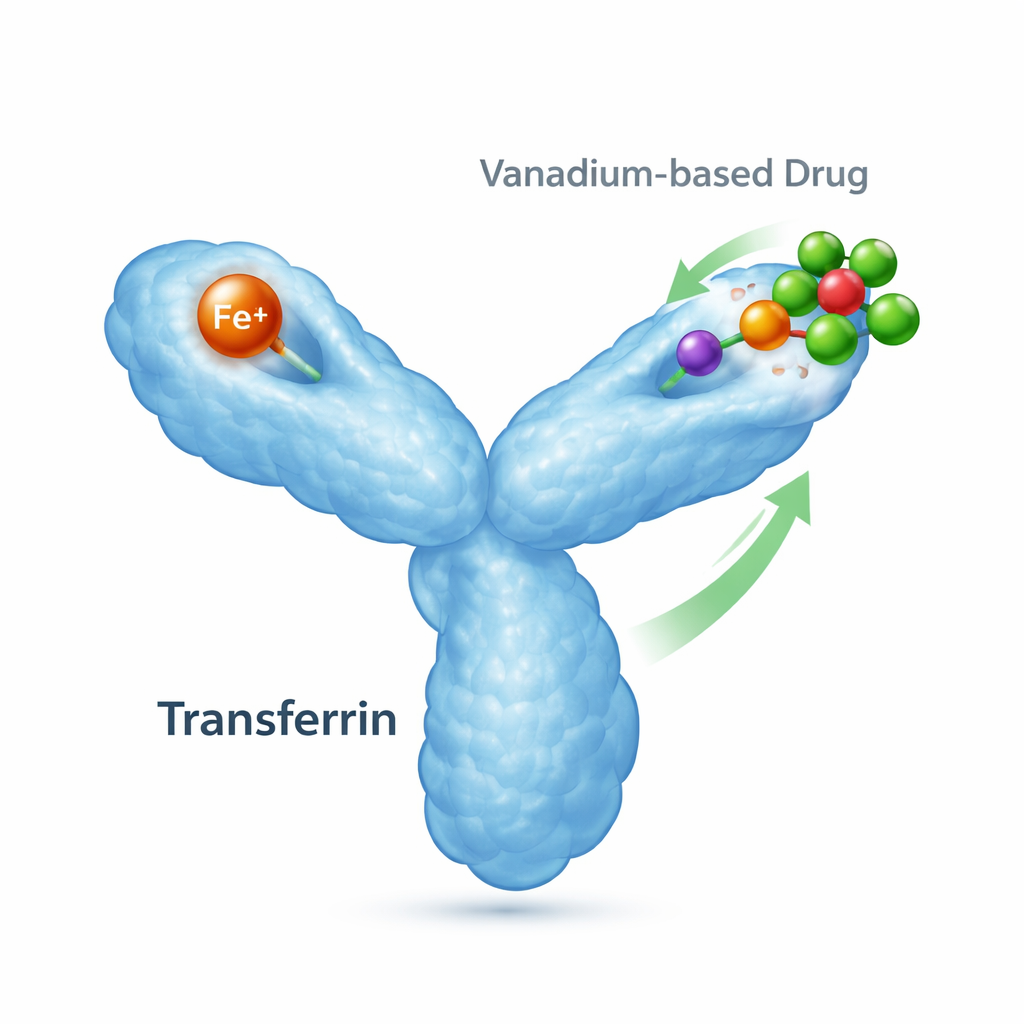
De ijzerkoerier van het lichaam en zijn nevenfuncties
Transferrine is een eiwit van ongeveer 80 kilodalton waarvan de hoofdtaak is ijzer vast te pakken en af te leveren aan cellen die het nodig hebben. Het heeft twee ‘lobben’, die elk één ijzerion kunnen binden, en het verandert van vorm afhankelijk van de aanwezigheid van ijzer. Wanneer ijzer bindt, klapt een lob dicht; zonder ijzer blijft hij open. Gespecialiseerde receptoren op celoppervlakken herkennen deze ijzerbeladen vormen en internaliseren ze, waardoor transferrine centraal staat in de ijzerbalans en de gezondheid van cellen. Transferrine kan echter ook andere metalen binden, waaronder metalen uit medische behandelingen, wat betekent dat het kan beïnvloeden waar metalen geneesmiddelen naartoe gaan en hoe ze werken.
Een vormsnapshot van vanadium op transferrine
De onderzoekers concentreerden zich op een goed bestudeerde vanadiumkandidaat die vaak wordt aangeduid als bis(acetylacetonato)oxovanadium(IV), geschreven als [VIVO(acac)₂]. Eerder werk toonde aan dat deze verbinding, of soorten die daarvan in water ontstaan, zich aan transferrine kunnen hechten, maar niemand had precies gezien hoe dat gebeurt. Met röntgendiffractie verkregen het team hoogresolutie-structuren van transferrine dat alleen ijzer draagt in de C-terminaal lob (de “FeC”-vorm), zowel vóór als na blootstelling aan het vanadiummiddel. In de met vanadium behandelde kristallen zagen ze niet het oorspronkelijke medicijn, maar een getransformeerde vanadium‑zuurstofcluster gebonden in de ijzervrije N-terminaal lob. Dit leverde het eerste directe structurele beeld op van een vanadiumfragment geassocieerd met menselijke transferrine.
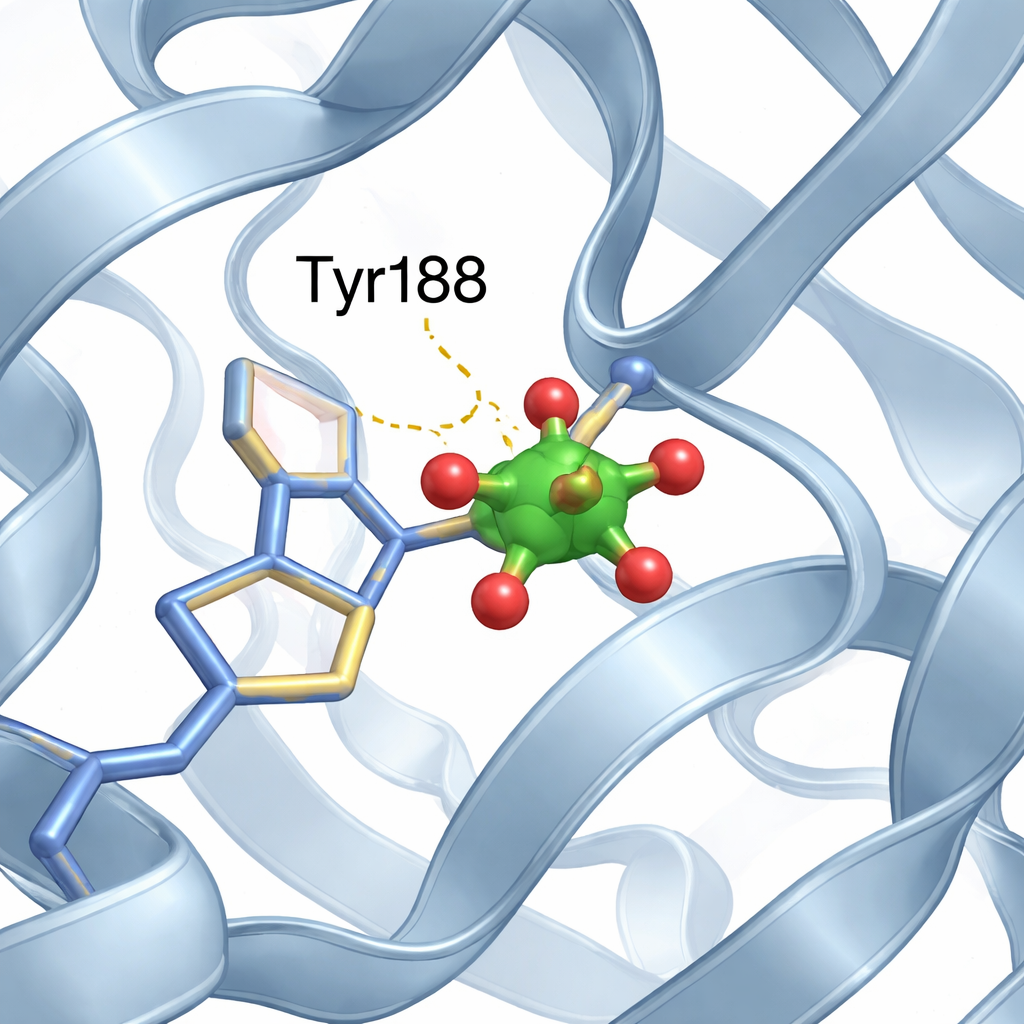
Een klein vanadiumcluster vindt een plekje
In de ijzerplaats van de N-lob identificeerde het team een kleine cluster bestaande uit twee vanadiumatomen en zuurstofatomen, het best te beschrijven als een gewijzigde “divanadaat”eenheid. Een van de zuurstofposities van de cluster wordt ingenomen door de zuurstof van een specifiek aminozuur, tyrosine 188 (Tyr188), waardoor een directe binding tussen eiwit en metaalcluster ontstaat. Aanvullende zwakkere interacties, zoals waterstofbruggen van nabijgelegen eiwitsegmenten, stabiliseren de cluster verder op zijn plaats. Belangrijk is dat, ondanks deze nieuwe metaalgast in een ijzerbindend holte, het eiwit zijn gebruikelijke open N-lob en gesloten C-lob rangschikking behoudt, bijna identiek aan de vanadiumvrije structuur.
Hoe transferrine de chemie van vanadium hervormt
In oplossing bij de pH en concentratie gebruikt voor kristallisatie is de specifieke twee‑vanadiumsoort die in het kristal werd gezien normaal gesproken slechts een klein deel van het geheel; grotere vanadium‑zuurstofclusters domineren doorgaans. Spectroscopische metingen en theoretische speciatieschattingen suggereren dat het oorspronkelijke vanadiummedicijn langzaam oxideert en uiteenvalt in water, waarbij eenvoudige vanadaationen worden gevormd die zich vervolgens tot verschillende clusters assembleren. De kristalstructuur geeft aan dat transferrine selectief dit kleine divanadaat‑achtige fragment stabiliseert boven de grotere clusters, en daarmee één chemische vorm uit een drukke oplossingsmix ‘kiest’ door een nauw aansluitende bindingsplaats bij Tyr188 en een ondersteunend netwerk van waterstofbruggen te bieden.
Het handdrukcontact met de celreceptor blijft behouden
Aangezien transferrine een receptor op celoppervlakken moet binden om ijzer af te leveren, vroegen de onderzoekers of het aanhechten van deze vanadiumcluster die cruciale handdruk zou verstoren. Met niet‑denaturerende gelelektroforese en een gevoelige techniek genaamd biolayer interferometrie maten ze hoe goed met vanadium behandeld transferrine aan de transferrinereceptor bond vergeleken met de onbehandelde ijzer‑alleen vorm. Beide gedroegen zich vrijwel identiek, met zeer sterke binding in het lage nanomolaire bereik. Dit bevestigt dat de vanadiumcluster, hoewel genesteld in de N-lob, de vorm van transferrine op het punt waar de receptor bindt niet significant verandert en dus het eiwit niet verhindert door cellen te worden herkend.
Wat dit betekent voor metalen geneesmiddelen
Voor niet‑specialisten is de kernboodschap dat deze studie een moleculair beeld levert van hoe een vanadiummedicijnafgeleide zich hecht aan het belangrijkste ijzertransporteiwit van het lichaam zonder zijn normale functie te ontregelen. Transferrine kan een specifiek klein vanadium‑zuurstofcluster in een ijzerplaats vangen, terwijl de algehele eiwitvorm en het vermogen om aan zijn receptor te binden nagenoeg ongewijzigd blijven. Dit helpt verklaren hoe vanadiumgeneesmiddelen mogelijk in circulatie zijn als verbonden met transferrine en benadrukt dat verschillende eiwitten de voorkeur kunnen geven aan verschillende groottes van vanadiumclusters. Zulke inzichten zijn essentieel voor het ontwerpen van slimmere metalen‑gebaseerde therapieën waarvan het gedrag in de bloedbaan — welke vormen ze aannemen, waar ze naartoe gaan en hoe lang ze blijven — voorspelbaar en beheersbaar is.
Bronvermelding: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Trefwoorden: vanadiumgeneesmiddelen, menselijke serumtransferrine, metalen-gebaseerde therapieën, eiwit–metaalbinding, structurele biologie