Clear Sky Science · nl
Lactam maakt afstandsboronatenomleggingen naar C═N-bindingen mogelijk
Een nieuwe snelweg voor het bouwen van medicijnachtige moleculen
Chemici zoeken voortdurend naar snellere, schonere manieren om de complexe moleculen in geneesmiddelen en geavanceerde materialen te construeren. Deze studie introduceert een slimme snelkoppeling waarbij een veelvoorkomende ringachtige structuur, een lactam, tijdelijk een reactie begeleidt en zich daarna terugtrekt — waardoor het mogelijk wordt eenvoudige, gemakkelijk verkrijgbare ingrediënten om te zetten in waardevolle bouwstenen voor de farmacie zonder dure metalen of ingewikkelde voorbereidende stappen.
Een stille hulp omvormen tot tijdelijk richtmiddel
Veel moderne geneesmiddelen en functionele materialen zijn gebaseerd op reacties van boronzuurderivaten, een familie van boronhoudende verbindingen die gewaardeerd worden vanwege hun betrouwbaarheid en milde eigenschappen. Traditioneel moeten chemici speciale “richtgroepen” vooraf aanbrengen op beginmateriaal om boronverbindingen ertoe te bewegen nieuwe bindingen met carbon‑stikstof dubbele bindingen (C=N) te vormen. Deze groepen fungeren als handvatten die de reactie sturen, maar kosten extra tijd, geld en stappen — en werken vaak alleen met zeer reactieve partners. De auteurs realiseerden zich dat lactams, ringvormige verwanten van de bekende amidebinding in eiwitten, kunnen dienen als ingebouwde, tijdelijke richtmiddelen. Door te coördineren met het boronatoom helpt het lactamzuurstof een hoog-geordend, vier-gelig boroncentrum te vormen dat een aangehecht fragment langs het molecuul kan verplaatsen, waardoor nieuwe C–N-bindingen ontstaan zonder een blijvende richtgroep.
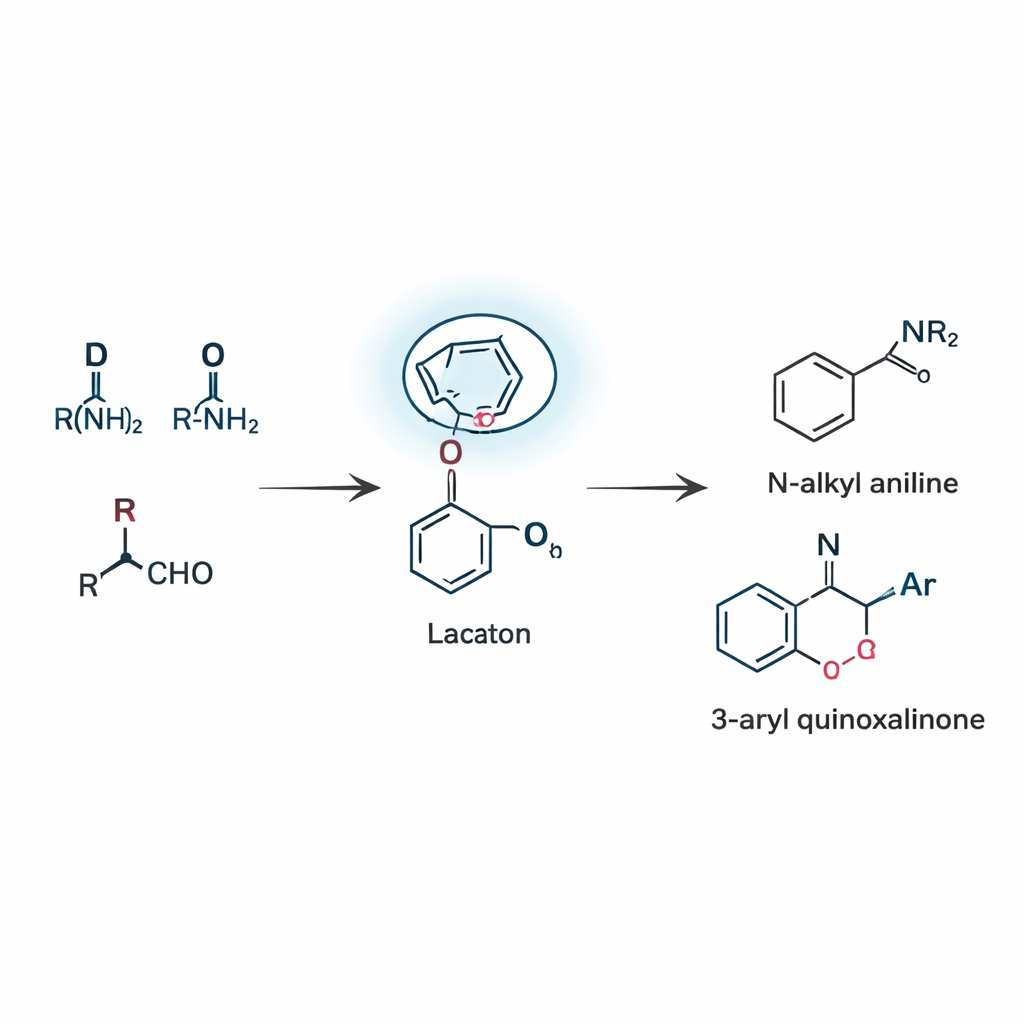
Twee families van nuttige producten bouwen met één strategie
Mits dit concept ontwikkelden de onderzoekers twee verwante reacties die beide leunen op deze lactam-geleide herschikking, bekend als een afstandsboronaat-rearrangement. In de eerste reactie komen drie eenvoudige componenten — een aldehyde, een amine en een boronzuur — samen om N‑alkylanilines te vormen, een kernelement dat voorkomt in talloze kandidaat-geneesmiddelen en kleurstoffen. De reactie verloopt via een zeldzame 1,5‑verschuiving, waarbij een arylgroep op boron over vijf atomen springt om de C=N-binding te bereiken. Door de katalysator, het oplosmiddel en de temperatuur zorgvuldig af te stemmen, realiseerden de onderzoekers behoorlijke opbrengsten en toonden ze aan dat veel verschillende substituenten, waaronder halogenen, alkylgroepen en heterocycli, worden verdragen. In de tweede reactiemodus wordt hetzelfde leidende idee toegepast op quinoxalinonen, een klasse stikstofrijke ringen die veel voorkomen in de medicijnchemie. Hier gebruikt de reactie helemaal geen toegevoegd metaal-katalysator en levert toch efficiënt 3‑arylquinoxalinonen, dankzij het vermogen van het lactam om boron te betrekken en het sleuteltussentijdse te stabiliseren.
Groene condities en late‑stage aanpassingen van geneesmiddelen
Naast het aantonen van een brede toepasbaarheid laten de auteurs zien dat deze strategie praktisch is voor echte moleculen. Omdat de 1,4‑rearrangement op quinoxalinonen onder metaalvrije omstandigheden in een specifiek alcoholisch oplosmiddel verloopt, vermijdt het de noodzaak van dure of toxische overgangsmetalen. Het team paste de methode toe op complexe fragmenten afgeleid van geregistreerde geneesmiddelen zoals ibuprofen en andere therapeutica die het quinoxalinone‑skelet bevatten. In elk geval bracht de reactie nieuwe arylgroepen op een specifieke positie in zonder andere gevoelige kenmerken te verstoren. Dit soort “late‑stage functionalisatie” stelt chemici in staat bestaande medicijnkernen snel van nieuwe zijgroepen te voorzien, waardoor de zoektocht naar verbeterde werkzaamheid, veiligheid of fysische eigenschappen wordt versneld.
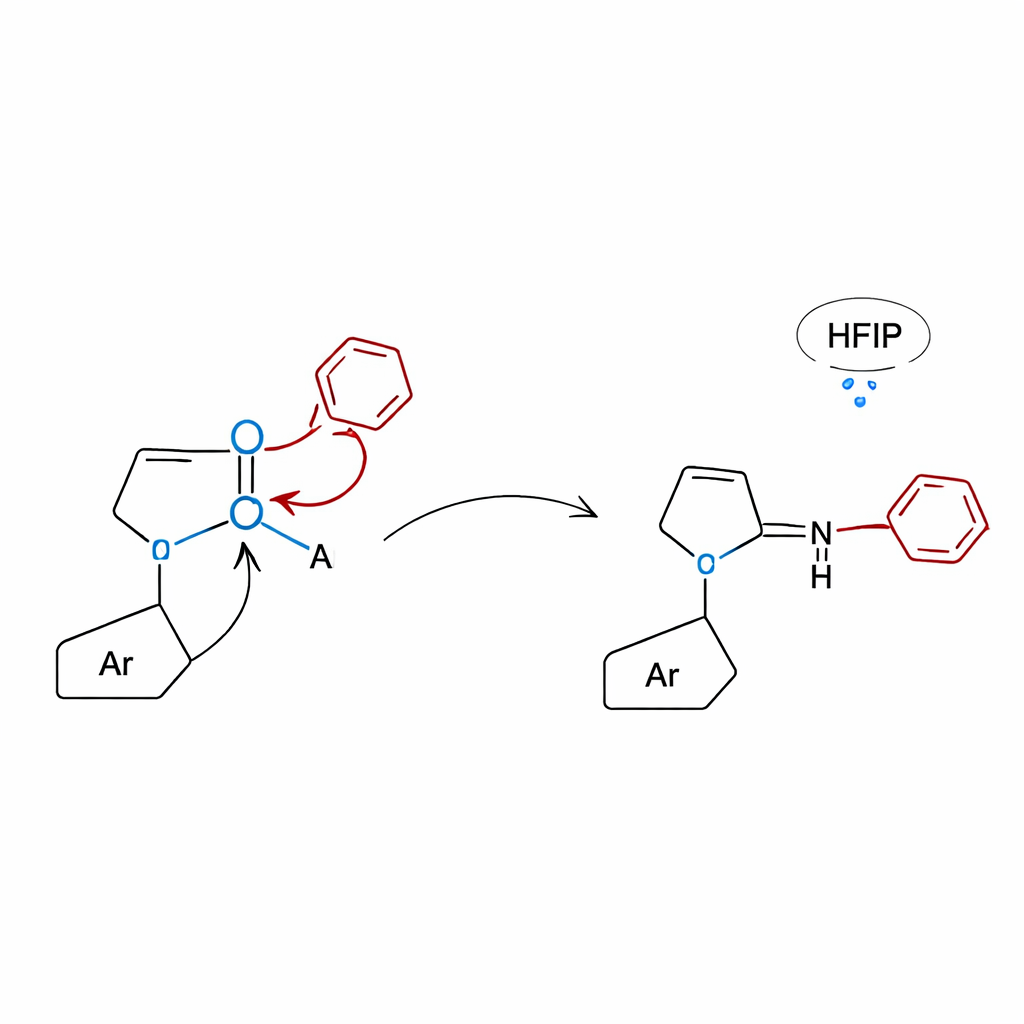
Onder de motorkap kijken met theorie en controletests
Om te begrijpen waarom de lactam-aanpak zo goed werkt, combineerden de onderzoekers zorgvuldig ontworpen controlexperimenten met computersimulaties. Wanneer moleculen zonder het lactamdeel werden getest, stokten de reacties vrijwel volledig, wat bevestigt dat de lactamring essentieel is voor het activeren van het boronzuur en het sturen van de herschikking. Kwantumchemische berekeningen toonden aan dat het lactamzuurstof aan boron bindt om een compact, vier‑gecoördineerd structuur te vormen waarvandaan de arylgroep kan migreren ofwel over vijf atomen (1,5‑verschuiving) om N‑alkylanilines te geven, of over vier atomen (1,4‑verschuiving) om 3‑arylquinoxalinonen te vormen. In het quinoxalinone‑geval verlaagt het waterstofbindingsnetwerk dat door het HFIP‑oplosmiddel wordt geboden verder de energiebarrière, waardoor de reactie onder relatief milde thermische omstandigheden zonder toegevoegde katalysator kan verlopen.
Waarom dit belangrijk is voor toekomstige geneesmiddelen
Al met al laat het werk zien dat een eenvoudige lactamring kan fungeren als een dynamisch, recyclebaar richtmiddel dat eerder ontoegankelijke bindingsvormende patronen in de boronzuurchemie ontsluit. Voor niet‑specialisten is de kernboodschap dat chemici nu een directere, efficiëntere manier hebben om basale bouwstenen om te zetten in twee belangrijke klassen stikstof‑bevattende moleculen die ten grondslag liggen aan veel geneesmiddelen. Omdat de methode dure metalen vermijdt, een breed scala aan functionele groepen tolereert en werkt op gevorderde medicijnachtige structuren, heeft zij het potentieel om het ontwerp en de optimalisatie van toekomstige farmaceutica en mogelijk nieuwe agrochemicaliën te stroomlijnen.
Bronvermelding: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
Trefwoorden: boronzuur, lactamchemie, C–N-bindingvorming, quinoxalinonen, medicijnchemie