Clear Sky Science · nl
Enzymen vinden via ortholoog-inferentie om het anti-kanker scaffold evodiamine te diversifiëren
Plantaardige chemicaliën omzetten in betere geneesmiddelen
Veel van de geneesmiddelen van vandaag begonnen hun bestaan als verdedigingschemicaliën in planten. Deze natuurlijke moleculen vertonen vaak krachtige effecten tegen kanker, infecties of pijn, maar ze zijn zelden perfecte geneesmiddelen. Chemici willen hun structuren graag precies aanpassen om ze veiliger en effectiever te maken, maar die moleculen zijn vaak zo complex dat zelfs kleine veranderingen moeilijk zijn. Deze studie laat zien hoe wetenschappers plantenenzymen kunnen inzetten als kleine moleculaire werktuigen om gerichte veranderingen aan te brengen in een anti-kankerverbinding genaamd evodiamine, wat mogelijk nieuwe wegen opent naar verbeterde therapieën.
Waarom dit plantmolecuul ertoe doet
Evodiamine is een natuurlijk verbinding die voorkomt in de vruchten van een boom die in de traditionele Chinese geneeskunde wordt gebruikt. Het behoort tot een familie van ringvormige moleculen die al ten grondslag liggen aan belangrijke geneesmiddelen tegen kanker, hoge bloeddruk en infecties. Evodiamine zelf heeft aangetoonde anticancereuze, ontstekingsremmende, pijnstillende en antimicrobiële eigenschappen, en sommige van zijn aangepaste versies lijken veelbelovend als multitarget leads voor kanker. De uitdaging is hoe je nieuwe chemische "handvatten", zoals zuurstofbevattende groepen, op heel specifieke plekken aan dit drukke scaffold kunt toevoegen zonder agressieve chemicaliën of meerstaps-synthesen te gebruiken.
Enzymen het moeilijke werk laten doen
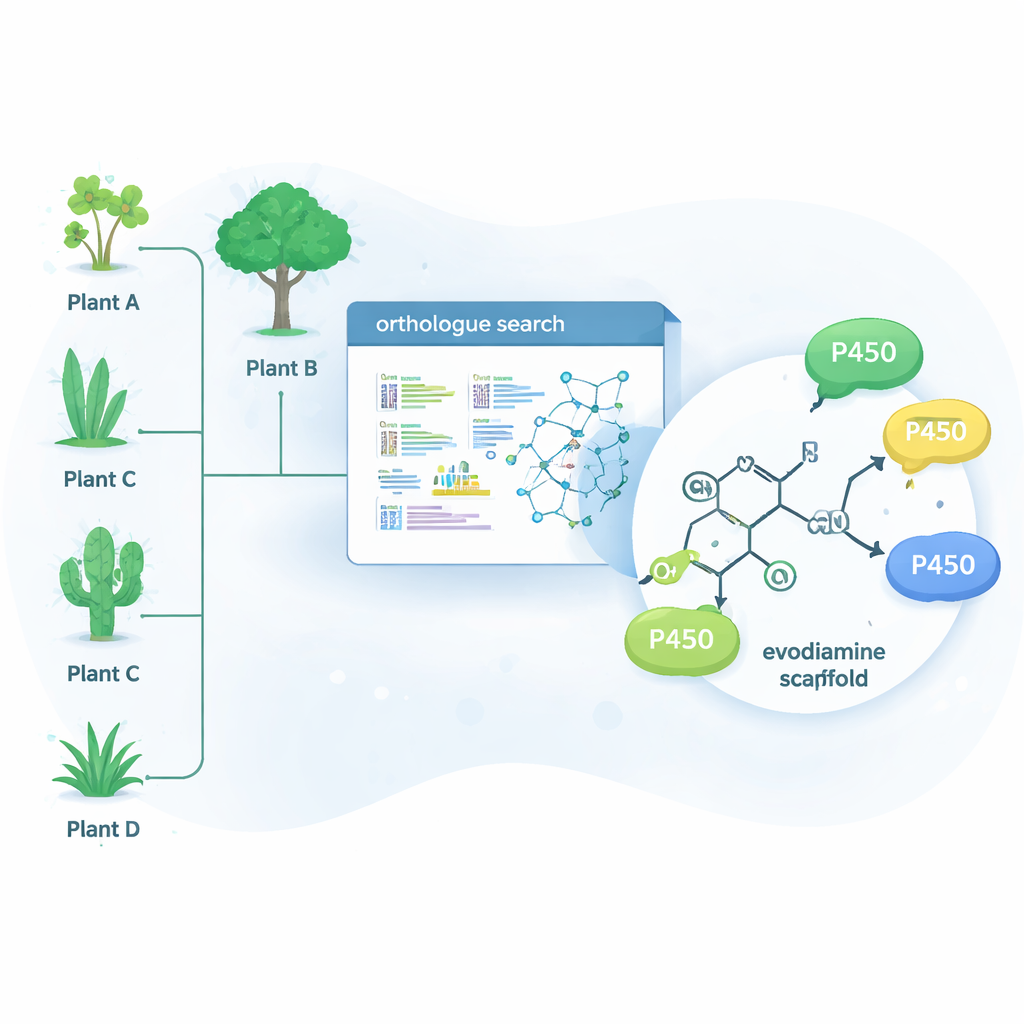
De natuur heeft veel van deze lastige chemische problemen al opgelost met behulp van enzymen — eiwitten die specifieke reacties katalyseren. Eén grote enzymfamilie, de cytochroom P450's, blinkt uit in het toevoegen van zuurstof aan anders onreactieve koolstof‑waterstofbindingen. Die ene stap kan drastisch veranderen hoe een molecuul zich in het lichaam gedraagt en kan ook een beginpunt creëren voor verdere chemische modificatie. In plaats van alleen te zoeken in planten die van nature evodiamine produceren, gebruikten de onderzoekers een bioinformaticatool genaamd OrthoFinder om genetische gegevens van 15 verschillende alkaloïde-producerende planten te doorzoeken. Ze zochten naar P450-enzymen die nauwe "orthologen" zijn van bekende alkaloïde-modificerende enzymen, met de redenering dat familieleden van deze enzymen mogelijk ook in staat zijn verwante, geneesmiddelachtige moleculen fijn af te stemmen.
Nieuwe enzymen vinden in onverwachte planten
Uit honderden kandidaatgenen beperkte het team de lijst tot 15 veelbelovende P450's en brachten ze deze tot expressie in gistcellen, die dienden als miniatuurfabriekjes voor enzymen. Ze voedden deze gisten vervolgens met een verzameling complexe plantmoleculen en analyseerden welke chemisch werden veranderd. Vier enzymen — drie afkomstig van de boom Camptotheca acuminata en één van de struik Tabernaemontana elegans — bleken op evodiamine in te werken, hoewel geen van beide planten erom bekend staat het te produceren. Deze enzymen introduceerden selectief een zuurstofatoom op één van twee posities van het evodiamine-ringssysteem, waardoor twee hoofdproducten ontstonden: 10‑hydroxyevodiamine en 3‑hydroxyevodiamine. Dergelijke geoxideerde versies zijn gemakkelijker verder te transformeren tot wateroplosbare of krachtigere geneesmiddelkandidaten, met mildere chemie dan traditionele synthetische routes.
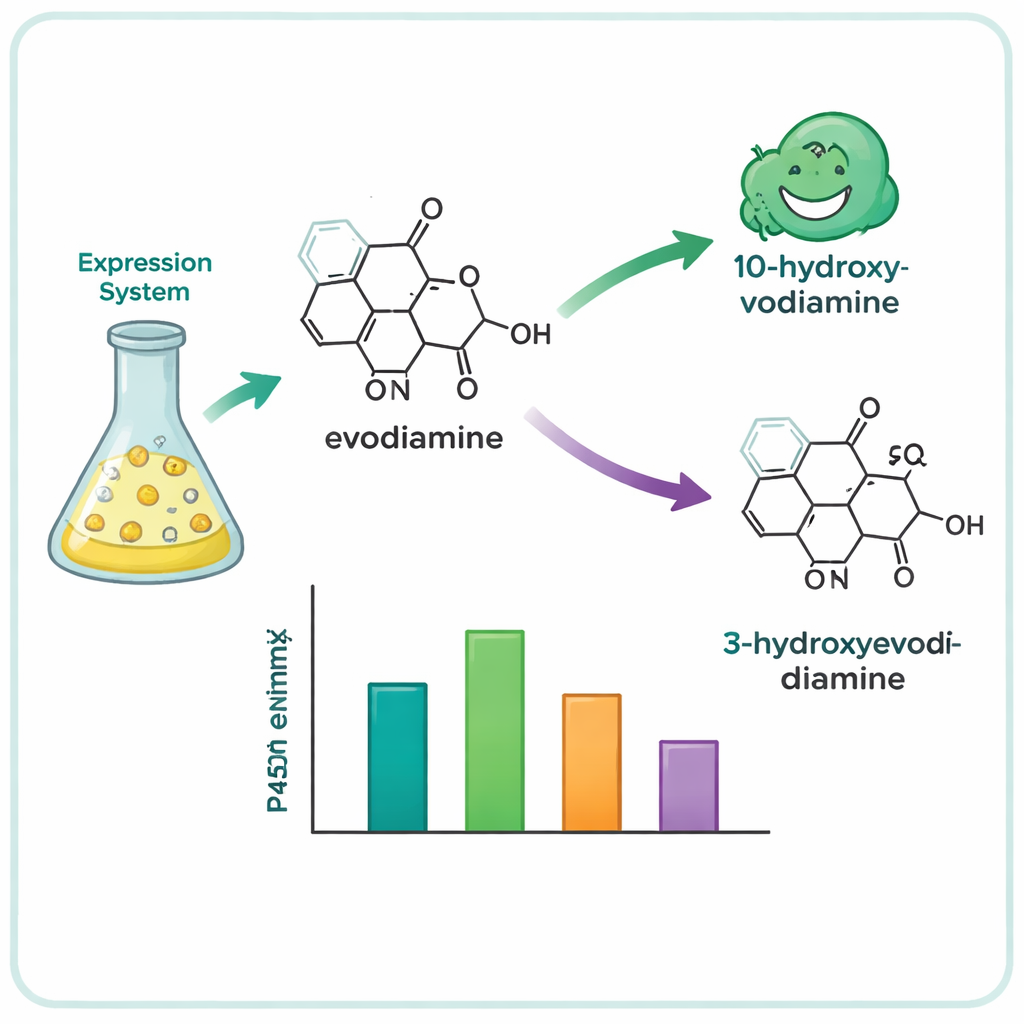
Een kijkje in de moleculaire gereedschapskist
Om te begrijpen waarom deze nauw verwante enzymen zich verschillend gedroegen, bouwden de onderzoekers driedimensionale modellen van het meest actieve enzym en zijn verwanten met moderne eiwit-structuurvoorspellingstools. Vervolgens gebruikten ze computerdocking om te zien hoe evodiamine in de actieve pocket van de enzymen zou kunnen liggen, dicht bij het ijzerhoudende centrum van de P450 waar de reactie plaatsvindt. De modellen benadrukten verschillende volumineuze, waterafstotende aminozuren — vooral fenylalanine-residuen — gepositioneerd nabij de aromatische ringen van evodiamine. Door deze posities zorgvuldig te muteren toonden de onderzoekers aan dat het veranderen van de grootte en vorm van deze pocket de activiteit kan verzwakken, kan beïnvloeden hoe goed het substraat past, of zelfs de bevooroordeelde zuurstofatieplaats kan verschuiven van de ene ring van het molecuul naar de andere. In één geval draaide een enkele mutatie de voorkeur van het enzym om van het maken van het 10‑hydroxyproduct naar het 3‑hydroxyproduct.
Wat dit betekent voor toekomstige geneesmiddelen
Voor niet‑specialisten is de belangrijkste conclusie dat de auteurs een praktische routekaart hebben gedemonstreerd voor het ontdekken en tunen van plantenenzymen die precieze, "chirurgische" aanpassingen kunnen uitvoeren op complexe geneesmiddelachtige moleculen. Door grootschalige genetische exploratie te combineren met enzymtesten en structurele modellering, ontdekten ze een set biokatalysatoren die het evodiamine-scaffold selectief kunnen herschikken op posities die moeilijk bereikbaar zijn met standaardchemie. Dit biedt niet alleen een schonere, duurzamere manier om geavanceerde versies van evodiamine te maken — zoals wateroplosbare anticancer leads — maar toont ook aan dat nuttige enzymen gevonden kunnen worden in planten die zelf het doelmolecuul niet produceren. Dezelfde strategie kan nu op veel andere natuurlijke producten worden toegepast, wat het ontwerp van volgende generatie plantaardige geneesmiddelen kan versnellen.
Bronvermelding: Kwan, B.D., Kim, T., Nguyen, H.H. et al. Orthologue inference-based enzyme mining for diversification of the anti-cancer evodiamine scaffold. Commun Chem 9, 73 (2026). https://doi.org/10.1038/s42004-025-01876-6
Trefwoorden: evodiamine, plantenenzymen, cytochroom P450, biokatalyse, geneesmiddelenonderzoek