Clear Sky Science · nl
PACS1-syndroommutatie verstoort dyneinegemedieerde vrachtafgifte via HDAC6 en BICD2
Waarom dit belangrijk is voor hersenontwikkeling
PACS1-syndroom is een zeldzame genetische aandoening die tot verstandelijke beperkingen, epileptische aanvallen en kenmerkende gelaatstrekken leidt. Voor families en clinici zijn de symptomen bekend, maar tot voor kort was onduidelijk wat er precies misgaat binnen de cellen van patiënten. Deze studie haalt die mysterie weg en laat zien hoe een letterverandering in het PACS1-gen het intracellulaire transportsysteem verstoort, vooral in neuronen, en hoe dat PACS1-syndroom verbindt met een bredere familie van ‘‘verkeers’’ziekten van het zenuwstelsel. 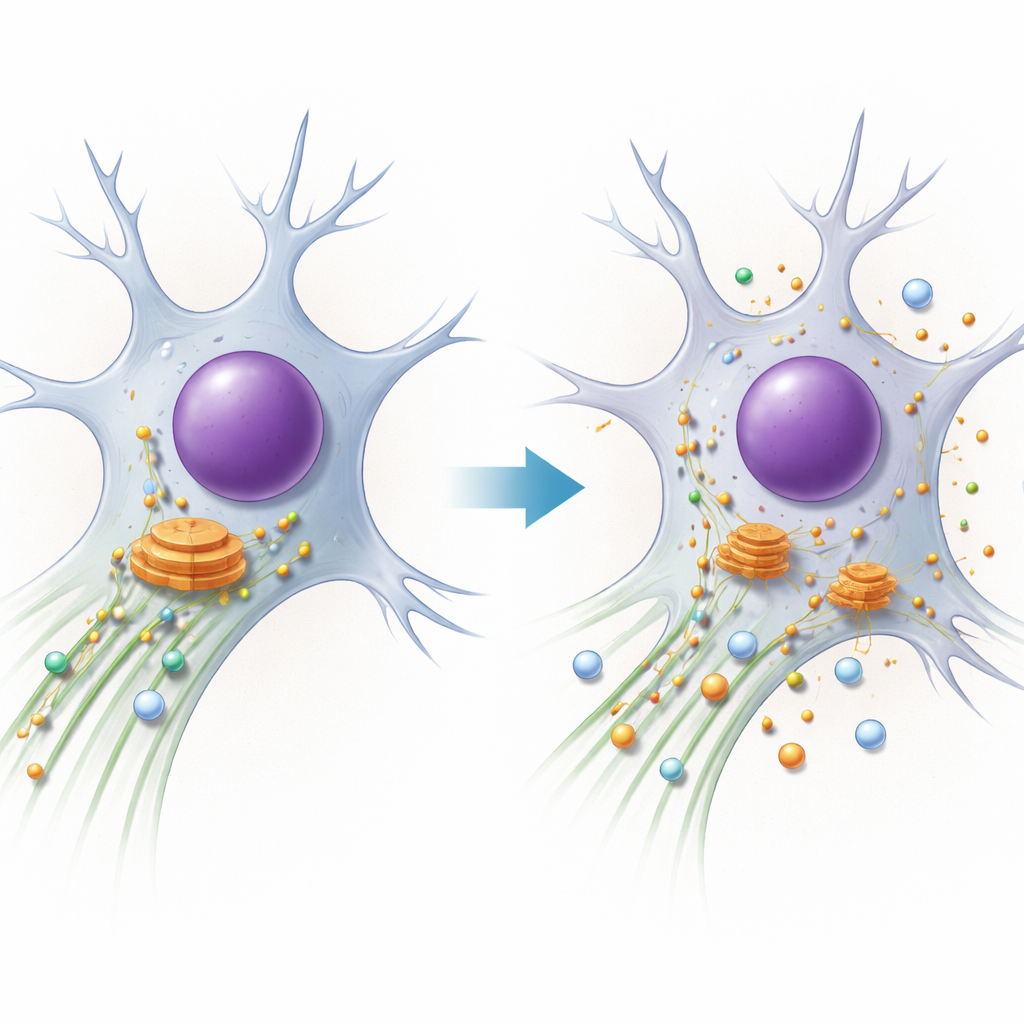
De afleversnelwegen van de cel
Elke cel is afhankelijk van microscopische snelwegen gemaakt van proteïnebuizen die microtubuli heten. Moleculaire motoren lopen over deze banen en vervoeren ladingen zoals enzymen en membraancompartimenten naar de plekken waar ze nodig zijn. Eén motor, dyneïne, is verantwoordelijk voor langeafstands ‘‘terugritten’’ die vracht van de buitenkant van de cel terugtrekken naar het centrum, waar een belangrijk sorteerstation, het Golgi-apparaat, zit. De auteurs richten zich op PACS1, een eiwit dat helpt bepalen welke lading dyneïne meeneemt en daarnaast de toestand van de sporen afstemt via een ander eiwit, HDAC6, dat een chemische merker (acetylatie) op de microtubuli reguleert. Neuronen, met hun zeer lange uitlopers, zijn bijzonder gevoelig voor zelfs kleine storingen in dit systeem.
Een gemuteerde coördinator die te stevig vastgrijpt
Het PACS1-syndroom wordt veroorzaakt door de terugkerende R203W-mutatie in PACS1. Het team ontdekte dat zowel normaal als gemuteerd PACS1 fysiek binden aan de zware keten van dyneïne, maar dat de gemuteerde vorm steviger vastklampt. Met huidcellen van patiënten en geïngineerde cellijnen lieten ze zien dat deze overmatige interactie hetzelfde resultaat oplevert als een gedeeltelijk verlies van dyneïnefunctie: het Golgi valt uiteen in verspreide mini-stapels en een belangrijk enzym, furine, dat normaal op de trans-zijde van het Golgi staat, wordt verkeerd gestuurd naar andere compartimenten. Door de structuur van PACS1 te ontleden, identificeerden ze een korte beta-streng ‘‘patch’’ die specifiek contact maakt met dyneïne. Toen ze dit patch wijzigden zonder andere PACS1-functies te verstoren, verloor furine opnieuw zijn juiste locatie, wat bevestigt dat de dyneïne–PACS1-handdruk cruciaal is voor correcte vrachtafgifte. 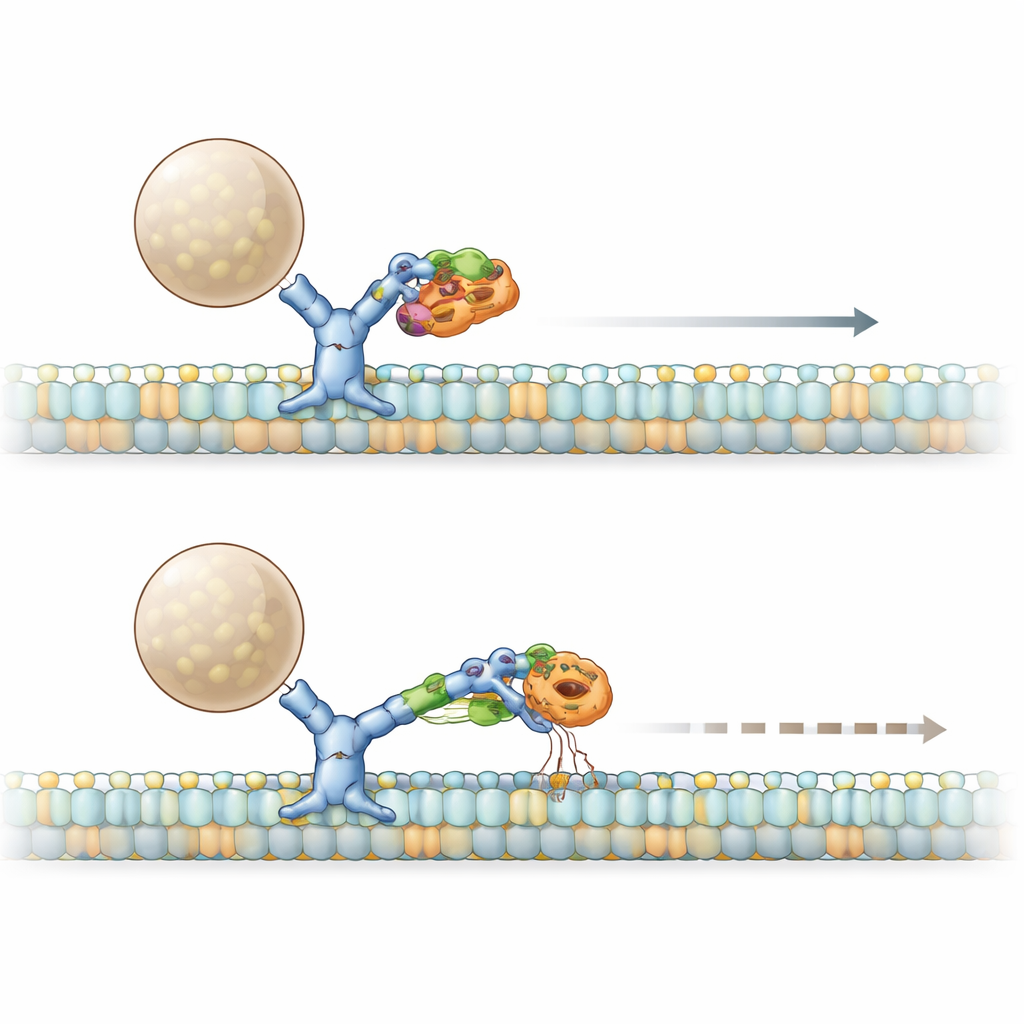
Hoe een drie-eiwittenalliantie de motor blokkeert
Het verhaal verdiept zich met twee aanvullende spelers: HDAC6 en een adaptor genaamd BICD2, die helpt bij het samenstellen van actieve dyneïnecomplexen. Het gemuteerde PACS1 verhoogt niet alleen de HDAC6-activiteit, waardoor de acetylatie op microtubuli afneemt, maar vormt ook een vergroot complex met HDAC6 en BICD2. Biochemische testen toonden aan dat mutant PACS1 en HDAC6 samen BICD2 van dyneïne wegtrekken, terwijl de samenwerking met een voorwaarts bewegende motor (kinesine) onaangetast blijft. In levende cellen vertraagde een kunstmatige lading die normaal vlot door dyneïne werd voortbewogen en werden er minder vrachten verplaatst wanneer mutant PACS1 aanwezig was. Het blokkeren van HDAC6 herstelde zowel de snelheid als het aantal bewegende deeltjes, wat aantoont dat het mutant PACS1–HDAC6–BICD2-complex als een rem werkt op dyneïnes vermogen om transport te starten en vol te houden.
Verkeer redden met een natuurlijke dyneïnhelper
De onderzoekers testten vervolgens of dyneïne ondanks het gemuteerde complex weer ‘‘geheractiveerd’’ kon worden. Ze bedienden zich van Lis1, een bekende dyneïnhelper die actieve motorassemblages stabiliseert. In patiëntencellen waren de Lis1-niveaus enigszins verlaagd. Toen het team extra Lis1 toevoegde, verbeterden twee zaken: het Golgi hergroepeerde weer dicht bij het celcentrum en lysosomen, een andere klasse organellen die naar buiten waren verschoven, keerden terug naar hun plaats. In dezelfde motiliteitsassay verhoogde Lis1 zowel de frequentie als de snelheid van dyneïnegedreven vrachtafgifte in aanwezigheid van mutant PACS1. Deze resultaten tonen aan dat het probleem niet is dat dyneïne ontbreekt, maar dat het gevangen zit in een slecht actieve toestand—een toestand die gedeeltelijk kan worden gecorrigeerd door óf HDAC6 te remmen óf dyneïneactivatie te versterken.
Een zeldzaam syndroom verbinden met een breder palet van aandoeningen
Door structurele analyse, celbiologie en live-imaging te combineren, stellen de auteurs een duidelijk model voor: PACS1 koppelt normaal geselecteerde ladingen aan dyneïne en verfijnt de prestaties van de motor via HDAC6 en microtubule-acetylatie. De R203W-mutatie opent het interactieoppervlak van PACS1, waardoor HDAC6 en BICD2 overgerekruteerd worden in een complex dat dyneïnes vermogen om microtubuli te grijpen en efficiënt te bewegen ondermijnt. Het resultaat is wijdverspreide misplaatsing van Golgi, lysosomen en andere ladingen, vooral in neuronen waar langeafstandsvervoer vitaal is. Dit mechanisme helpt verklaren waarom het verlagen van PACS1 of HDAC6 met antisensetherapieën hersenafwijkingen in muismodellen corrigeert en nu bij patiënten wordt onderzocht. In bredere zin plaatst het PACS1-syndroom binnen het groeiende spectrum van microtubuleverkeersstoornissen, naast aandoeningen veroorzaakt door mutaties in dyneïne, BICD2 en aanverwante transportfactoren.
Bronvermelding: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
Trefwoorden: PACS1-syndroom, dyneintransport, microtubuleverkeer, Golgi-organisatie, neurale ontwikkeling