Clear Sky Science · nl
Microglia veroorzaken HIV-geïnduceerde transcriptionele en metabole veranderingen in menselijke neurale organoïden
Waarom veranderingen in de hersenen bij HIV nog steeds belangrijk zijn
Moderne hiv-medicijnen laten veel mensen lang en gezond leven, maar toch krijgt tot de helft nog steeds subtiele problemen met geheugen, aandacht of stemming. Deze studie stelt een dringende vraag: wat gebeurt er in de hersenen, zelfs wanneer het virus onder controle is, wat zenuwcellen in de loop van de tijd stilletjes kan schaden? Met behulp van kleine in het laboratorium gekweekte “mini-hersenen” die menselijk hersenweefsel nabootsen, zoomen de onderzoekers in op hoe hiv en de immuuncellen van de hersenen met elkaar in wisselwerking treden en zowel ontsteking als cellulair energiegebruik verstoren op manieren die ten grondslag kunnen liggen aan deze aanhoudende klachten. 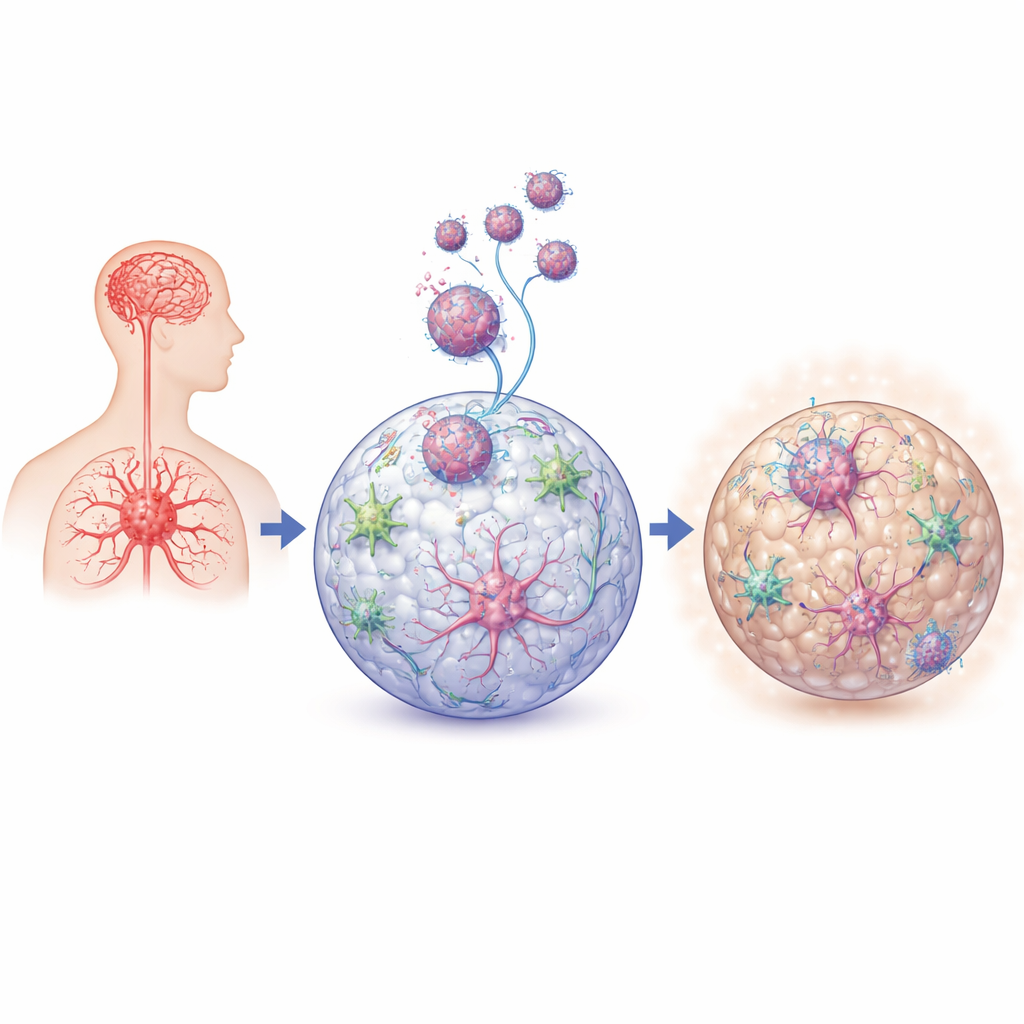
Mini-hersenen en de waakzame wachters van de hersenen
In plaats van volledige menselijke hersenen te bestuderen — wat bij levende mensen zelden mogelijk is — gebruikte het team driedimensionale neurale organoïden: erwtgrote bolletjes menselijk zenuwweefsel gekweekt uit stamcellen. In deze organoïden plaatsten ze microglia, de inheemse immuunwachters van de hersenen, die patrouilleren op bedreigingen en helpen gezonde verbindingen tussen neuronen te onderhouden. Vervolgens infecteerden ze microglia met een hiv-stam die bekendstaat om hersencellen te targeten en lieten deze geïnfecteerde microglia zich in de organoïden nestelen. Deze opzet creëerde een controleerbaar, menselijk model van vroege hiv-invasie in de hersenomgeving, waardoor de wetenschappers organoïden met en zonder microglia en met actief of inactief virus konden vergelijken.
Waar het virus zich verbergt en wie het raakt
Microscopiebeelden en virale metingen toonden aan dat het virus sterk repliceerde binnen microglia en dat virale eiwitten zich verspreidden naar aangrenzende cellen. Laatfase virale eiwitten werden niet alleen in microglia gevonden maar ook in stervormige ondersteunende cellen, astrocyten, terwijl neuronen zelf geen duidelijke tekenen van directe infectie lieten zien. Desondanks verschenen virale regulatoire eiwitten nabij neuronen, wat suggereert dat hiv hun gedrag indirect kan beïnvloeden. Organoïden die microglia bevatten, hadden veel hogere niveaus van viraal genetisch materiaal dan die zonder, wat de rol van microglia als een langlevend reservoir en versterker van hiv in de hersenen benadrukt.
Immuunalarmsignalen en een nieuwe doorgang voor hiv
Toen de onderzoekers onderzochten welke genen aan- of uitgezet werden, vonden ze dat hiv veel wijdere veranderingen teweegbracht wanneer microglia aanwezig waren. Honderden genen die gekoppeld zijn aan ontsteking en antivirale verdediging namen sterk in activiteit toe, inclusief routes die signaalmoleculen en de interferonrespons reguleren. Een opvallende bevinding was de sterke toename van een receptor genaamd CCR6, die als secundaire toegangspoort voor hiv kan dienen en ook de beweging van immuuncellen beïnvloedt. Merkers van astrocytenactivatie, vaak gezien bij hersenontsteking, waren eveneens verhoogd, terwijl bepaalde chemische boodschappers, zoals het chemokine CCL13, in de omliggende vloeistof stegen. Samen schetsen deze verschuivingen het beeld van een hersenweefselomgeving die zeer reactief en ontstekingsgericht wordt zodra hiv-geïnfecteerde microglia aanwezig zijn.
Veranderingen in brandstofgebruik binnen gestreste hersencellen
Buiten genactiviteit onderzocht het team hoe hiv de chemie van celmetabolisme verandert — de manier waarop cellen hun brandstof en bouwstenen beheren. Met behulp van computermodellen gebaseerd op de gendata brachten ze in kaart welke metabole reacties versnelden of vertraagden in geïnfecteerde organoïden. Ze ontdekten een kenmerkende "herbedrading" van aminozuurgebruik en -transport, vooral voor moleculen zoals arginine, proline, tryptofaan en de energiegerelateerde verbinding alfa-ketoglutaraat. Transporteiwitten die deze stoffen tussen cellulaire compartimenten verplaatsen, waren actiever in geïnfecteerde organoïden met microglia. De modellen suggereerden dat cellen sommige aminozuren exporteerden, andere omleiden naar alternatieve energieroutes, en meer tussenproducten naar mitochondriën duwden, alsof het weefsel onder metabole stress stond en probeerde te voldoen aan hoge energie-eisen. Dergelijke veranderingen kunnen glutamaatniveaus verhogen en de afbraak van tryptofaan verstoren — beide gekoppeld aan oxidatieve stress, verstoorde communicatie tussen neuronen en stemmings- en cognitieve problemen. 
Wat dit betekent voor mensen die met hiv leven
Samenvattend toont de studie aan dat hiv-geïnfecteerde microglia zowel immuunsignalen als energiehuishouding in nabijgelegen hersencellen kunnen herstructureren, zelfs zonder directe infectie van neuronen. Deze door microglia aangedreven "immunometabole" disbalans verzwakt waarschijnlijk het ondersteuningssysteem waarop neuronen vertrouwen, en bevordert chronische ontsteking en subtiele maar progressieve hersendysfunctie. Door vroege moleculaire en metabole veranderingen aan te wijzen — zoals CCR6-opregulatie en specifieke aminozuurverschuivingen — kunnen deze organoïdenmodellen helpen toekomstige biomarkers te identificeren om mensen met een hoger risico op hiv-gerelateerde cognitieve problemen te herkennen en therapieën te sturen die niet alleen tegen virale replicatie beschermen maar ook tegen de stille metabole belasting van de hersenen.
Bronvermelding: Capendale, P.E., Helgers, L.C., Ambikan, A.T. et al. Microglia cause HIV-induced transcriptional and metabolic changes in human neural organoids. Commun Biol 9, 436 (2026). https://doi.org/10.1038/s42003-026-09864-9
Trefwoorden: HIV en de hersenen, neurocognitieve stoornissen, microglia, hersenorganoïden, hersenmetabolisme