Clear Sky Science · nl
Het secreet-eiwit CLCF1 verbetert cholestatische leverziekte door remming van de hepatale galzuursynthese en bevordering van galzuurexcretie
Waarom dit onderzoek belangrijk is voor levergezondheid
Cholestatische leverziekten zijn aandoeningen waarbij gal, een spijsverteringsvloeistof die door de lever wordt gemaakt, niet goed afgevoerd wordt en zich in plaats daarvan ophoopt, waardoor de lever van binnenuit langzaam wordt vergiftigd. Huidige medicijnen helpen maar een deel van de patiënten en veel mensen hebben uiteindelijk een levertransplantatie nodig. Deze studie onthult een uiteraard geproduceerd eiwit, CLCF1 genaamd, dat het lichaam lijkt aan te zetten als een verdedigingsmechanisme tijdens cholestatische leverziekte. Inzicht in hoe dit eiwit werkt kan de weg wijzen naar nieuwe behandelingen die de lever beschermen door zowel de productie van schadelijke galcomponenten te verminderen als het lichaam te helpen ze efficiënter kwijt te raken.
Een verborgen helper in zieke levers
De onderzoekers begonnen met het onderzoeken van leverweefsel van patiënten met primaire biliary cholangitis en primaire sclerosing cholangitis, twee belangrijke vormen van chronische cholestatische leverziekte. Ze vergeleken mensen met vroege ziekte met degenen met geavanceerdere cholestase en analyseerden ook bestaande openbare gen-datasets. In deze onafhankelijke menselijke gegevensbronnen viel één geheim eiwit op: CLCF1 behoorde consequent tot de sterkst verhoogde genen in cholestatische levers. Hogere CLCF1-niveaus correleerden met slechtere bloedmarkers van ziekteernst, wat suggereert dat de lever dit eiwit opschroeft naarmate stress en galophoping erger worden. Bij patiënten in een vroeg stadium die behandeld werden met het standaardmiddel ursodeoxycholzuur, hadden degenen die goed reageerden vaak meer CLCF1 in hun lever, wat erop wijst dat dit eiwit mogelijk een meer aanpasbare, behandelbare lever markeert.
CLCF1 testen in diermodellen
Om verder te gaan dan menselijke correlaties, werkten de onderzoekers met muizen en gebruikten zowel genetische als dieet-gebaseerde modellen om cholestatische leverziekte na te bootsen. In twee verschillende muismodellen verhoogde cholestase sterk de productie van Clcf1 in de lever, wat de menselijke bevindingen weerspiegelt. Toen de wetenschappers specifiek de receptor voor CLCF1 uit levercellen verwijderden, verslechterde de cholestatische schade drastisch: galgangen groeiden excessief, leverweefsel stierf af, ontsteking nam toe, littekenweefsel stapelde zich op en toxische galzuren bouwden zich op. Het omgekeerde experiment liet een hoopvoller beeld zien. Toen het team een onschadelijk virus gebruikte om Clcf1 alleen in de lever te verhogen, waren de muizen beschermd. Hun levers zagen er gezonder uit, bloedwaarden verbeterden, littekenvorming nam af en de hoeveelheid galzuren die in de lever vastzat daalde aanzienlijk.
De kraan dichtdraaien en de afvoer openen
Hoe vermindert CLCF1 zo effectief een galzuuroverbelasting? De onderzoekers vonden twee aanvullende werkingen. Ten eerste kalmeerde CLCF1 rechtstreeks het galproducerende apparaat van de lever. In meerdere muismodellen en in gekweekte levercellen schakelde extra CLCF1 consequent belangrijke enzymen uit die cholesterol omzetten in galzuren, en draaide daarmee de kraan voor nieuwe galproductie dicht. Dit gebeurde zonder activering van de gebruikelijke leverregelaar voor gal, een nucleaire receptor genaamd FXR, wat suggereert dat CLCF1 een alternatieve route binnen levercellen gebruikt om de galsynthese te vertragen. Ten tweede beïnvloedde CLCF1 hoe gal verder in het lichaam werd verwerkt. Het herschikte de darmmicrobiota naar bacteriën die bijzonder goed zijn in het verwerken van galzuren en verhoogde de hoeveelheid galzuren die via de ontlasting het lichaam verlieten, wat fungeert als een sterkere afvoer.
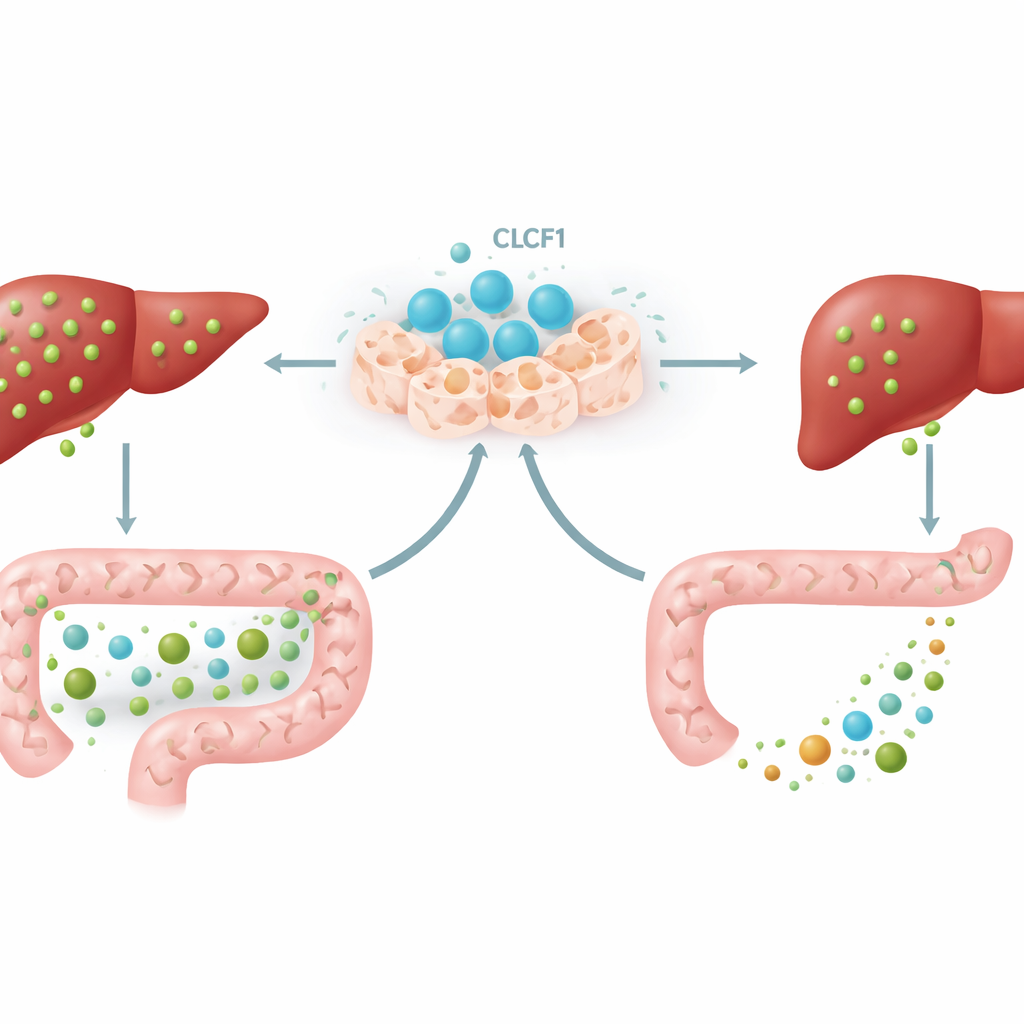
Het gesprek tussen darm en lever
Een belangrijk onderdeel van de verklaring betrof een signaleringslus tussen de darm en de lever. Bepaalde galzuren in het darmkanaal activeren een sensor genaamd FXR in darmslijmvliescellen, die vervolgens een boodschapperhormoon vrijgeven dat bij muizen FGF15 wordt genoemd. Dit hormoon reist via het bloed naar de lever en vertelt die om minder galzuren te produceren. Met extra CLCF1 stapelden muizen specifieke typen galzuren op in hun darmen—vooral vormen die sterke FXR-activatoren zijn. Daardoor werd intestinale FXR aangezet, stegen de FGF15-niveaus in zowel darm als lever, en dempte de lever nog verder zijn galzuurproductie. Toen wetenschappers intestinale FXR blokkeerden met een darm-beperkt geneesmiddel, verviel een groot deel van het beschermende effect van CLCF1, wat aantoont dat dit darm–lever-‘gesprek’ een essentieel onderdeel is van de werking van het eiwit.
Wat dit kan betekenen voor toekomstige behandelingen
Samen schetsen deze bevindingen CLCF1 als een ingebouwde veiligheidsklep voor cholestatische leverziekte. Het eiwit vermindert galzuurniveaus aan beide zijden: het vertraagt hun productie in de lever en bevordert hun verwijdering via de darm, geholpen door gunstige darmmicroben en een hormonaal feedbacksignaal. In tegenstelling tot bestaande medicijnen die FXR in het hele lichaam activeren en bijwerkingen kunnen veroorzaken zoals jeuk en afwijkende bloedvetten, lijkt CLCF1 galregulatie zachter en selectiever te sturen, vooral via de darm. Hoewel dit werk nog in muizen en laboratoriummonsters is uitgevoerd, suggereert het dat het versterken van CLCF1 of het nabootsen van zijn routes de basis kan vormen voor nieuwe therapieën—en dat het meten van dit eiwit, of de galzuren die het in de darm verrijkt, kan helpen om patiënten te identificeren die het meest zouden profiteren.
Bronvermelding: Liu, M., Su, Y., Hu, Y. et al. The secretory protein, CLCF1, improves cholestatic liver disease by inhibiting hepatic bile acid synthesis and promoting bile acid excretion. Commun Biol 9, 370 (2026). https://doi.org/10.1038/s42003-026-09847-w
Trefwoorden: cholestatische leverziekte, galzuren, darm–lever-as, CLCF1, darmmicrobioom