Clear Sky Science · nl
Het type VI-secretiestelsel van Acinetobacter: mechanismen, biologie en therapeutische mogelijkheden
Verborgen wapens in ziekenhuiskiemen
Veel mensen weten dat sommige ziekenhuiskiemen bestand zijn tegen antibiotica, maar minder beseffen dat deze microben ook felle onderlinge gevechten voeren. Deze review bekijkt een microscopische “veerbeladen speer” in Acinetobacter, een groep bacteriën waartoe de beruchte ziekenhuisbacterie Acinetobacter baumannii behoort. Begrijpen hoe dit ingebouwde wapen werkt, wanneer het wordt ingeschakeld en hoe het helpt bij het vestigen van infecties kan nieuwe wegen openen voor het opsporen en ontwapenen van levensbedreigende, medicijnresistente infecties.
Een overlevingsmachine, niet slechts een gifpijl
Acinetobacter-soorten leven in bodem, water en op onze huid, maar sommige zijn uitgegroeid tot zeer succesvolle ziekenhuispathogenen. Een belangrijk instrument in hun arsenaal is het Type VI-secretiestelsel, of T6SS, een klein contractiel apparaat verankerd in de celomhulling. Wanneer het afgaat, vuurt het een naaldachtige piek af die geladen is met toxische eiwitten naar naburige cellen, en vaak die concurrerende bacteriën op het contact doodt. In tegenstelling tot sommige andere microben die meerdere versies van dit systeem dragen, heeft pathogene Acinetobacter doorgaans maar één T6SS, maar heeft deze enkele opstelling zo aangepast dat hij vele doelen dient, van het afweren van concurrenten tot het vormen van infecties.
Hertekende hardware: een ongewone lanceerbasis
De meeste bacteriën bouwen hun T6SS rond een standaardset onderdelen, maar Acinetobacter heeft verschillende sleutelstukken verbouwd. Het mist een veelvoorkomende buitenmembraananker genaamd TssJ en vertrouwt in plaats daarvan op een trio gespecialiseerde helpers: TsmK vormt een fundament in het binnenmembraan, TslA stabiliseert een lang “tunnel” eiwit (TssM) terwijl het door de celwand loopt, en TagX snijdt lokaal door de wand om ruimte te maken voor het wapen. Daarbovenop moet een bepaald piekeiwit, VgrG1, bijna perfect van vorm zijn om het systeem überhaupt te laten vuren—enkele aminozuurveranderingen kunnen het uitschakelen. Samen laten deze aanpassingen zien hoe evolutie ontbrekende onderdelen kan vervangen door nieuwe oplossingen, terwijl het basisprincipe van afvuren behouden blijft.
Slimme besturing: wanneer aanval modus logisch is
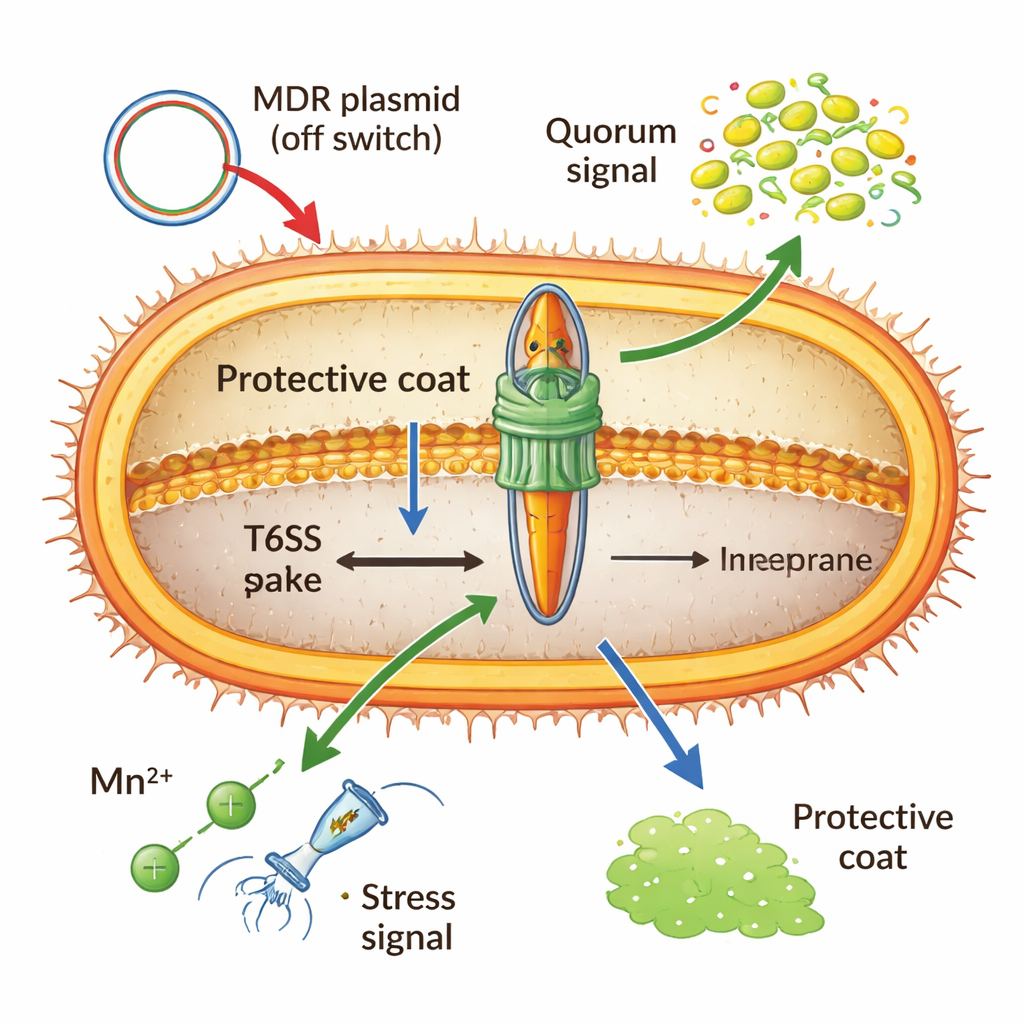
Het bouwen en afvuren van deze nanomachine kost veel energie, dus Acinetobacter houdt het onder strikte controle. Een globaal DNA-bindend eiwit (H-NS) en speciale repressoren op plasmiden die multiresistentie dragen, kunnen het systeem in de “uit” stand vergrendelen, vooral wanneer resistentiegenen tussen cellen worden uitgewisseld. Bij hoge celdichtheid kunnen chemische “quorum”-signalen het inschakelen, waardoor de bacteriën worden voorbereid op competitie op korte afstand. Metaalionen spelen ook een rol: onder oxidatieve stress activeert geïmporteerd mangaan een klein RNA dat ervoor zorgt dat belangrijke T6SS-boodschappen worden afgebroken, waardoor het wapen wordt gedimd ten behoeve van overleving in de gastheer. Zelfs de capsule—een suikerrijke buitenlaag—werkt zowel als schild als rem, doordat het inkomende aanvallen blokkeert maar ook fysiek het eigen afvuren van Acinetobacter dempt.
Een veelzijdige gereedschapskist van microscopische klappen
Wanneer Acinetobacter de trekker overhaalt, kan het een breed scala aan toxines afleveren. Sommige enzymen knagen door de stevige celwand van rivalen; andere tasten stilletjes celmembranen aan, en weer andere knippen DNA binnen doelcellen in stukken. Elk toxine is gekoppeld aan een passende “immuniteits”eiwit dat de aanvaller beschermt tegen eigen vuur. Eén DNA-knippert toxine, inmiddels TafE genoemd, kan zelfs schimmels doden, wat wijst op kruisdomeinconflicten in omgevingen zoals de darmen of longen. Genomische studies suggereren dat Acinetobacter nog veel meer, nog niet gekarakteriseerde toxines codeert, vaak gebundeld in grote Rhs-eiwitten die als modulaire dragers fungeren. In plaats van te vertrouwen op één klap, lijken deze bacteriën gelaagde aanvallen te gebruiken die meerdere essentiële structuren tegelijk beschadigen.
Infecties, genen en toekomstige behandelingen vormen
Bewijs uit isolates van patiënten en diermodellen suggereert dat een actief T6SS vaak samengaat met ernstigere ziekte, sterkere ontsteking en beter overleven van de bacteriën in gastheren. Door naburige microben te doden, komt er ook DNA vrij dat natuurlijk competente Acinetobacter-cellen kunnen opnemen, wat de verspreiding van eigenschappen zoals antibioticaresistentie versnelt. Toch is het constant actief houden van het wapen kostbaar, dus veel succesvolle ziekenhuisstammen dragen plasmiden of mutaties die het stilzetten zodra resistentie veiliggesteld is. Over het geheel genomen betogen de auteurs dat dit secretiestelsel niet simpelweg moet worden gezien als een virulentiefactor, maar als een flexibel “fitnessmodule” dat Acinetobacter omhoog of omlaag afstelt om agressie, persistentie en energiegebruik in balans te brengen. Deze nieuwe kijk wijst op praktische toepassingen, van vaccins die op geconserveerde T6SS-onderdelen mikken tot medicijnen die selectief het afvuurmechanisme blokkeren, waardoor artsen een gevaarlijke en zich aanpassende ziekenhuisvijand te slim af kunnen zijn.
Bronvermelding: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Trefwoorden: Acinetobacter, type VI-secretiestelsel, antibioticaresistentie, bacteriële competitie, ziekenhuisinfecties