Clear Sky Science · nl
Glycosylering als dynamische regulator van RLR- en cGAS-STING-geïnduceerde aangeboren immuunsignaalroutes
Hoe suikertags cellen helpen virussen te detecteren
Onze cellen houden voortdurend toezicht op binnendringende virussen, en een groot deel van deze verdediging berust op kleine suikertags die aan eiwitten zijn gebonden. Deze review legt uit hoe deze suikertags, bekend als glycosylering, meer als dimmers functioneren dan als eenvoudige aan/uit-knoppen voor belangrijke antivirale routes. Inzicht in deze op suikers gebaseerde fijnregeling kan nieuwe wegen openen om vaccins te versterken, virale infecties te behandelen en het immuunsysteem tegen kanker in te zetten.
Het vroege waarschuwingssysteem van de cel
Wanneer virussen een cel binnendringen, laten ze herkenbare stukjes RNA of DNA achter. Gespecialiseerde "alarmsystemen" patrouilleren in het celinterieur op dit genetische afval. Eén systeem, het RIG-I-achtige receptorpad (RLR), detecteert viraal RNA. Een ander, bekend als het cGAS–STING-pad, voelt DNA op dat op de verkeerde plaats in de cel verschijnt. Zodra ze geactiveerd zijn, zetten beide routes chemische cascades in gang die eindigen in de afgifte van type I interferonen en ontstekingsmoleculen—krachtige signalen die naburige cellen waarschuwen en immuunreacties oproepen. Omdat te veel of te weinig van deze respons schadelijk kan zijn, moet de cel deze alarmen zorgvuldig afstemmen, en glycosylering is een van de sleutelmechanismen daarvoor. 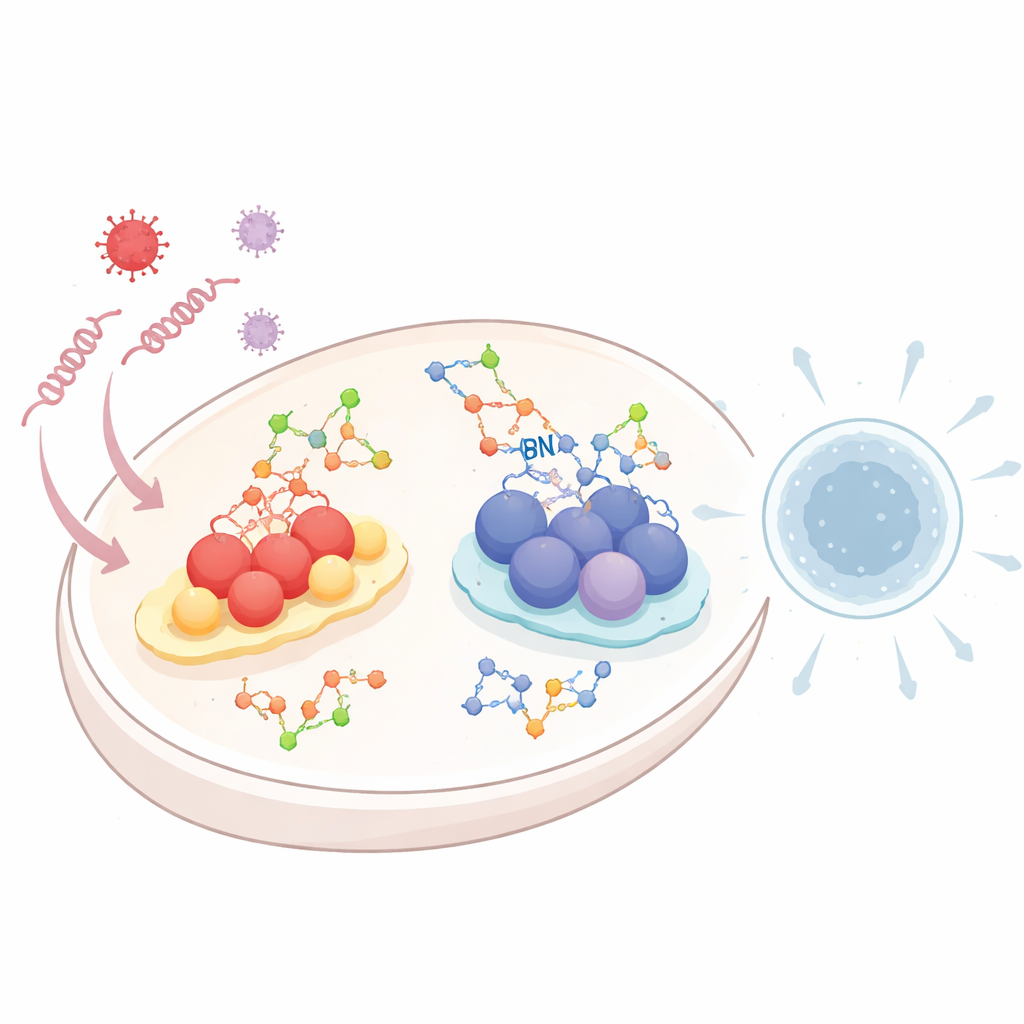
Suikerkappen als precisiecontroles
Glycosylering voegt kleine suikereenheden toe aan eiwitten op verschillende locaties in de cel. In het interne vervoersnetwerk van de cel, het endoplasmatisch reticulum en het Golgi-apparaat, helpen omvangrijke N-gebonden suikerketens eiwitten bij het correct vouwen, het behouden van stabiliteit en het vervoeren naar het juiste membraan. Daarentegen plaatst een slankere vorm, O-GlcNAcylatie, een enkel suikerrestje op eiwitten in het cytoplasma en de kern. Deze minimalistische tag is zeer dynamisch en wordt snel vernieuwd doordat twee enzymen hem toevoegen of verwijderen als reactie op nutriëntenniveaus en stress. De review beschrijft hoe deze verschillende suikertypes niet simpelweg immuunsensoren aan of uit zetten; in plaats daarvan regelen ze hoe gemakkelijk sensoren samenklonteren, hoe lang ze blijven bestaan en hoe sterk ze signaleren. Op die manier koppelt glycosylering de metabole toestand van de cel direct aan haar paraatheid om infecties te bestrijden.
Het afstemmen van de RNA-sensorroute
Binnen het RNA-detecterende RLR-systeem fungeert een centraal relais-eiwit, MAVS, dat op mitochondriën zit, als een belangrijk knooppunt. De review laat zien dat O-GlcNAcylatie op MAVS zowel antivirale signalering kan versnellen als afremmen, afhankelijk van waar het suikerrestje wordt aangebracht. Suikertags op bepaalde locaties bevorderen verdere eiwitmodificaties, zoals een specifiek type ubiquitineketen, die helpen dat MAVS grote signaalclusters vormt en sterke interferonproductie aandrijft tegen RNA-virussen. Andere suikerlokaties houden MAVS onder normale omstandigheden verspreid en inactief, waardoor onnodige ontsteking wordt voorkomen. Virale infectie en veranderingen in het suikerproducerende metabole pad van de cel kunnen het evenwicht tussen deze activerende en remmende tags verschuiven. Verwante modificaties op een andere factor, IRF5, kunnen het immuunsysteem richting schadelijke "cytokinestormen" duwen, wat benadrukt dat meer suiker niet per se beter is. Tegelijkertijd kunnen virussen N-gebonden suikers op celoppervlakte-eiwitten zoals de groeifactorreceptor EGFR exploiteren om upstream-sensoren zoals RIG-I te markeren voor afbraak, waardoor antivirale verdediging wordt verzwakt.
Het afstemmen van de DNA-sensorroute
Ook de DNA-detecterende cGAS–STING-route wordt sterk beïnvloed door glycosylering. STING, een membraaneiwit in het endoplasmatisch reticulum, heeft N-gebonden suikerketens nodig om goed te vouwen, stabiel te blijven en, eenmaal geactiveerd door DNA-afgeleide boodschappers, samen te klonteren tot signaalvormende complexen. Zonder deze suikers lukt het STING niet om de hogere-orde structuren te vormen en door de celcompartimenten te trafficken die nodig zijn voor robuuste interferonvrijgave. Tegelijkertijd versterkt O-GlcNAcylatie van STING op een specifieke plaats een andere set chemische tags die clustering en verplaatsing bevorderen, wat antivirale signalen tegen DNA-virussen versterkt. Suikerrijke ketens, sulfaat-bevattende glycosaminoglycanen gebouwd in het Golgi, helpen bovendien door geactiveerd STING te helpen polymeriseren tot lange structuren die downstream-enzymen rekruteren. Virussen voeren tegenaanvallen uit door hun eigen glycoproteïnen te veranderen of door afbraakpaden te activeren die STING richten, vaak in dezelfde cellulaire ruimtes waar deze suikerdecoraties worden toegevoegd of verwerkt. 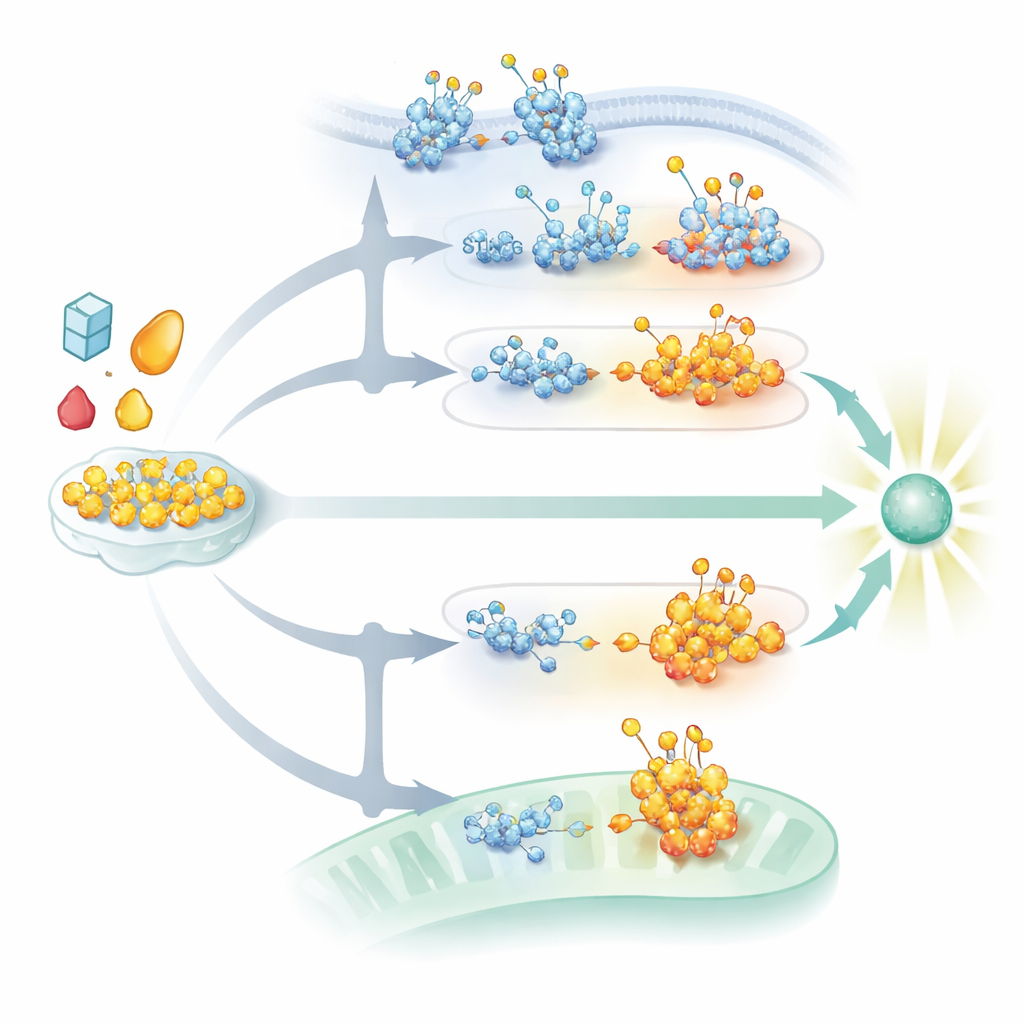
Metabolisme, ziekte en toekomstige therapieën
Aangezien de belangrijkste suiverdonor voor O-GlcNAcylatie wordt geproduceerd via een metabole route die bekend staat als de hexosamine-biosynthetische route, beïnvloeden verschuivingen in nutriëntengebruik rechtstreeks antivirale signaalgeving. Veel virussen stimuleren dit pad in hun voordeel, terwijl experimenteel verhogen of blokkeren van de hexosamineflux antivirale reacties in diermodellen kan versterken of verzwakken. De review verbindt deze mechanismen met menselijke ziekte: tumoren herprogrammeren vaak glycosylering om interferonsignalen te dempen en zo aan immuunaanvallen te ontsnappen, terwijl chronische metabole stress of erfelijke defecten in glykaanverwerking het evenwicht naar schadelijke autoimmuunreacties kunnen kantelen. De auteurs betogen dat enzymen die glycosylering controleren—vooral diegenen die O-GlcNAc toevoegen of verwijderen of belangrijke N-gebonden structuren opbouwen—veelbelovende maar uitdagende geneesmiddeldoelen zijn. Toekomstige therapieën zullen waarschijnlijk site-specifiek en contextbewust moeten werken, de "glyco-code" in de richting van betere bescherming tegen infecties, kanker en ontstekingsaandoeningen bijsturen zonder nieuwe vormen van immuundisbalans te veroorzaken.
Het grote plaatje voor dagelijkse gezondheid
In gewone bewoordingen laat dit artikel zien dat de frontlinie antivirale alarmen van het lichaam niet in isolatie werken—ze zijn verbonden met het energieverbruik en de suikerchemie van de cel. Kleine suikertags op een handvol kritische eiwitten beslissen of een verdwaald viraal genoom een gematigde waarschuwing, een volledige verdediging of een gevaarlijke overreactie veroorzaakt. Door dit op suikers gebaseerde controlesysteem te ontcijferen en uiteindelijk te leren bijstellen, hopen onderzoekers behandelingen te ontwerpen die vaccins effectiever maken, hardnekkige infecties helpen verwijderen, tumoren blootleggen aan het immuunsysteem en weglopende ontsteking bij auto-immuunziekten tot rust kunnen brengen.
Bronvermelding: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
Trefwoorden: aangeboren immuniteit, glycosylering, RLR-route, cGAS-STING, O-GlcNAcylatie