Clear Sky Science · nl
Groeisnelheid-gestuurde modellering suggereert dat fenotypische aanpassing medicijnresistentie veroorzaakt in BRAFV600E-gemuteerde melanoom
Kankercellen die leren omgaan met medicijnen
Gerichte geneesmiddelen hebben de behandeling van veel mensen met melanoom, een ernstige vorm van huidkanker, ingrijpend veranderd. Toch houden deze middelen vrijwel altijd op met werken: tumoren die eerst krimpten beginnen weer te groeien. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen melanocyten, naast het ontwikkelen van genetische mutaties, ook "leren" te overleven door hun gedrag aan te passen — en kan dat leren verklaren waarom bepaalde toedieningswijzen beter werken dan andere?
Van gevoelige cellen naar overlevers
De onderzoekers richtten zich op melanoomcellen met een veelvoorkomende verandering in het gen BRAF, waardoor ze bijzonder gevoelig zijn voor een klasse medicijnen genaamd BRAF-remmers. In eerder laboratoriumwerk werden deze cellen blootgesteld aan het middel encorafenib in verschillende doses en gedurende verschillende tijdsduur. Door nauwkeurig te meten hoe snel de cellen groeiden of stierven onder elke conditie, verdeelden de auteurs de cellen in grofweg twee categorieën: medicijn-naieve cellen die het middel nooit hadden gezien, en medicijn-geadaptateerde cellen die minstens een week in het middel hadden geleefd. Medicijn-naieve cellen groeiden goed zonder behandeling maar werden sterk geremd of gedood door het middel. Medicijn-geadaptateerde cellen groeiden daarentegen beter in aanwezigheid van het middel maar verloren dat voordeel wanneer het middel werd verwijderd — wat suggereert dat hun overleving verbonden was aan een flexibele, omkeerbare toestandsverandering in plaats van aan blijvende genetische schade.
Een kaart van verborgen celgedrag
Om deze veranderingen te begrijpen bouwde het team een wiskundig model waarin elke kankercel een "fenotype-toestand" krijgt toegewezen — een abstracte positie op een schaal van zeer medicijngevoelig tot zeer medicijnresistent. In plaats van alleen twee celtypen te veronderstellen, lieten ze veel tussentoestanden toe, die geleidelijke gedragsverschuivingen weerspiegelen zoals waargenomen in biologische markers van resistentie. Voor elke combinatie van toestand en medicijndosis schatten ze een netto groeisnelheid, die positief (meer delingen dan sterfte) of negatief (meer sterfte dan delingen) kan zijn. Al deze snelheden werden gerangschikt in een raster, een "fitheidsmatrix," die werkt als een landschap: sommige toestanden bij bepaalde doses zijn gunstige plekken om te gedijen, andere zijn dodelijk. Cellen in het model kunnen stap voor stap over dit landschap bewegen naarmate de behandeling aan- of uitgezet wordt.
Drijven cellen of klimmen ze naar voordeel?
Het belangrijkste onbekende was hoe cellen zich over dit landschap verplaatsen. De auteurs testten vier mogelijke strategieën. In de ene veranderen cellen nooit van toestand, zodat resistente cellen vanaf het begin aanwezig moeten zijn. In een andere dwalen cellen willekeurig tussen aangrenzende toestanden, als een zwerftocht, ongeacht of hun situatie verbetert. In de twee overige strategieën neigen cellen te bewegen naar toestanden waar hun groeisnelheid hoger is — ofwel met ruis, met enkele misstappen, of krachtig, altijd klimmend naar betere overleving. Wanneer het team computersimulaties draaide en die vergeleek met echte laboratoriumdata, vooral experimenten waar het middel continu of in een aan–uit-patroon (één week aan, één week uit) werd gegeven, konden alleen de strategieën waarbij cellen klimmen naar hogere fitheid reproduceren wat werd waargenomen: intermitterende behandeling met een hoge dosis onderdrukte het aantal cellen beter dan continue behandeling met dezelfde totale tijd en een grotere totale hoeveelheid medicijn.
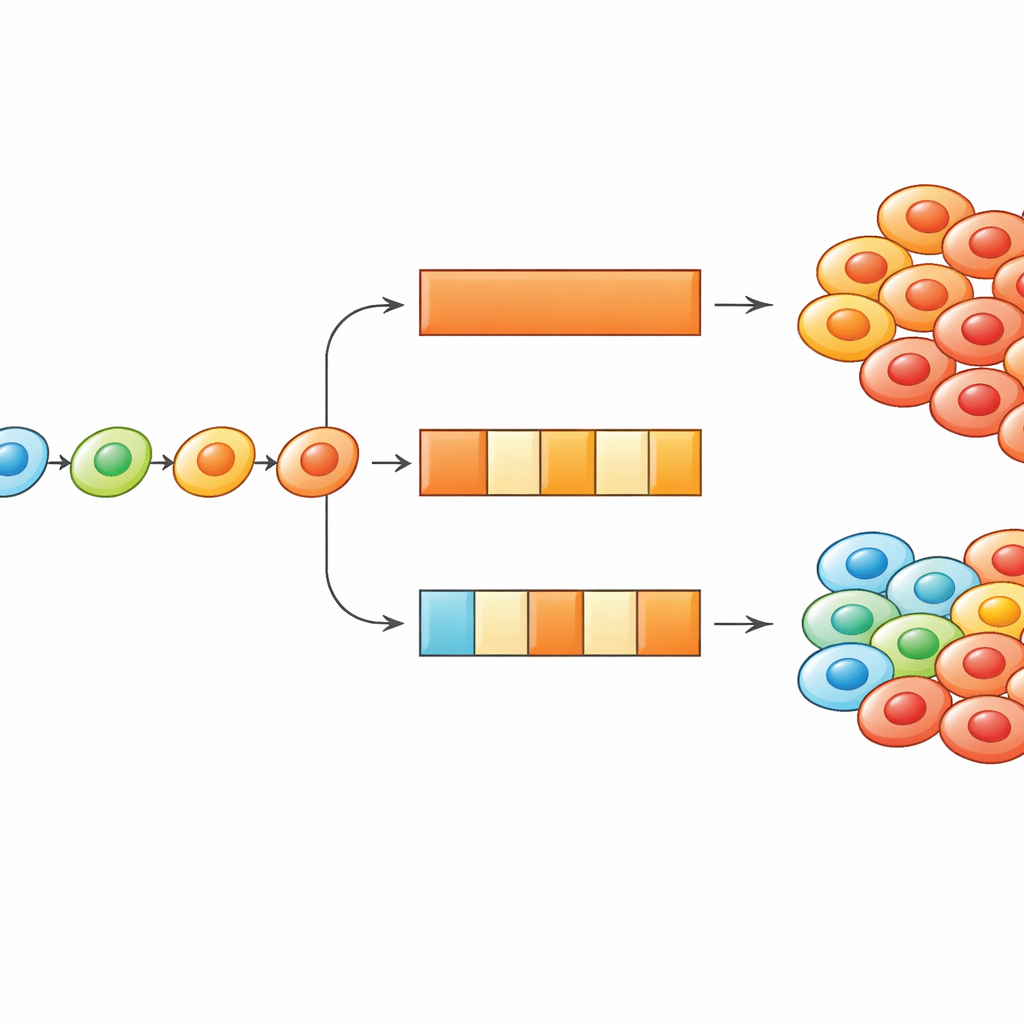
Gebruik van aan–uit dosering om adaptatie tegen kanker te keren
Dieper gravend gebruikten de onderzoekers zowel simulaties als eenvoudigere vergelijkingen om te onderzoeken hoe vaak cellen hun toestand mogen veranderen en hoe lang medicijn-aan- en medicijn-uit-periodes duren. Ze vonden dat wanneer cellen zich op een gerichte manier aanpassen, behandelschema's kunnen worden afgestemd om deze adaptatie ofwel te vertragen of juist uit te buiten. Het verkorten van de frequentie waarmee cellen hun toestand kunnen bijwerken — conceptueel het vertragen van de biologische mechanismen die fenotypische verandering mogelijk maken — maakt intermitterende behandelingen doorgaans krachtiger, omdat cellen niet zo snel naar sterk resistente toestanden kunnen klimmen. Omgekeerd, als cellen beginnen in een sterk resistente toestand, kunnen medicijnpauzes ze de tijd geven terug te glijden naar meer gevoelige toestanden, zodat het opnieuw toedienen van het middel een golf van celdood veroorzaakt. De studie toont hoe de timing van dosering en de snelheid van cellulaire adaptatie samen bepalen welk schema het beste werkt.
Wat dit betekent voor toekomstige kankerzorg
Voor een leek is de kernboodschap dat kankercellen niet louter vaste vijanden zijn; het zijn vormveranderaars. In dit melanoomsysteem lijken de cellen actief toe te bewegen naar gedragingen die hen helpen groeien onder de heersende omstandigheden. Het model van de auteurs suggereert dat deze gerichte adaptatie op zichzelf — zonder het aannemen van verschillende permanente klonen — kan verklaren waarom aan–uit medicatieschema's soms beter presteren dan constante dosering, zelfs wanneer ze in totaal minder medicijn gebruiken. Hoewel deze resultaten afkomstig zijn van in vitro cellen en meer onderzoek nodig is voordat ze patiëntenbehandeling kunnen sturen, biedt de aanpak een praktisch kader: door te meten hoe snel en in welke richting kankercellen zich aanpassen, kunnen artsen mogelijk behandelschema's ontwerpen die niet alleen tumoren aanvallen maar ook hun fenotypische "leerproces" richting doodlopende wegen sturen in plaats van ontsnappingsroutes.
Bronvermelding: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Trefwoorden: melanoom, medicijnresistentie, cellulaire plasticiteit, intermitterende therapie, wiskundige modellering