Clear Sky Science · nl
Structurele basis van activatie door dimerisatie van de quinol-afhankelijke stikstofoxidereductase van Neisseria meningitidis
Hoe bacteriën ons immuunsysteem te slim af zijn
Wanneer ziekteverwekkende bacteriën het lichaam binnendringen, zetten onze immuuncellen toxische moleculen zoals stikstofoxide vrij om ze te doden. Sommige pathogenen hebben echter moleculaire trucs ontwikkeld om deze aanval te neutraliseren en te overleven. Deze studie onthult op atomaire schaal hoe een sleutelenzym van de bacterie zichzelf herconfigureert tot paren om veel beter stikstofoxide te ontgiften, en waarom begrip van dit vormveranderende gedrag nieuwe wegen naar antibioticumontwerp kan openen.
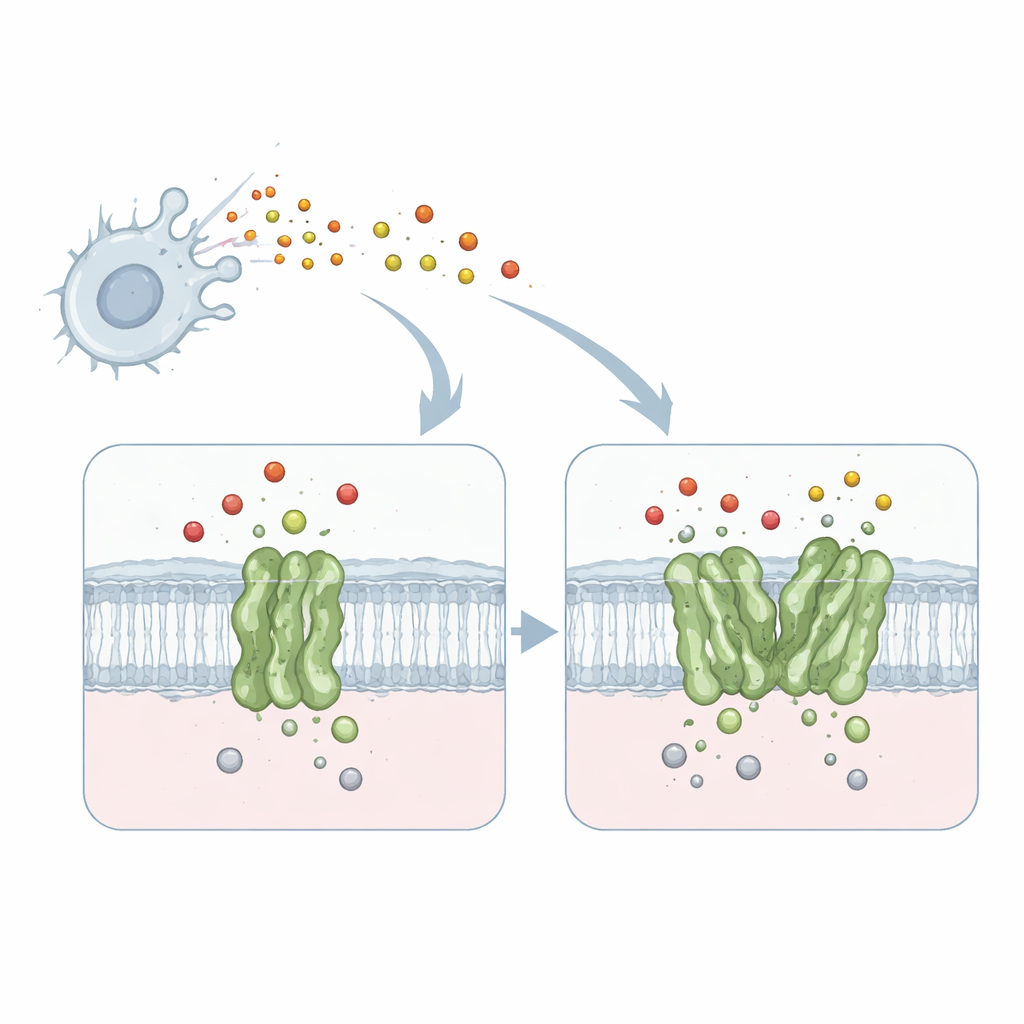
Een klein apparaat dat een toxisch gas deactiveert
Het werk richt zich op een membraaneiwit dat quinol-afhankelijke stikstofoxidereductase heet, of qNOR, afkomstig van de meningitisveroorzakende bacterie Neisseria meningitidis. qNOR zit in het bacteriële celmembraan en zet stikstofoxide — een toxisch gas geproduceerd door ons immuunsysteem — om in minder schadelijke producten. Deze ontgifting stelt de microbe in staat te blijven ademen en groeien, zelfs in vijandige omgevingen zoals menselijke macrofagen. Omdat ademhaling en verwijdering van stikstofoxide vitaal zijn voor het overleven van de pathogeen, is qNOR een aantrekkelijk doelwit voor nieuwe antimicrobiële middelen.
Één is goed, maar twee zijn beter
Eerdere biochemische studies toonden aan dat qNOR zowel als enkelvoudige eenheid (monomeer) als als paar (dimeer) kan voorkomen, en dat het dimeer twee- tot viermaal sneller werkt bij het neutraliseren van stikstofoxide. Tot nu toe was onduidelijk waarom het simpelweg samenvoegen van twee kopieën van hetzelfde enzym zo’n dramatisch effect op de prestatie had. Om dit te beantwoorden gebruikten de onderzoekers hoogresolutie single-particle kryo-elektronenmicroscopie om gedetailleerde driedimensionale structuren van zowel monomere als dimerische qNOR uit dezelfde bacteriestam vast te leggen. Ze verkregen bijna-atomaire resoluties — 1,89 ångström voor het dimeer en 2,25 ångström voor het monomeer — scherp genoeg om individuele aminozuurzijgroepen, metaalionen en veel watermoleculen te lokaliseren.
Een flexibele helix wordt een stabiliserende beugel
Verrassend genoeg leek het katalytische hart van het enzym — het metaalcentrum waar stikstofoxide wordt omgezet — in beide vormen vrijwel identiek. De sleutelverschillen deden zich in plaats daarvan op enige afstand voor, in een transmembrane helix genaamd TM10 en in hoe deze contact maakt met een andere helix (TM2) wanneer twee qNOR-moleculen paaren. In het monomeer is TM10 los verankerd en kan het aanzienlijk zwiepen en buigen, zoals aangetoond door computationele analyse van de kryo-EM-gegevens. In het dimeer vergrendelt TM10 van elke partner tegen de buurhelix om een bundel van vier helixen te vormen, waardoor de beweging sterk wordt beperkt. Deze stabilisatie herpositioneert subtiel een cruciaal aminozuur, een glutamaat genaamd Glu563, waardoor het dichter bij een ander glutamaat (Glu494) nabij het actieve centrum komt te liggen en zo een meer gefocuste route vormt voor binnenkomende protonen die voor de reactie nodig zijn.
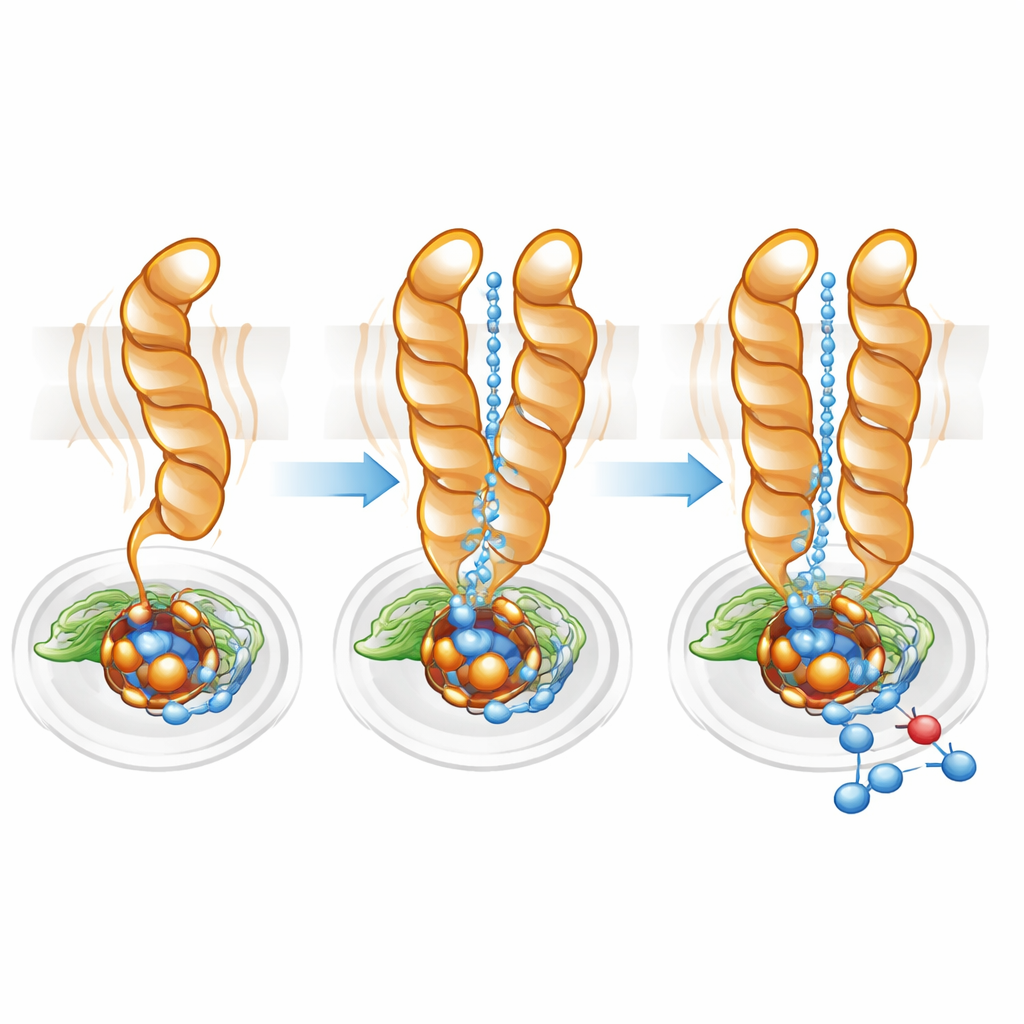
Het fijnregelen van de protonenweg
Protonen — positief geladen waterstofionen — moeten efficiënt van het celinterieur naar het begraven actieve centrum worden geleverd zodat de reductie van stikstofoxide kan verlopen. Met behulp van padmapping-software vond het team een hydrofiele holte die het cytoplasma met het actieve centrum verbindt in zowel monomeer als dimeer. In het monomeer was dit kanaal echter breder en diffuuser, in overeenstemming met de grotere mobiliteit van TM10. In het dimeer hielpen de vergrendelde positie van TM10 en de gunstige oriëntatie van Glu563 een directer en beter georganiseerd pad te definiëren. Het muteren van Glu563 naar aminozuren die niet dezelfde interacties kunnen vormen, sneed de enzymactiviteit terug tot minder dan 10% van normaal en destabilisereerde ook het dimeer, terwijl mutaties op gerelateerde posities de hoeveelheid essentieel non-heemijzer in het actieve centrum verminderden. Gezamenlijk tonen deze resultaten aan dat dimeervorming en de precieze positionering van Glu563 en Glu494 sterk gekoppeld zijn aan zowel structurele integriteit als katalytische efficiëntie.
Structurele inzichten omzetten in nieuwe behandelingen
De bevindingen laten een duidelijke lijn zien van eiwitparing aan het membraanoppervlak tot fijne aanpassingen diep in het actieve centrum die bepalen hoe effectief qNOR stikstofoxide verwijdert. In eenvoudige bewoordingen: wanneer twee kopieën van het enzym zich vastklampen, richten ze een flexibel segment op en verstevigen het, waardoor protonen beter naar het reactiemiddel worden geleid en de output van het enzym toeneemt. Voor geneesmiddelenontwikkeling suggereert dit een onconventionele strategie: in plaats van het actieve centrum direct te blokkeren, zou men moleculen kunnen ontwerpen die het dimeer uit elkaar wrikken of de Glu563–Glu494-interactie verstoren, waardoor het enzym in zijn trage monomere toestand wordt geforceerd. Omdat qNOR en verwante enzymen cruciaal zijn voor het overleven van verschillende gevaarlijke, medicijnresistente pathogenen, kunnen dergelijke structuurgeleide benaderingen bijdragen aan de volgende generatie gerichte antimicrobiële middelen.
Bronvermelding: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Trefwoorden: ontgifting van stikstofoxide, bacteriële ademhaling, membraanenzymen, kryo-elektronenmicroscopie, doelen voor antimicrobiële middelen