Clear Sky Science · nl
Ruimtelijke multiomics onthult door irreversibele elektroporatie veroorzaakte immuno‑metabole kenmerken van de ontstekingsrand bij leverkanker
Waarom een nieuwe behandeling voor leverkanker nader onderzoek nodig heeft
Irreversibele elektroporatie (IRE) is een nieuwere methode om levertumoren te vernietigen met korte, hoogspanningspulsen in plaats van warmte. Omdat het nabijgelegen bloedvaten en galwegen kan sparen, is het vooral nuttig voor tumoren op kwetsbare locaties. Toch keert de tumor bij tot een derde van de patiënten terug direct naast het behandelde gebied. Deze studie onderzoekt wat er in die smalle grenszone na IRE gebeurt — en of onzichtbare veranderingen in immuuncellen en celmetabolisme daar stilletjes het decor klaarzetten voor herval van de kanker.
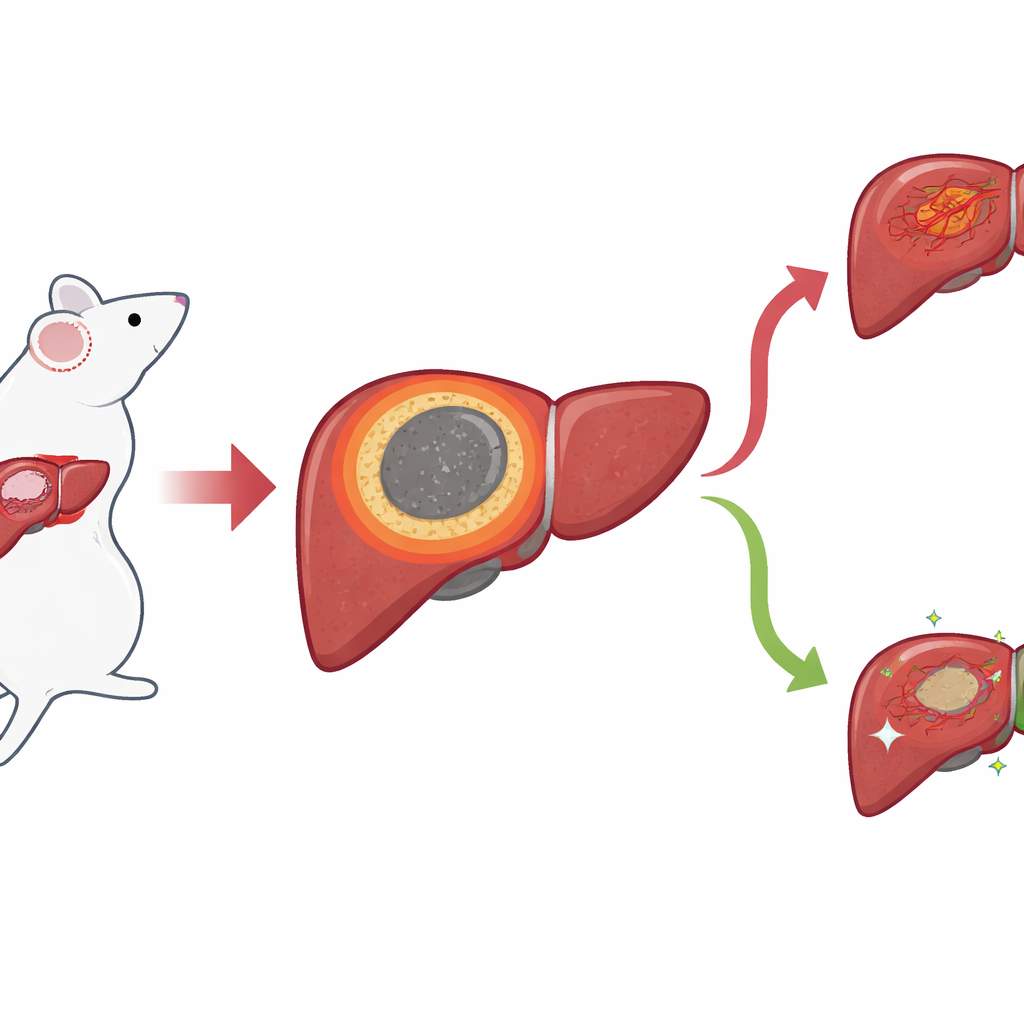
Een smalle rand met grote gevolgen
Met behulp van een muismodel voor leverkanker richtten de onderzoekers zich op de dunne ring weefsel die zich vormt tussen de dode, geablateerde kern en de omliggende gezonde lever na IRE. Zij noemen dit de ontstekingsrand, of IM. Standaardmicroscoopbeelden toonden aan dat deze zone precies daar ligt waar lokale recidieven gewoonlijk verschijnen, maar de grenzen waren met het blote oog moeilijk te bepalen. Om een scherper beeld te krijgen, pasten de onderzoekers ruimtelijke methoden toe die aangeven welke genen en kleine moleculen aanwezig zijn en tegelijk hun locatie in het weefsel behouden. Met ruimtelijke transcriptomica brachten ze genactiviteit plek voor plek in kaart en ontdekten een duidelijke cluster van plekken die precies samenviel met de IM en de necrotische kern scheidde van normaal lever- en tumorgewebe.
Immuuncellen verzamelen zich — maar velen remmen de aanval
Vervolgens gebruikten de wetenschappers single‑cell en single‑nucleus RNA‑sequencing, samen met een krachtige profielmethode genaamd CyTOF, om individuele celtypen door de lever heen in kaart te brengen. Ze vonden dat de IM wordt gedomineerd door een type immuuncel dat macrofagen wordt genoemd. Met name een subpopulatie die leek op "lipid‑associated macrophages" (LAMs) trok binnen enkele dagen na IRE massaal de IM binnen. Deze cellen dragen oppervlaktemarkers en genexpressiesignaturen die samenhangen met immuunsuppressie, waaronder hoge niveaus van PD‑L1, een molecuul dat bekendstaat om het dempen van T‑celreacties. Genexpressieanalyses suggereerden dat deze macrofagen bedreven zijn in het insluiten van materiaal, het reageren op chemische aantrekstoffen en het uitzenden van signalen die juist de T‑cellen kunnen beperken die nodig zijn om kankercellen te doden. Beelden bevestigden dat PD‑L1‑positieve macrofagen veel talrijker waren in de IM dan in nabijgelegen normaal weefsel.
Een brandpunt van veranderde vetchemie
Daarna legde het team dit immuunlandschap over elkaar heen met ruimtelijke metabolomica, een massa‑spectrometriebeeldvormingsbenadering die de verdeling van honderden kleine moleculen in kaart brengt. Ze toonden aan dat de IM een metabolisch vingerafdruk heeft die verschilt van zowel de dode kern als de omliggende lever. In deze smalle band waren veel lipidenroutes sterk versterkt, waaronder de productie van onverzadigde vetzuren, derivaten van arachidonzuur en sphingolipiden. Belangrijke signaalvetten zoals prostaglandinen en leukotriënen, afgeleid van arachidonzuur, waren verrijkt in de IM, terwijl andere enzymroutes voor de verwerking van hetzelfde molecuul relatief zwakker waren. Een andere lipidenfamilie, sphingolipiden — waaronder ceramiden en sphingomyelinen — stapelde zich ook op, ondersteund door verhoogde expressie van enzymen die ze maken en ombouwen.
Een stapsgewijze verschuiving van schade naar brandstofrijk niche
Door de ontstekingsrand in drie dunne lagen te verdelen van de necrotische kern naar buiten, zagen de onderzoekers een geleidelijke verschuiving in chemie. Dichtbij de dode zone waren complexe lipiden en cholesterolgerelateerde moleculen het hoogst, terwijl verder naar buiten kleine energierelateerde moleculen zoals glucose en bepaalde aminozuren toenamen. Dit patroon suggereert dat het weefsel over een korte afstand transformeert van een lipid‑geladen, signaalrijke omgeving naar een omgeving gericht op het voorzien in brandstof voor celoverleving en -groei. De auteurs stellen dat deze stapsgewijze herprogrammering helpt de lipiden‑hongerige, immunosuppressieve macrofagen in stand te houden die de IM domineren en stilletjes de grond kunnen voorbereiden voor tumorcellen om zich opnieuw te vestigen.
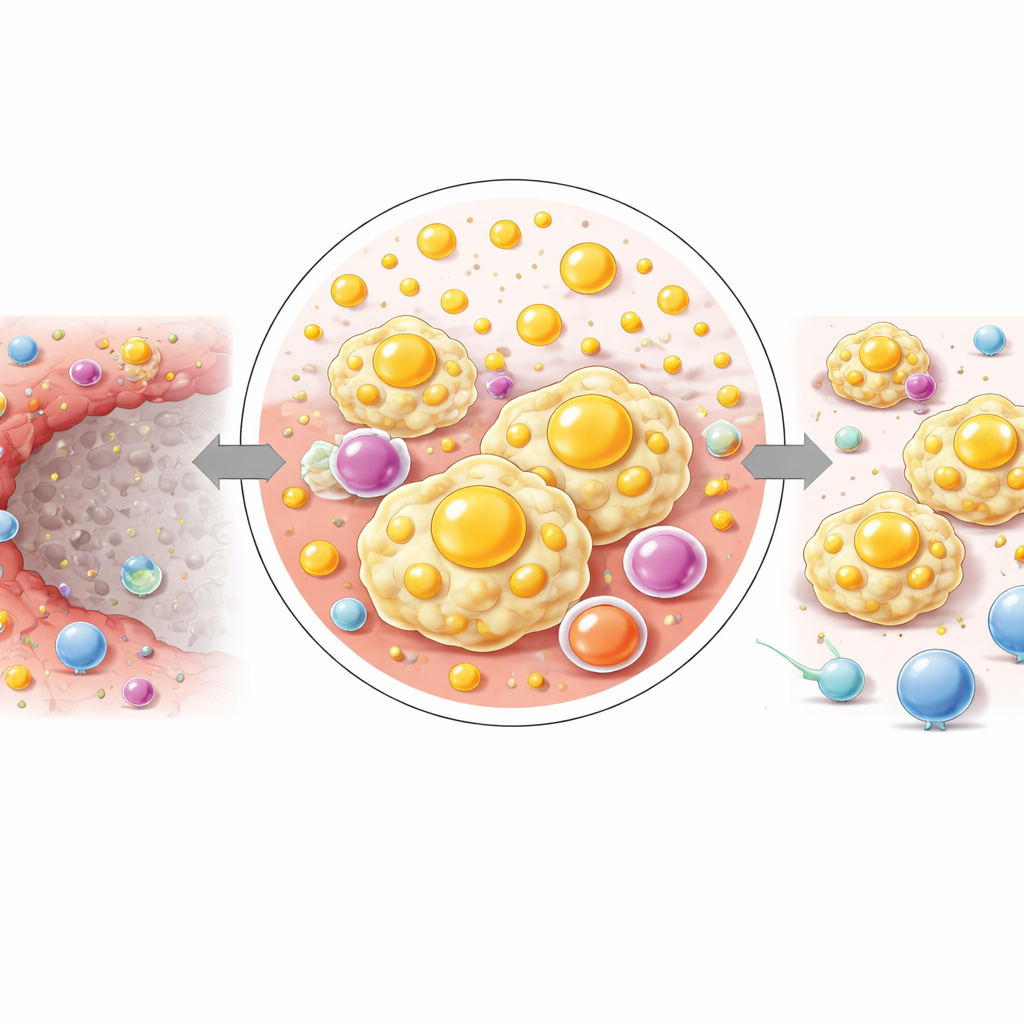
Wat dit betekent voor toekomstige zorg bij leverkanker
In eenvoudige bewoordingen laat dit werk zien dat IRE meer doet dan alleen tumorcellen doden: het creëert ook een smalle ring weefsel waar immuuncellen en vetchemie samen een afgeschermde, tumorvriendelijke buurt vormen. Macrofagen in deze zone zijn talrijk, volgeladen met lipiden en geneigd T‑cellen uit te schakelen in plaats van te helpen. Omdat deze veranderingen sterk verbonden zijn met specifieke metabole routes, wijzen ze op nieuwe behandelrichtingen. Het combineren van IRE met geneesmiddelen die het lipidenmetabolisme remmen of PD‑L1 blokkeren in deze rand zou in principe een recidiefgevoelige zone kunnen veranderen in een gebied dat de klus tegen leverkanker daadwerkelijk klaart.
Bronvermelding: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Trefwoorden: leverkanker, tumorablatie, immuunmicro‑omgeving, macrofagen, lipidenmetabolisme