Clear Sky Science · nl
NRF2-activatoren en de remmer van nucleaire export, selinexor, beperken coronavirussen door een netwerk te richten dat ACE2, TMPRSS2 en XPO1 omvat via een NRF2-onafhankelijke route
Medicijnen die cellen helpen “nee” te zeggen tegen coronavirussen
De meeste coronavirusbehandelingen richten zich tegenwoordig op het virus zelf. Maar virussen zijn meesters in veranderen, en nieuwe varianten kunnen die middelen snel minder effectief maken. Deze studie onderzoekt een andere strategie: onze eigen cellen minder gastvrij maken voor zowel gevaarlijke coronavirussen zoals SARS-CoV-2 als mildere seizoensstammen. Door te sleutelen aan hoe cellen enkele belangrijke poortwachter-eiwitten behandelen, laten de onderzoekers zien dat bestaande kleine moleculen infectie in laboratoriummodellen sterk kunnen verminderen, en dat ze dit doen op een manier die niet afhankelijk is van het antivirale pad waarvoor ze oorspronkelijk bekend waren.
Een nieuw perspectief op coronavirusverdediging
Het team concentreerde zich op verbindingen die bekendstaan om het activeren van een cellulair beschermingsprogramma, gecontroleerd door een eiwit genaamd NRF2. Deze verbindingen—4-octyl itaconate (4OI), bardoxolone (BARD) en sulforafaan (SFN)—werden getest naast selinexor (SEL), een middel dat een transportsysteem blokkeert genaamd XPO1, dat andere eiwitten uit de celkern helpt verplaatsen. In long- en nierscelmodellen verlaagden alle vier de middelen het niveau van SARS-CoV-2 zonder de cellen te beschadigen. Ze werkten ook tegen meerdere zorgelijke varianten. Verrassend genoeg repliceerden de virussen juist beter wanneer NRF2 genetisch werd verwijderd, wat bewijst dat NRF2 van nature beschermend is—maar de middelen bleven toch goed werken, wat aantoont dat hun antivirale kracht via een andere route komt. 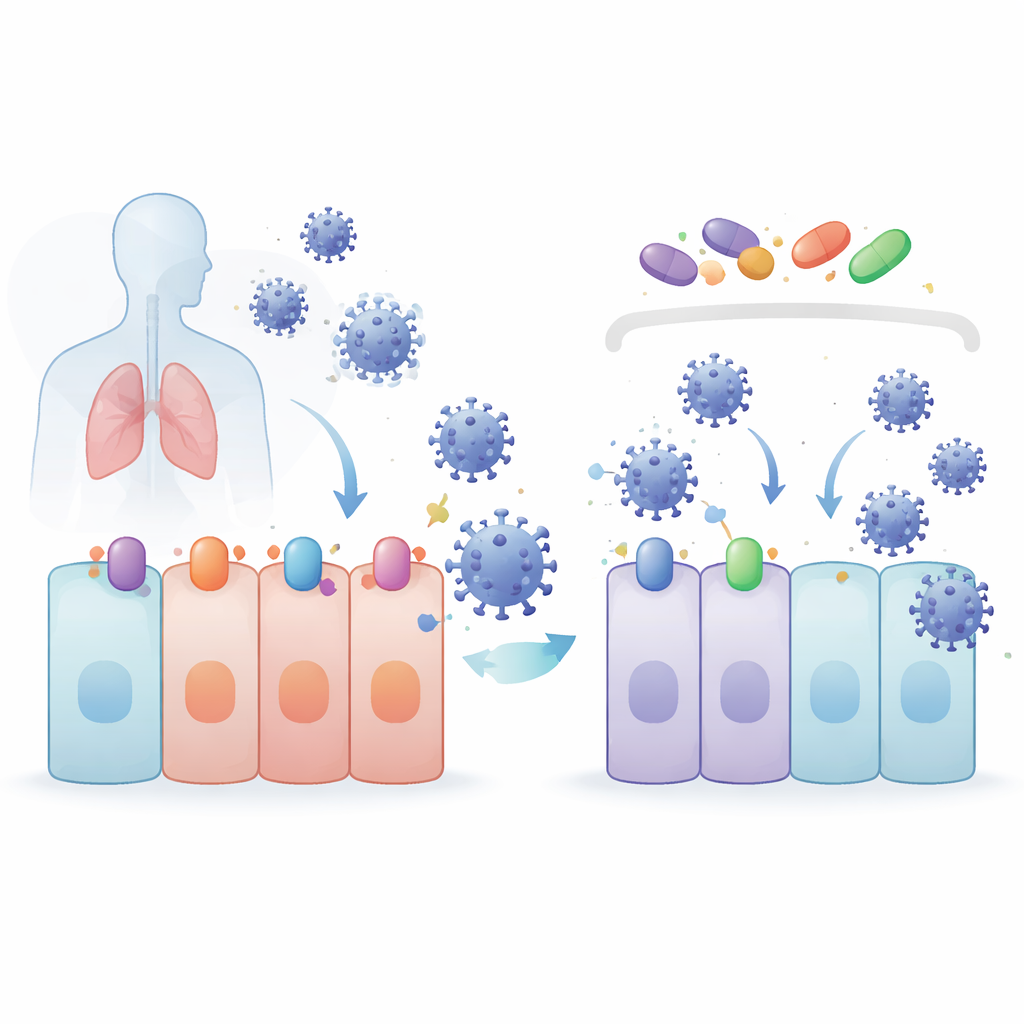
De virale voordeur afsluiten
Coronavirussen beginnen een infectie door aan receptoreiwitten op het celoppervlak te binden. Voor SARS-CoV-2 en verwante virussen is de belangrijkste deur ACE2, met hulp van een knipend enzym genaamd TMPRSS2. Ook het exporteiwit XPO1 lijkt de infectie te bevorderen. De onderzoekers vonden dat 4OI, BARD, SFN en SEL allemaal de hoeveelheden ACE2, TMPRSS2 en XPO1 in menselijke longcellen verlaagden. 4OI en SEL waren vooral krachtig wanneer ze aanwezig waren vóór infectie, en ze blokkeerden de toegang van virusachtige deeltjes die bedekt waren met coronaviruss‑spike-eiwitten. Met andere woorden: deze middelen vertragen het virus niet alleen nadat het binnen is—ze helpen de sloten en hendels verwijderen die het virus nodig heeft om de deur in de eerste plaats te openen.
Hoe cellen belangrijke hulpstoffen van het virus ontmantelen
Dieper gravend lieten de onderzoekers zien dat 4OI de afbraak van ACE2-eiwit versnelt. Onder normale omstandigheden blijft ACE2 urenlang bestaan; met 4OI verdween het van het celoppervlak in een fractie van die tijd. Deze vernietiging vereiste twee cellulaire labelaars, NEDD4L en MDM2, die moleculaire "weggooime"-vlaggetjes aan eiwitten bevestigen. Het blokkeren van deze labelaars verzwakte het vermogen van 4OI om ACE2 te elimineren. Verrassend genoeg was het gebruikelijke eiwitafbraakmechanisme, het proteasoom, niet de belangrijkste route. In plaats daarvan werd ACE2 naar het recycle‑ en afvalsysteem van de cel, het lysosoom, geleid. De middelen verlaagden ook de genactiviteit voor ACE2 en XPO1, deels door de activatie van STAT3 te verminderen, een eiwit dat normaal gesproken de aflezing van het ACE2-gen versterkt. 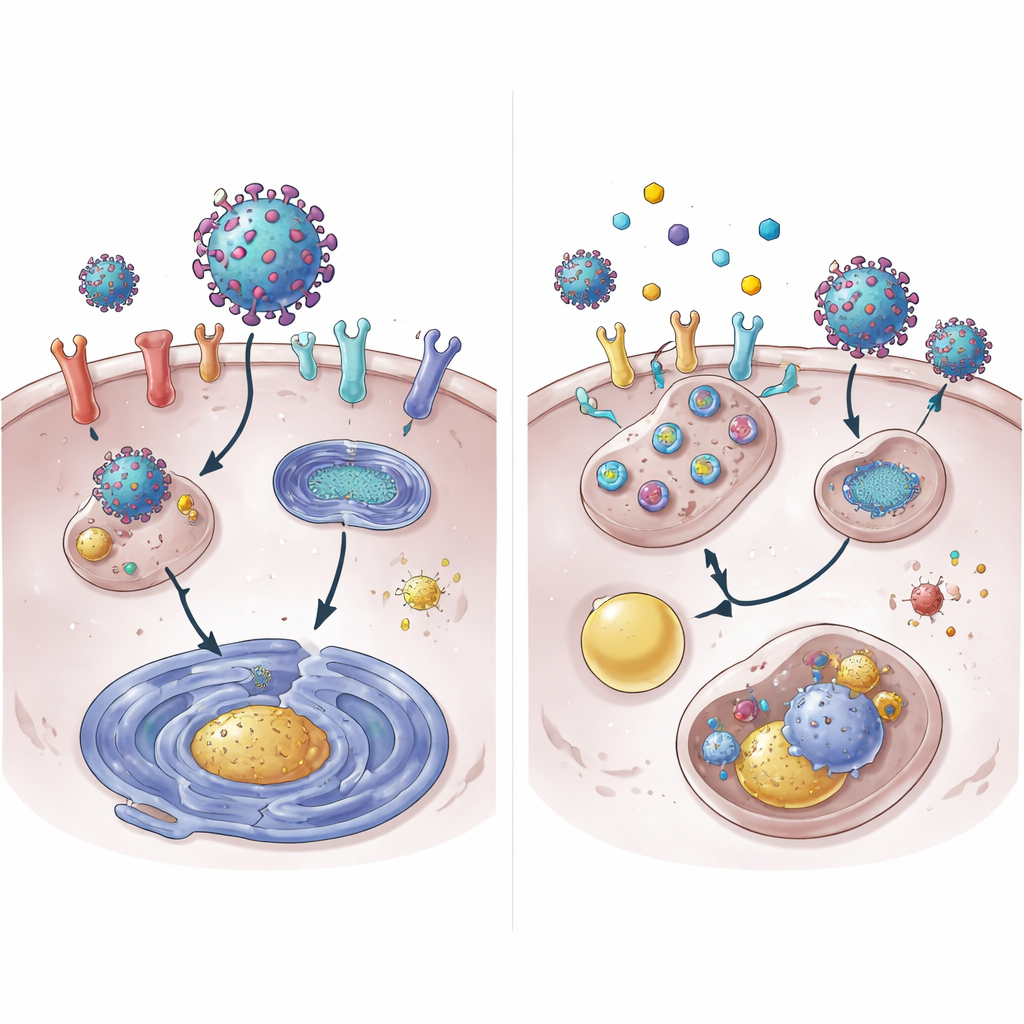
Seizoenscoronavirussen en de XPO1‑verbinding
De wetenschappers richtten zich vervolgens op hCoV-229E, een seizoenscoronavirus dat meestal milde verkoudheden veroorzaakt maar gevaarlijk kan zijn bij mensen met een verzwakt immuunsysteem. Met behulp van aangepaste virussen die oplichten bij replicatie, toonden ze aan dat alle vier de verbindingen 229E sterk onderdrukten in long- en bloedvatcellen, zelfs wanneer NRF2 ontbrak. In tegenstelling tot SARS-CoV-2 gebruikt dit virus een andere receptor, ANPEP, die de middelen niet veranderden. In plaats daarvan volgde hun effect nauwkeurig hoe sterk ze XPO1 verminderden. Het naar beneden brengen van XPO1 zelf verlaagde de 229E-replicatie sterk, en het effect van selinexor verdween vrijwel in deze XPO1-arme cellen. Deze volgorde—SEL het meest afhankelijk van XPO1, BARD het minst—suggereert dat elk middel een iets andere mix van doelen heeft, met XPO1 als een centraal knooppunt voor veel van hun antivirale acties.
Wat dit kan betekenen voor toekomstige behandelingen
Voor niet‑specialisten is de kernboodschap dat het mogelijk is coronavirussen te bestrijden niet alleen door het virus aan te vallen, maar door onze eigen cellen subtiel te herbedraden zodat ze moeilijker te infecteren zijn. In in het laboratorium gekweekte menselijke cellen verwijderden de onderzochte verbindingen cruciale aanhechtingsplaatsen en hulpwegen waarop SARS-CoV-2 en een veelvoorkomend verkoudheidsvirus vertrouwen, en ze deden dit grotendeels zonder het NRF2-pad dat ze aanvankelijk interessant maakte. Hoewel deze bevindingen nog preklinisch zijn en niet direct in medicijnen vertaald kunnen worden, wijzen ze op een veelbelovende weg: middelen die tegelijk virale toegang verminderen, schadelijke ontsteking dempen en weefsels beschermen door een gedeeld netwerk van gastheer‑eiwitten zoals ACE2, TMPRSS2 en XPO1 te targeten.
Bronvermelding: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
Trefwoorden: gastheerrichtte antivirale middelen, coronavirusintocht, ACE2 en TMPRSS2, NRF2-activatoren, XPO1-remming