Clear Sky Science · nl
Ultrasnelle en specifieke miRNA-kwantificering via enkel-molecuul fluorescentie-quenchenkinetiek
Waarom snelle ziektestests ertoe doen
Het stellen van diagnoses voor aandoeningen zoals kanker of virale infecties komt vaak neer op het opsporen van zeer kleine sporen van genetisch materiaal in bloed of andere lichaamsvloeistoffen. De huidige gouden standaardtests kunnen zeer nauwkeurig zijn, maar zijn soms traag, duur of hebben moeite om zeer zeldzame signalen te detecteren. Deze studie introduceert een nieuwe microscoopgebaseerde methode, Q‑FISH, die deze genetische aanwijzingen in minder dan een seconde kan aflezen. Als dit in klinische hulpmiddelen wordt omgezet, zouden die snelheid en precisie het makkelijker kunnen maken om ziekten eerder te ontdekken, de werking van behandelingen te volgen en de zorg per patiënt te personaliseren.
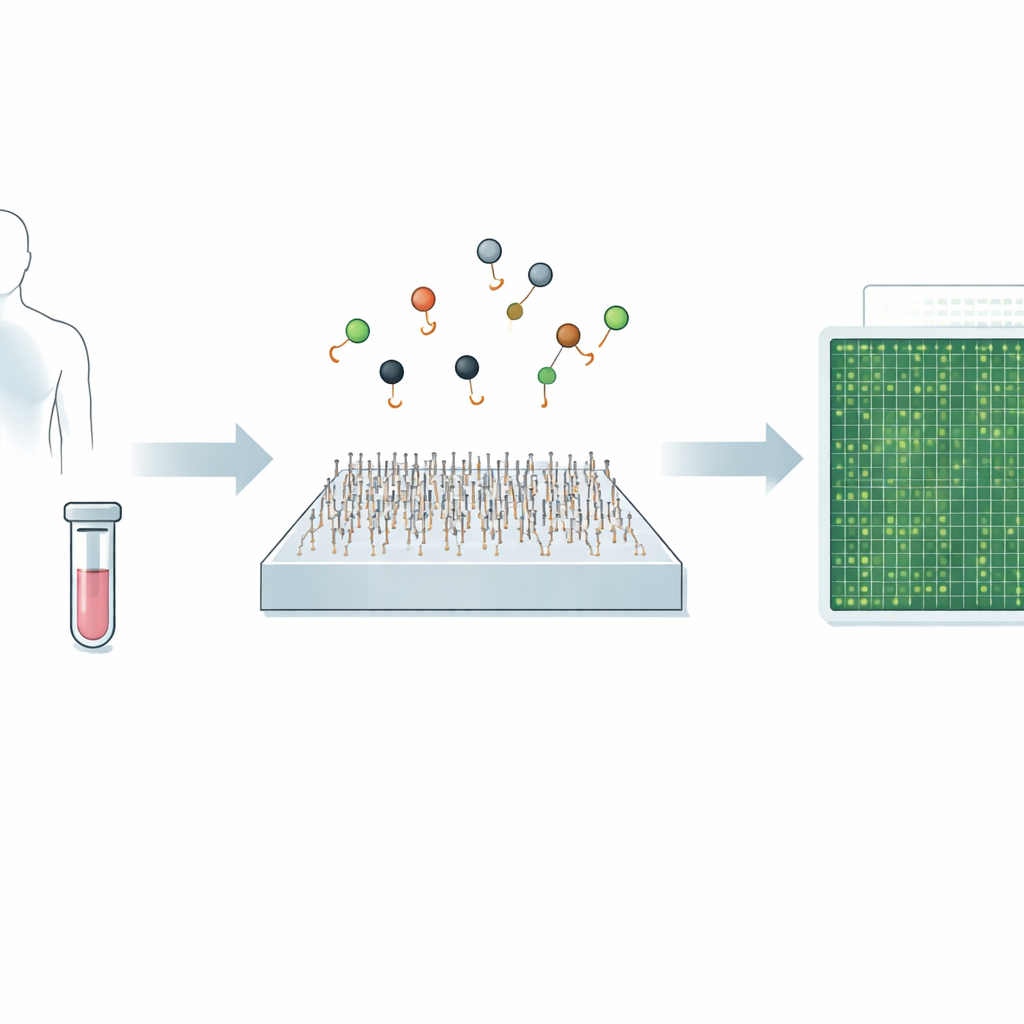
Een nieuwe manier om kleine genetische berichten te zien
Het werk richt zich op microRNAs—korte RNA-fragmenten die helpen bij de regulatie van genexpressie en sterk verbonden zijn met veel vormen van kanker, hartziekten, infecties en hersenaandoeningen. Omdat microRNAs zo klein zijn en vaak slechts in één of twee basen verschillen, hebben standaardmethoden zoals PCR en next‑generation sequencing moeite om nauw verwante types uit elkaar te houden, vooral wanneer ze in zeer lage hoeveelheden aanwezig zijn. Recente enkel-molecuul beeldvormingsbenaderingen verbeterden deze specificiteit door te volgen hoe individuele probes binden en loslaten, maar ze waren nog steeds relatief traag en hadden ongeveer tien minuten nodig om een enkel doel te analyseren.
Het licht zien flikkeren om het juiste doel te vinden
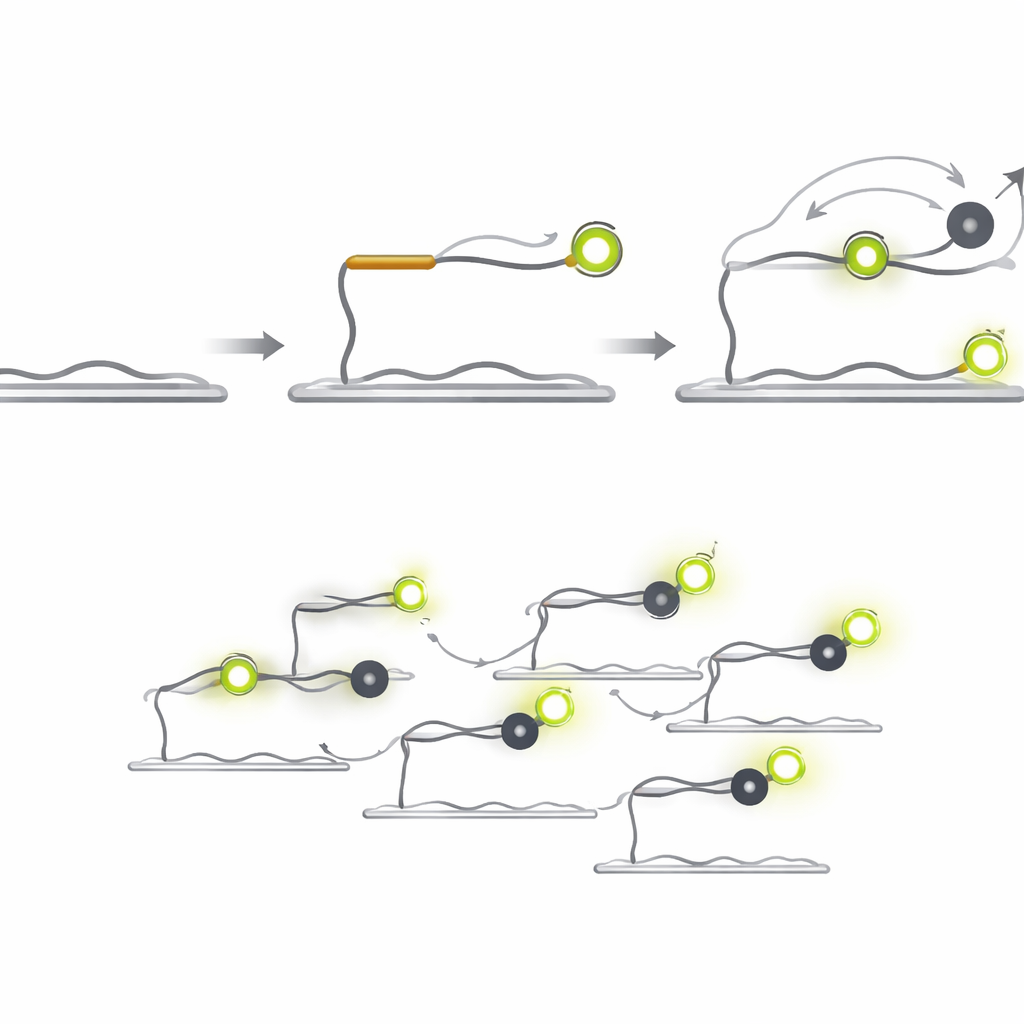
Q‑FISH keert het probleem om door gebruik te maken van de korte lichtflikkeringen van enkelmoleculen. De methode gebruikt twee korte DNA-probes die aangrenzende plaatsen op een doel-microRNA herkennen. De ene probe draagt een fluorescerende kleurstof die oplicht onder een laser, terwijl de andere een “quencher” draagt die het licht absorbeert wanneer deze in de buurt komt. De fluorescerende probe bindt aan het doel en blijft lang genoeg zitten om zichtbaar te zijn, terwijl de quencher-probe zo ontworpen is dat hij snel bindt en weer loslaat. Elke keer dat de quencher naast de kleurstof landt, valt het licht plotseling weg; wanneer hij vertrekt, gaat het licht weer omhoog. Door deze snelle aan‑ en uitflitsen van individuele moleculen op te nemen en te analyseren hoe lang de heldere en gedoofde periodes duren, kan het systeem bepalen of er een echt doel aanwezig is.
Van minuten naar milliseconden
Aangezien de quencher-probe zelf geen licht uitzendt, kan deze in veel hogere concentraties worden gebruikt dan de fluorescerende probes zonder storende achtergrondverlichting te veroorzaken. Het verkorten van de quencher-probe verhoogt de snelheid waarmee hij loslaat, en het verhogen van de concentratie vergroot hoe vaak hij landt. Samen leiden deze ontwerpoverwegingen tot een dramatische toename van de snelheid. In tests met een kankergerelateerd microRNA genaamd let‑7a bereikte Q‑FISH meer dan 70% van zijn maximale detectie-efficiëntie in slechts één seconde observatie. Vergelijkbare enkel-molecuulmethoden hadden tientallen tot honderden seconden nodig om vergelijkbare prestaties te bereiken, waardoor Q‑FISH in praktische zin meer dan 600 keer sneller is.
Bijna identieke signalen scheiden en echte monsters meten
De onderzoekers toonden ook aan dat Q‑FISH onderscheid kan maken tussen verschillende leden van de let‑7 microRNA-familie, die bijna dezelfde sequentie delen maar verschillende rollen hebben in de regulatie van kankergerelateerde genen. Ze gebruikten twee multiplexstrategieën. In de ene werden verschillende quencher-probes na elkaar geïntroduceerd, elk afgestemd op een iets ander microRNA; in de andere werden de probes met verschillende kleuren gelabeld en gelijktijdig geïmaged. In beide gevallen maakte het aflezen van de flikkerpatronen het team mogelijk om binnen ongeveer een seconde correct vast te stellen welk microRNA welke was. Ten slotte pasten ze de methode toe op totaal RNA geëxtraheerd uit menselijk lever- en longweefsel. Door bekende hoeveelheden synthetische microRNAs toe te voegen en de resulterende spots te tellen, bouwden ze kalibratiecurven en bepaalden daarna de natuurlijke niveaus in de weefsels, waarbij duidelijke verschillen tussen organen werden aangetoond.
Wat dit kan betekenen voor toekomstige tests
Samenvattend laat de studie zien dat Q‑FISH specifieke microRNAs met zeer hoge nauwkeurigheid kan identificeren, zelfs wanneer ze bijna identiek aan elkaar zijn, en dat dit kan met snelheden die eerdere enkel-molecuulmethoden ver overtreffen. Hoewel de experimenten werden uitgevoerd op voorbereide monsters met een gespecialiseerde microscoop, zou het onderliggende idee—het gebruiken van snelle licht-quenchevenementen in plaats van alleen langzame binding—kunnen worden aangepast aan veel soorten genetische markers, inclusief tumor-DNA-fragmenten in bloed. Met verdere ontwikkeling en gestroomlijnde monsterbereiding kan deze benadering helpen bij het dichterbij brengen van snelle, sterk gemultiplexte en uiterst gevoelige moleculaire diagnostiek voor het dagelijks klinisch gebruik.
Bronvermelding: Kim, J., Hohng, S. Ultrafast and specific miRNA quantification via single-molecule fluorescence quenching kinetics. Commun Biol 9, 432 (2026). https://doi.org/10.1038/s42003-026-09714-8
Trefwoorden: microRNA detectie, enkel-molecuul beeldvorming, moleculaire diagnostiek, fluorescentie-quenchen, liquid biopsy