Clear Sky Science · nl
Een twee‑stappen strategie gemedieerd door actine stelt Campylobacter jejuni in staat mitochondriale aggregatie en ijzerhomeostase te bevorderen, voor intracellulair overleven en persistentie
Waarom dit kleine gevecht binnen cellen ertoe doet
Voedselvergiftiging door onvoldoende doorbakken kip wordt vaak toegeschreven aan de bacterie Campylobacter jejuni. De meeste mensen herstellen, maar deze microbe is opmerkelijk goed in overleven in verschillende omgevingen, wat de verspreiding van boerderij naar bord bevordert. Deze studie onderzoekt wat er gebeurt wanneer de bacterie schuilt in een vrijlevende amoebe—een veelvoorkomende microbe in zoetwater—en onthult een verrassend verfijnde overlevingstruc die draait om het herschikken van het interne skelet van de cel, het clusteren van energieproducerende ‘krachtcentrales’ genaamd mitochondriën, en het beheersen van ijzer en schadelijke zuurstofchemie. Inzicht in deze verborgen fase van zijn levenscyclus kan wijzen op nieuwe manieren om contaminatie te beteugelen voordat de bacterie mensen bereikt.
Een microbe die oefent in amoeben
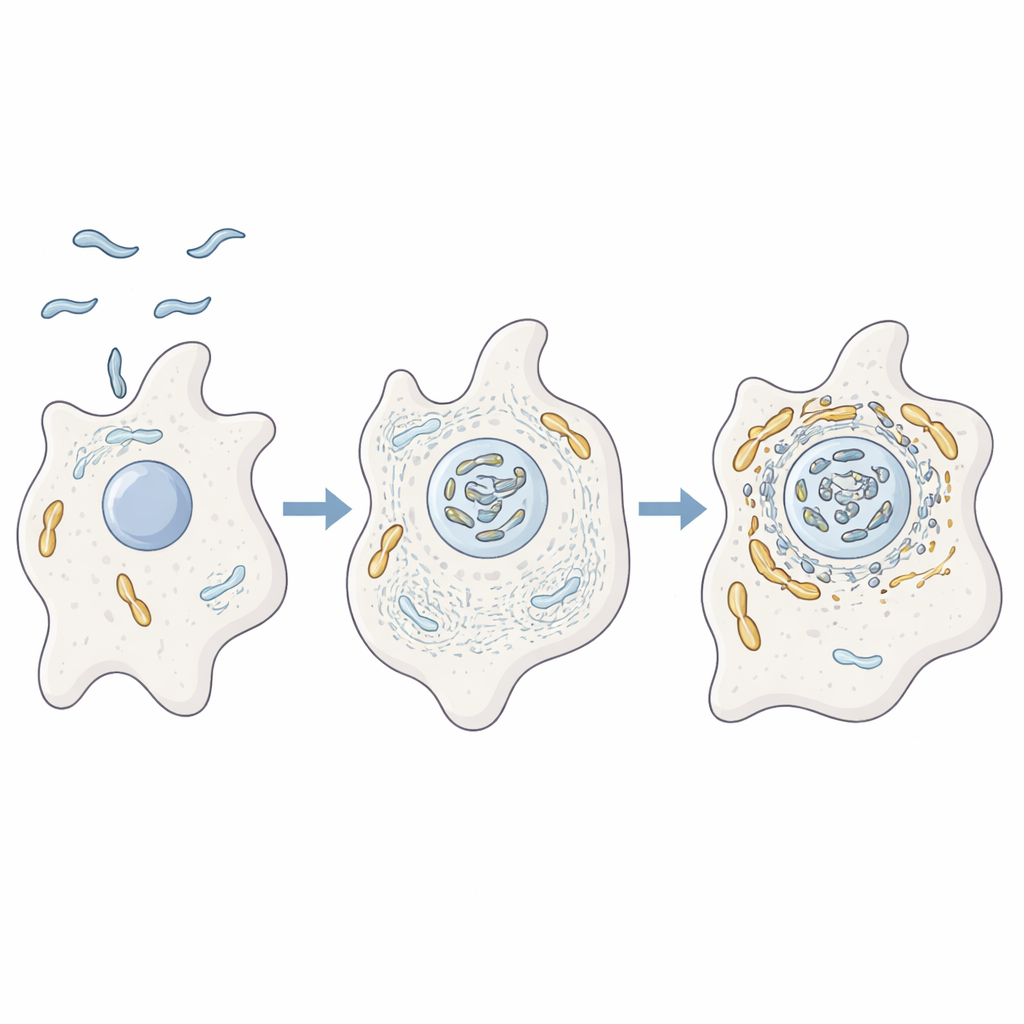
De auteurs bestudeerden hoe C. jejuni zich gedraagt in de amoebe Acanthamoeba castellanii, een eencellig organisme dat in bodem en water leeft. Deze amoeben fungeren als oefenterreinen voor veel ziekteverwekkende bacteriën, doordat ze bescherming bieden tegen ongunstige omstandigheden en desinfectiemiddelen. Met behulp van geavanceerde proteïneanalyse, microscopie en genetische mutanten toonden de onderzoekers aan dat wanneer C. jejuni amoeben infecteert, het nauw geassocieerd raakt met de mitochondriën van de gastheer. Tegelijkertijd is het interne geraamte van de amoebe dat uit actine bestaat, samen met eiwitten die vorm en beweging reguleren, sterk verrijkt in de buurt van deze mitochondriën, wat suggereert dat de bacterie actief de binnenarchitectuur van de gastcel herschikt.
Het buigen van het celskelet om krachtcentrales te verplaatsen
Om te testen of actine deze interactie daadwerkelijk aandrijft, blokkeerde het team het vormen van actinefilamenten of het vertakken tot netwerken. Onder deze omstandigheden verzamelden mitochondriën zich niet langer nabij de bacteriën maar bleven verspreide stippen, en nam het overleven van de bacterie af. Vervolgens concentreerden ze zich op twee bacteriële hulpstoffen, CiaD en CiaI, die via de flagel van de bacterie—een zweepachtige staart—in gastcellen worden geïnjecteerd. CiaD bleek de actinegroei te stimuleren en prikkelige uitsteeksels aan het amoeboppervlak te bevorderen, waardoor de cel de bacteriën makkelijker kan opnemen. Eenmaal binnen werden mitochondriën gezien die zich actine‑afhankelijk rond het bacteriële compartiment groeperen, waardoor de bacterie in een bevoorrechte zone met veel gastheerenergietransductie komt te liggen.
Een moleculaire schakel die mitochondriën opnieuw vormgeeft
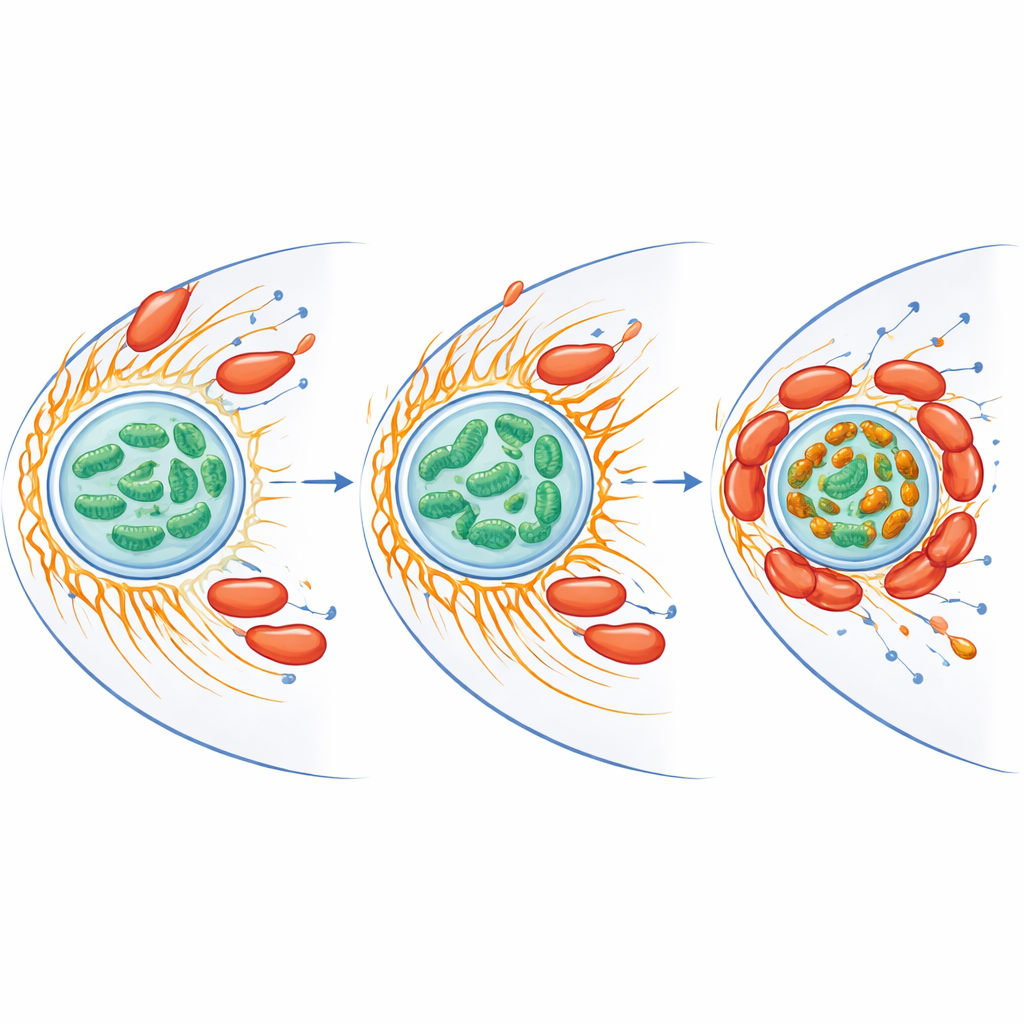
Hoewel CiaD belangrijk is voor de opname, bepaalt CiaI wat daarna gebeurt. Toen de onderzoekers het gen voor CiaI verwijderden, veroorzaakte C. jejuni geen sterke mitochondriale aggregatie meer en overleefde slecht binnen amoeben. Het toevoegen van gezuiverd CiaI gebonden aan kleine bolletjes, zonder levende bacteriën, was voldoende om nabijgelegen mitochondriën te laten fusiëren en clusteren en lokaal actine te verwijderen. Biochemische tests toonden aan dat CiaI energie-dragende moleculen op een cooperatieve manier bindt en zich gedraagt als een moleculaire schakel die zijn activiteit aan of uit kan zetten afhankelijk van de omstandigheden in de gastheer. De auteurs stellen voor dat nadat CiaD‑gedreven actinegroei mitochondriën dichterbij heeft gebracht, CiaI lokale actineafbraak induceert en het mitochondriale netwerk herstructureert tot dichte aggregaten die het bacteriehoudende compartiment omringen.
Het herbedraden van ijzer en stress in de gastheercel
Mitochondriën doen meer dan alleen energie produceren—ze beheren ook ijzer en genereren reactieve zuurstofspecies, chemisch agressieve vormen van zuurstof die microben kunnen doden. De onderzoekers vonden dat infectie de totale vrije ijzerhoeveelheid binnen mitochondriën verminderde, maar tegelijk felle ijzerrijke clusters creëerde waar mitochondriën rond de bacteriën aggregeerden. Eiwitten die betrokken zijn bij ijzerhuishouding en bij verdediging tegen oxidatieve stress namen toe in zowel gastheer als bacterie. Toen het team vrij ijzer verwijderde met een chelerend middel, nam de uitbarsting van reactieve zuurstofspecies van de amoebe af en steeg het overleven van C. jejuni dramatisch. Mitochondriën in geïnfecteerde cellen vertoonden ook een hogere membraanpotentiaal, een teken van verhoogde activiteit, wat suggereert dat de bacterie de krachtcentrales van de gastheer in een toestand duwt die haar eigen persistentie bevordert terwijl schadelijke zuurstofchemie wordt beperkt.
Wat dit betekent voor voedselveiligheid en infectie
Samen genomen ondersteunen de resultaten een twee‑stappen strategie: eerst stimuleert CiaD actinegroei om de bacterie te helpen amoeben binnen te dringen en mitochondriën naar de insteekplaats te trekken; vervolgens breekt CiaI lokaal actine af en remodellert mitochondriën tot ijzerrijke clusters die het bacteriehoudende compartiment omhullen, terwijl de oxidatieve verdediging van de gastheer wordt afgezwakt. Deze fijn afgestelde controle over celvorm, energiegebruik en metaalbalans helpt C. jejuni te overleven binnen amoeben en draagt waarschijnlijk bij aan het vermogen om in de omgeving te persistenten en later mensen te infecteren. Door de sleutelspelers in dit microscopische touwtrekken te onthullen, wijst de studie op nieuwe doelwitten—zoals de Cia‑eiwitten, actine‑mitochondriale contacten of ijzerhandhavingsroutes—die verstoord zouden kunnen worden om contaminatie en ziekte te verminderen.
Bronvermelding: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Trefwoorden: Campylobacter, amoeben, mitochondriën, actine cytoskelet, ijzerhomeostase