Clear Sky Science · nl
Meerdimensionale regulatie van GluK3-kainaatreceptoren wordt bemiddeld door Neto-subunits en zink
Waarom kleine schakelaars in de hersenen belangrijk zijn
Iedere gedachte, herinnering en stemming in de hersenen berust op microscopische schakelaars die geladen deeltjes in en uit zenuwcellen laten stromen. Deze studie richt zich op zo’n schakelaar: een relatief weinig bekend receptorproteïne genaamd GluK3. Door te achterhalen hoe partnerproteïnen en zinkionen het gedrag van GluK3 fijnregelen, geven de bevindingen aanwijzingen over hoe hersencircuits in balans blijven — en hoe die balans kan verschuiven bij aandoeningen zoals epilepsie, depressie en schizofrenie.
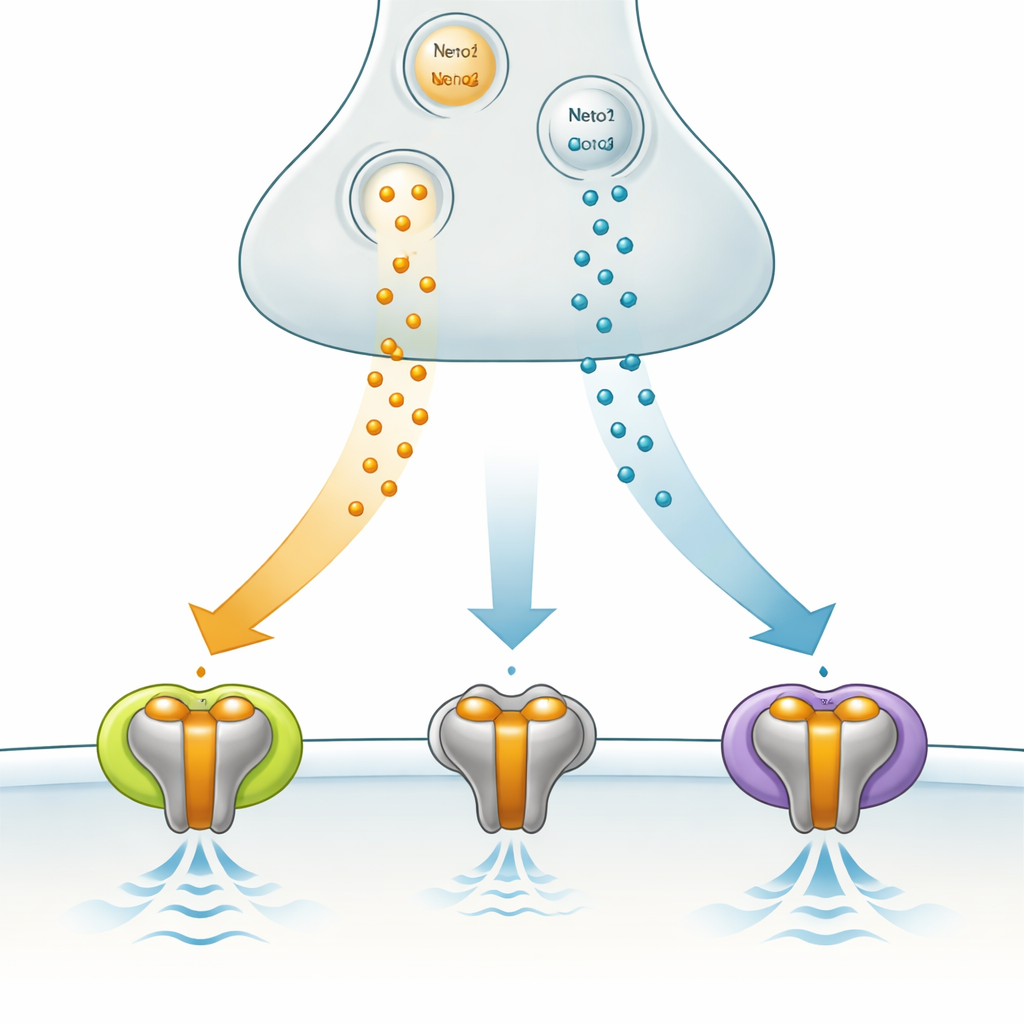
Een gespecialiseerd signaalfilter in de hersenen
GluK3 behoort tot de familie van kainaatreceptoren, onderdeel van de grotere groep glutamaatreceptoren die de snelle communicatie tussen neuronen verzorgen. In tegenstelling tot sommige verwanten schakelt GluK3 signalen niet simpelweg aan of uit; het werkt meer als een filter dat het meest gevoelig is voor korte, sterke uitbarstingen van de boodschapperstof glutamaat. Het komt veel voor in hersengebieden zoals de hippocampus, die belangrijk is voor geheugen en het patroon van netwerkritmes, en veranderingen in GluK3-functie zijn gekoppeld aan angstgerelateerd gedrag. Deze eigenschappen maken GluK3 tot een veelbelovend, maar nog slecht begrepen, doelwit om hersenactiviteit bij gezondheid en ziekte te moduleren.
Hulp‑eiwitten die aan de touwtjes trekken
Het team onderzocht hoe twee hulp‑eiwitten, Neto1 en Neto2, het gedrag van GluK3 veranderen in menselijke cellen die zijn gemodificeerd om deze componenten te produceren. Beide hulpstukken vertraagden hoe snel GluK3 na activatie uitschakelt en verminderden een natuurlijke vorm van interne blokkade die normaal de stroom begrenst. Ze hadden echter tegengestelde effecten op hoe snel GluK3 hergebruikt kan worden. Met Neto1 herstelden receptoren zich snel, klaar om te reageren op snelle, herhaalde signalen. Met Neto2 werd het herstel veel langzamer, wat integratie van signalen over langere intervallen bevordert. In wezen kan een synaps door te kiezen voor verschillende hulp‑eiwitten bepalen of GluK3 zich gedraagt als een detectie‑mechanisme voor snelle vuurgeflechten of als een langzamer, middelen berekenend sensor.
Zink als een tweede regellaag
Veel glutamaat‑vrijmakende zenuweinden geven ook zink af, dat aan receptoren kan binden en hun werking kan veranderen. Eerder werk toonde aan dat zink GluK3 ongewoon versterkt, terwijl het de neiging heeft andere receptortypen te dempen. Hier vonden de auteurs dat deze versterking sterk afhangt van welk Neto‑eiwit aanwezig is. Wanneer GluK3 solitair functioneert, verdubbelt zink ruwweg de tijd dat de receptor actief blijft en neemt de stroom licht toe. Toevoeging van Neto1 dempt dit effect. Daarentegen versterken zink en Neto2, wanneer GluK3 met Neto2 samengaat, samen de stroom sterk, veel meer dan elk afzonderlijk kon doen. Dit suggereert dat synapsen rijk aan Neto2 en zink GluK3‑gemedieerde signalen tijdens intense activiteit sterk kunnen versterken, terwijl Neto1‑rijke synapsen terughoudender blijven.
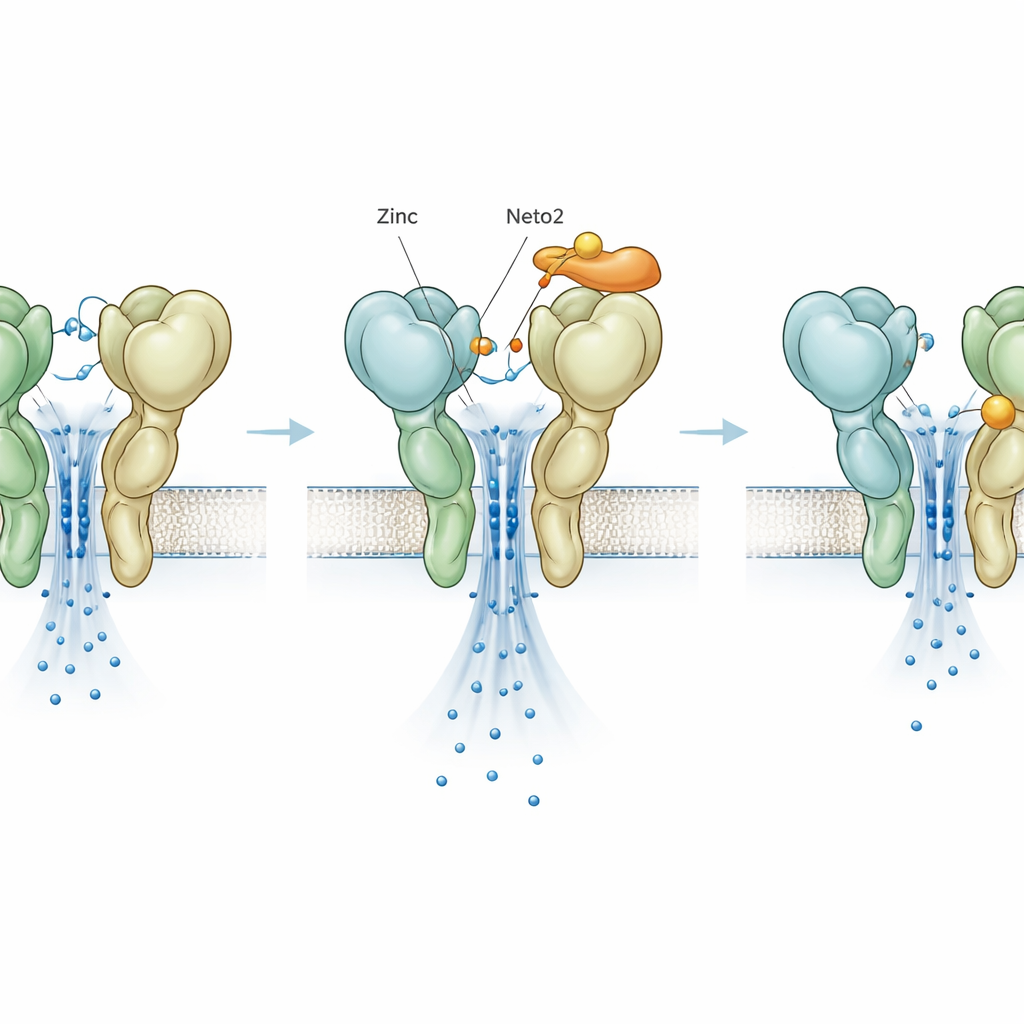
Een verborgen rem blootgelegd door mutatie
Om de effecten van zink los te koppelen van die van de hulp‑eiwitten, maakten de onderzoekers een één‑lettermutatie in GluK3, aangeduid D759G, die een bekend zinkbindend centrum verwijdert. Zoals verwacht maakte deze mutatie de receptor zelf stabieler en langzamer om uit te schakelen, wat het gebruikelijke effect van zink nabootst. Verrassend genoeg versterkte zink deze gemuteerde receptor niet; in plaats daarvan versnelde het de uitschakeling en verminderde de stroom, wat wijst op een tweede, eerder verborgen zinkplaats die als een rem fungeert. Neto1 en Neto2 behielden hun karakteristieke effecten op de mutant, wat laat zien dat hun kerninvloed niet afhangt van de oorspronkelijke zinkplaats. Toch werd zelfs deze nieuw ontdekte remmende zinkwerking verschillend getuned door de twee hulpstukken, wat een extra instelbare knop aan het systeem toevoegt.
Structuur zien achter functie
Om functie aan vorm te koppelen gebruikte het team cryo‑elektronenmicroscopie om de gemuteerde GluK3‑receptor in een niet‑actieve toestand te visualiseren. De beelden toonden dat het glutamaatbindende domein in de D759G‑mutant compacter en dichter verpakt is vergeleken met normale GluK3. Deze structurele aanscherping maakt het waarschijnlijker moeilijker voor de receptor om in een uitschakel‑configuratie te kantelen, wat verklaart waarom de mutant, net als zinkgebonden GluK3, langer actief blijft. Tegelijkertijd lieten de beelden zien dat niet alle delen van de receptor in één vaste opstelling vergrendeld waren, wat wijst op een van nature flexibele architectuur die bijzonder gevoelig is voor kleine chemische prikkels.
Wat dit betekent voor hersengezondheid
Het geheel van bevindingen schetst GluK3 niet als een eenvoudige aan‑/uit‑schakelaar maar als een fijn afstelbaar knooppunt waar glutamaat, hulp‑eiwitten en zink samenkomen. Neto1 en Neto2 bepalen hoe snel signalen vervagen en hoe snel receptoren weer kunnen reageren, terwijl zink de activiteit zowel verder kan versterken als, onder bepaalde omstandigheden, kan remmen via meerdere bindingsplaatsen. Omdat GluK3, Neto‑eiwitten en zink samen voorkomen in synapsen die betrokken zijn bij geheugen en geassocieerd worden met epilepsie en psychiatrische aandoeningen, kan begrip van deze meerdimensionale controle toekomstige therapieën sturen die synaptische signalering subtiel herkalibreren in plaats van deze volledig uit te schakelen.
Bronvermelding: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
Trefwoorden: kainaatreceptoren, GluK3, Neto-eiwitten, synaptisch zink, synaptische plasticiteit